
Рефераты по сексологии
Рефераты по информатике программированию
Рефераты по биологии
Рефераты по экономике
Рефераты по москвоведению
Рефераты по экологии
Краткое содержание произведений
Рефераты по физкультуре и спорту
Топики по английскому языку
Рефераты по математике
Рефераты по музыке
Остальные рефераты
Рефераты по авиации и космонавтике
Рефераты по административному праву
Рефераты по безопасности жизнедеятельности
Рефераты по арбитражному процессу
Рефераты по архитектуре
Рефераты по астрономии
Рефераты по банковскому делу
Рефераты по биржевому делу
Рефераты по ботанике и сельскому хозяйству
Рефераты по бухгалтерскому учету и аудиту
Рефераты по валютным отношениям
Рефераты по ветеринарии
Рефераты для военной кафедры
Рефераты по географии
Рефераты по геодезии
Рефераты по геологии
Рефераты по геополитике
Рефераты по государству и праву
Рефераты по гражданскому праву и процессу
Рефераты по делопроизводству
Рефераты по кредитованию
Рефераты по естествознанию
Рефераты по истории техники
Рефераты по журналистике
Рефераты по зоологии
Рефераты по инвестициям
Рефераты по информатике
Исторические личности
Рефераты по кибернетике
Рефераты по коммуникации и связи
Дипломная работа: Изучение свойств бактериальной суспензии и ее применение в подготовительных процессах переработки мехового сырья
Дипломная работа: Изучение свойств бактериальной суспензии и ее применение в подготовительных процессах переработки мехового сырья
Аннотация
Изучение свойств бактериальной суспензии и ее применение в подготовительных процессах переработки мехового сырья
Выпускная квалификационная работа (дипломная работа). ФСТД, 2006.
Объектом исследования являются природные жиры - нерпичий, свиной, шерстный; синтетический - Tanning oil G; модифицированный- сульфированный рыбий жир и микроорганизмы, выделенные из жира нерпы и шерстного жира, а также из сточных вод после проведения процесса обезжиривания, образцы меховой овчины, шкурки белки.
Цель работы изучение морфолого-культуральных свойств микроорганизмов и исследование их деструктирующей способности.
В результате исследования изучены морфолого-культуральные свойства микроорганизмов и возможность применения микроорганизмов, способных деструктировать жировые вещества для биотехнологического процесса обезжиривания меховой овчины, шкурок белки.
Установлено, что предложенный биотехнологический способ обезжиривания обеспечивает оптимальное удаление жировых веществ с поверхности волосяного покрова и из кожевой ткани.
Разработаны маточные растворы для обезжиривания, позволяющие проводить процесс с меньшим расходом синтетических поверхностно-активных веществ, исключение из рабочего состава формальдегида и карбоната натрия.
Основные технологические показатели: исключение из сточных вод формальдегида, сокращения содержания в сточных водах синтетических поверхностно-активных веществ, сокращение расхода химматериалов.
Область применения – для дальнейшего внедрения в производство.
Экономический эффект достигается за счет сокращения расхода химматериалов и сточных вод.
Введение
В настоящее время экономическое состояние страны ставит перед легкой промышленностью много проблем, среди которых важнейшими являются процессы интенсификации производства и рост его эффективности. Основным источником повышения эффективности мехового производства является проведение исследовательских работ с целью совершенствования технологии с применением новых способов обработки и химических материалов. Интенсификация производства предполагает повышение степени механизации и автоматизации трудоемких работ. Рыночные отношения предъявляют новые требования к предприятиям легкой промышленности. Предприятия должны обеспечить экологическую безопасность окружающей среды от возможных отрицательных последствий, оставаясь кредитоспособными и иметь высокие показатели экономической эффективности производства. Все это ведет к тому, что руководители стремятся внедрять те технологии, которые дают полуфабрикат с высокими показателями качества и параметрами, соответствующими ГОСТам, выработанными с минимальными затратами труда, химматериалов и времени.
Характерной особенностью предприятий кожевенной и меховой промышленности является большое потребление воды и, следовательно, большой объем отработанных жидкостей, так называемых сточных вод, которые относятся к числу наиболее опасных для водоемов.
Содержание загрязнений в сточных водах кожевенно-меховой промышленности столь велико, что в случае поступления последних в водный объект, может вызвать необратимые процессы, включая полное разрушение сложившейся экосистемы. Поэтому проблема экономного использования воды, снижения количества сточных вод, уменьшения их загрязнения в настоящее время является одной из важных проблем.
В связи с этим целью работы являлось изучение деструкции жировых веществ микроорганизмами, выделенных из природных жиров и сточных вод, после процесса обезжиривания и разработка параметров для проведения биотехнологического обезжиривания меховых шкур.
1. Литературный обзор. Применение ферментов в кожевенной и меховой промышленности
Ферментативная обработка сырья одно из наиболее перспективных направлений совершенствования биотехнологических процессов в производстве кожи и меха. Известны работы по использованию ферментов в отмоке, золении, обезволашивании, позволяющие интенсифицировать жидкостные процессы и существенно снизить загрязненность сточных вод.
Основанием для применения ферментов при обработке шкур явились развитие ферментной промышленности и расширение выпуска различных ферментных препаратов, в том числе для меховой промышленности.
Обработка шкур с применением ферментов является более рациональной по сравнению с другими способами, обеспечивает высокое качество кожи — мягкость, легкость, пластичность, кроме того, способствует повышению производительности труда и увеличению выхода площади полуфабриката, что в целом дает значительный экономический эффект [1].
1.1 Применение ферментов в производстве кожи
В кожевенном производстве процессы с применением ферментов протекают на коллагеновых структурах уже подвергшихся изменениям в той или иной степени в результате консервирования, золения и др. процессов.
Отмока сырья с применением ферментов позволяет значительно ускорить и усовершенствовать обводнение кожевенного сырья, особенно законсервированного высушиванием. Далее, ферментативные процессы при обезволашивании кожевенного сырья, процесс мягчения целиком основан на воздействии протеолитических ферментов на дерму – коллаген. Главным вопросом в механизме ферментативного воздействия является выявление роли протеолитических ферментов на коллагеновые структуры кожного покрова различных видов животных и разных их возрастов. Исследования в этой области очень разноречивы. Например, коллаген молодых животных менее устойчив к воздействию протеолитических ферментов, чем коллаген взрослых животных. Также известно, что нативный коллаген и другие белки устойчивы к действию ферментов, а денатурированный коллаген, подвергшийся термической, механической, кислотной, щелочной, солевой обработке, гидролизуется под воздействием протеолитических ферментов [2].
Обработка свиного голья в растворах ферментов способствует освобождению его от остатков корней волоса, эпидермиса, пигмента и кожного жира, смесь которых в кожевенном производстве называется гнейстом. После мягчения гнейст легко удаляется из ткани опавшего голья при легком нажиме. Очистка голья от гнейста необходима, так как при дальнейших обработках он вызывает пятнистость и грубость лицевой поверхности кожи [3].
Были проведены многочисленные исследования, в которых предпринимались попытки использовать протеолитические ферменты. Известно, что в технологии кожи разрыхление структуры достигается сначала обработкой шкур в щелочных растворах (золение), а затем мягчением измененного коллагена протеолитическими ферментами. Мягчению подвергают уже обезволошенные шкуры, поэтому выбор ферментов не лимитируется их действием на волос или на прочность связи волоса с кожевой тканью.
Ряд исследователей считают, что свежий, незолоеный и необработанный нейтральными солями коллаген разрушается панкреатином. Так, кусок шкуры был обработан панкреатином при температуре 400С (панкреатин менялся в течение обработки много раз). Потери азота составили 27 %. Исследования проведенные на изолированных коллагеновых волокнах под контролем микроскопа в камере с подогревом, показали, что 5% раствор панкреатина при 400С в течение 5 часов вызывает растворение коллагеновых волокон. Нативные волокна коллагена сначала распадаются на элементарные волокна, вследствие растворения промежуточного вещества, а затем на отдельные отрезки, которые переходят в раствор [4].
В кожевенном производстве ферментные препараты применяются как мягчения голья, так и для обезволашивания овчины. Наибольшее преимущество ферментов проявляется при использовании их для обезволашивания. При этом устраняется широко применяемый в производстве хромовых кож намазной известково-сульфидный способ обезволашивания. Это позволяет исключить применение вредных химических материалов, повысить культуру производства и производительность труда, упростить очистку сточных вод. Кроме того, ферментная обработка повышает качество снимаемой шерсти. Основной причиной недостаточного применения ферментного метода обезволашивания является высокая стоимость выпускаемых ферментных препаратов [5].
Введение ферментной обработки для свиного сырья способствует:
- более легкому удалению щетины;
- раскрытию коллагеновых пучков и разрыхлению плотной структуры;
- дополнительному обезжириванию сырья.
Указанные факторы обуславливают получение съема щетины стандартного голья, что имеет немаловажное значение для выполнения последующих процессов и операций, особенно золения, придают мягкость и эластичность готовой коже, повышают качество и выход щетины.
Принципы построения методики обезволашивания свиного сырья ферментами такие же, как и для других видов сырья. После промывки, отмоки и обезжиривания следует ферментная обработка при повышенной температуре в присутствии антисептиков ванным, намазным или комбинированным способами [6].
Шкуры овец являются основным видом кожевенного сырья, обезволашивание которого с помощью ферментов находит все большее применение. Одна из главных причин этого сохранение высокого качества шерсти – ценного сырья для текстильной промышленности. Шерсть, снятая бактериологическим (швицеванием или после обработки ферментами) способом, равноценна стриженной шерсти. Для получения шерсти высокого качества за рубежом взамен электростирижки широко применяется ферментный метод обезволашивания для шкур овец тонкорунных, полутонкорунных и других пород. При этом выход шерсти увеличивается на 10-20 % в сравнении с выходом при электростирижке. Повышенный выход шерсти объясняется большей ее длиной из-зи отсутствия разрушения корня и нижней части волоса, которые происходят при известково-сульфидном обезволашивании или остатков волоса при электрострижке. Длина шерсти, снятой ферментным способом, примерно на 10-30 % больше, чем длина шерсти, снятой указанными выше методами.
Преимущества по качеству и общему выходу шерсти сохраняются и при ферментном обезволашивании овчины в кожевенном производстве.
Ферментная обработка овчины с целью последующего удаления шерсти способствует получению высококачественных с большей мягкостью и эластичностью перчаточных и одежных кож, а так же кож для анилиновой отделки вследствие большей чистоты и гладкости лицевой поверхности [7].
Кроме того, в последние годы повысились санитарно-гигиенические требования к очистке сточных вод на кожевенных заводах.
В настоящее время в большинстве стран для обезжиривания кожевенного сырья преимущественно используются бактериальные протезы с разной степенью очистки. Большой интерес для кожевенной промышленности представляют препараты протеолитических ферментов, полученные методом распылительного высушивания. Перспективным является получение препаратов методом многоступенчатого вымораживания.
Испытания проводили на кожевенном заводе при центральном научно-исследовательском институте Кожобувной промышленности. Результаты исследования показали, что препараты обладают хорошей обезволашивающей способностью при обработке различных видов кожевенного сырья. При обработке свиного сырья наблюдалось сильное ослабление связи щетины с дермой за 18-20 часов. В этом случае так же отмечалось хорошее обезжиривание сырья. При ферментативной обработке свиного сырья содержание жира уменьшилось более чем в 4 раза. Для сравнительной оценке обезжиривающей способности препарата были поставлены контрольные опыты, где вместо ферменного препарата использовали специальные обезжиривающие вещества, применяемые в кожевенной промышленности. Исследования показали что, применение ферментных препаратов из культуры Bac. Mesentericus шт. 11-11 позволяет для этого вида сырья исключить последующий процесс обезжиривания полуфабриката [8].
В работе Чурсина В.И., Шапкарина Н.П. исследовано влияние различных ферментов и их комбинаций на свойства дермы. Эксперименты проводили на образцах сырья из яловки легкой развесом 18-24 кг мокросоленого консервирования. В данной работе использованы следующие ферментные препараты: щелочная протеаза с активностью 51300 ед/г(ТУ 64-13-19-89), коллагеназа с активностью 118 ед/г (по данным производителя – ЗАО«Биопрогресс»), протосубтилин Г-Зх с активностью 70 ед/г (ГОСТ 23636-90).
Обработку ферментами проводили при ж.к. 1,5, температуре 30ºС в присутствии 3% карбамида и при рН =9,5. Расход ферментных препаратов устанавливали исходя из их активности, а именно, для коллагеназы-0,1%, для щелочной протеазы-0,5%, для протосубтилина-1% от массы сырья. Обработку проводили в течение 4 ч.Некоторое ослабление волоса было отмечено для образцов, обрабатывавшихся в присутствии коллагеназы. После промывки образцы направляли на золение, которое осуществляли при расходе гидроксида натрия 2% и сульфида натрия 0,6%. Полное удаление шерсти наблюдалось при ферментативной обработке коллагеназой и протосубтилином Г-Зх.Для обезволашивания образцов, которые подвергались обработке щелочной протеазой, расход сульфида натрия увеличивали до1,2%от массы сырья.
Таблица 1- Кинетика процессов и состояния голья на отдельных стадиях обработки
| Расход фермента | Состояни е голья после золения |
Степень пропикеле ванности через 4ч,% |
Прокрас соединениями хрома,% |
Температура сваривания,С | |||
| 1ч | 3ч | 5ч | |||||
| Коллагеназа -0,1% | Сильный нажор, повреждение лицевой мембраны | 100 | 50 | 60 | 90 | 79 | |
|
Протосубтилин Г-Зх-1% |
Сильный нажор, повреждение лицевой мембраны | 80 | 20 | 60 | 80 | 91 | |
| Щелочная протеаза-0,5% | Незначительный нажор,остатки шерсти | 100 | 80 | 100 | 86 | ||
Как следует из таблицы 1, представленные результаты не позволяют дать однозначную интерпретацию действия ферментов на ослабление связи волоса с дермой и протекание последующих процессов, но объясняют многие важные моменты ферментативного обезволашивания. В то же время использование коллагеназы в данной концентрации приводит к повреждению лицевой поверхности и, принимая во внимание незначительную температуру сваривания, вызывает существенную деструкцию коллагеновых фибрилл.
Протосубтилин, относящийся к протеазам общего действия, в большей степени разрушает эпидермис, в состав которого входят глобулярные гликопротеиды, протеогликаны и «мягкие» коллагеновые белки. Это, в свою очередь, вызывает повреждение лицевого слоя голья.
Щелочная протеаза активно гидролизует неколлагеновые белки, способствуя полному освобождению от них волокнистой структуры дермы. Как результат для этих образцов отмечаются высокие значения пропикелеванности и продубленности.
Следует подчеркнуть, что степень поврежденности лицевой поверхности голья в результате ферментной обработки находится в тесной зависимости с содержанием общих белков в отработанных растворах после золения.
Представлялось интересным по той же схеме оценить действие бинарных смесей ферментных препаратов, которое может быть более интенсивным за счет синергетического эффекта и расширения спектра гидролизуемых связей.
На основании полученных результатов выяснилось, что комбинация ферментных препаратов позволяет улучшить как процесс обезволашивания- золения, так и процесс дубления. Хороший эффект обезволашивания достигается при совместной обработке коллагеназой и протосубтилином Г-Зх. Это объясняется более высокой способностью протосубтилина Г-Зх разрушать эпидермальные слои шкуры, облегчая тем самым доступ коллагеназы к коллагеновым белкам, выстилающих волосяные сумки. Однако, отсутствие эффективного воздействия на глобулярные белки неколлагенового характера не позволяет добиться полного извлечения их из структуры дермы, что несколько снижает скорость проникания дубящих солей к активным центрам коллагеновой молекулы.
Наиболее эффективен с этой точки зрения состав, включающий протосубтилин Г-Зх и щелочную протеазу, позволяющий практически полностью очистить дерму от неколлагеновых белков и обеспечить хорошую степень обезволашивания в процессе золения.
Сравнительная оценка действия ферментов показала различия в их влияния на те или иные характеристики голья и полуфабриката. Более эффективными в целях обезволашивания являются диады соответствующих ферментных препаратов, обеспечивающих к тому же более высокие технологические преимущества при проведении преддубильно-дубильных процессов [9].
Шкуры угря по сравнению со шкурами других видов рыб имеют наиболее сложное гистологическое строение, что определяет необходимость специфической их обработки с целью получения кож [10].
В работе Харчуткиной Е.М., Болдовской Е.П., Дормидонтовой О.В. и др. для разработки методики отмоки-обезжиривания шкур угря были выбраны препараты липаза флюозим ГЗх, обеспечивающая достижение хорошего обезжиривающего и отмачивающего эффекта, и протеаза Прок, способствующая обводнению шкур.
При изыскании эффективного способа отмоки обезжиривания шкур угря, позволяющего сохранить рисунок лицевой поверхности, было сделано предположение о возможности совместного использования липазы и протеазы. В связи с этим изучалось влияние последовательности введения ферментных препаратов в обрабатывающую жидкость на активность системы.
Таблица 2- Влияние последовательности введения ферментных препаратов в обрабатывающую жидкость на активность системы
| Вариант | Ферментный препарат | рН | Протеолитическая активность по методу Ансона, ед/г | Липолитическая активность по методу Ота-Ямада, ед/г |
| 1 | Протеаза | 7 | 75,4 | 10000 |
| 2 | Протеаза | 10 | 36,9 | 5000 |
| 3 | Липаза | 7 | 55,4 | 100000 |
| 4 | Липаза | 10 | 33,8 | 95000 |
| 5 | Протеаза + субстрат; липаза | 7 | 73,8 | 80000 |
| 6 | Протеаза + субстрат; липаза | 10 | 50,8 | 70000 |
| 7 | Липаза + субстрат; протеаза | 7 | 29,2 | 140000 |
| 8 | Липаза + субстрат; протеаза | 10 | 9,2 | 133000 |
| 9 | Протеаза + липаза | 7 | 23,1 | 35000 |
| 10 | Протеаза + липаза | 10 | 10,8 | 30000 |
Из данных таблицы 2 видно, что при одновременном дозировании ферментных препаратов активность системы меньше суммарной активности отдельно взятых препаратов.
Рассматривая данное явление, можно предположить, что снижение протеолитической и липолитической активности является результатом изменения структурных особенностей обоих ферментных препаратов (гидролиз связей в цепях молекул ферментов, блокировка функциональных групп активного центра и т.д.), и, как следствие этого, их инактивированием.
Анализируя варианты введения ферментных препаратов в раствор, можно сделать вывод о том, что совместное использование липазы флюозим ГЗх и протеазы Прок возможно лишь при условии их поочередного введения. Данные таблицы 2 показывают также, что введение в субстрат липазы флюозим ГЗх, а затем протеазы Прок приводит к значительному снижению протеолитической активности полиферментной системы, что может объяснятся особенностями механизма каталитической реакции, при которой флюозим ГЗх, воздействуя на субстрат, затрудняет каталитическое действие протеазы Прок.
Результаты эксперимента показали, что применение композиции ферментных препаратов при одновременном их дозировании приводит к снижению протеолитической и липолитической активностей; в случае предварительного введения в обрабатывающую жидкость липазы увеличивается липолитическая активность системы и уменьшается протеолитическая, а в случае предварительного введения в обрабатывающую жидкость протеазы увеличивается протелитическая активность системы и уменьшается липолитическая.
Таким образом, для получения кож из шкур угря рекомендуется технология, предусматривающая отмоку-обезжиривание в водном растворе липазы флюозим ГЗх и протеазы Прок при их последовательном введении. Это позволит получить кожевенный полуфабрикат с сохранением специфического рисунка лицевой поверхности, хорошими прочностными и упруго-пластическими свойствами [11].
В работе С.П. Кочетовой и других использован фермент протакрин, представляющий собой комплексную щелочную протеазу. Для работы использовалось сырье КРС массой 25-30 кг.
Воздействие ферментов на сосочковый и сетчатый слои дермы зависит от глубины и скорости проникания в толщу дермы, поэтому представляют интерес методы, дающие возможность проследить за движением и локализацией ферментов в дерме.
Для исследования изменений, происходящих в дерме под действием ферментов был использован метод количественного анализа структуры по РЭМ- изображению.
Образцы КРС исследовали после отмоки, щелочной подготовки и ферментативного обезволашивания. Для каждого образца проводили послойный анализ изменений, происходящий в сосочковом, пограничном и в сетчатом слое.
На сосочковом слое дермы после отмоки были видны отдельные пучки волокон в плотной упаковке, после щелочной подготовки наблюдалось разделение отдельных пучков на волокна, после ферментативной обработки достигалось разделение отдельных пучков на волокна, становились видны отдельные тонкие волоконца, связующие пучки волокон. В пограничной области дермы между сетчатым и сосочковыми слоями после отмоки были видны плотно упакованные пучки волокон, после щелочной подготовки отдельные пучки в большей степени разделены на волокна, после ферментативной обработки видна система тонких волоконец, связывающих между собой отдельные пучки и более крупные волокна. Разделение же самих пучков на волокна в сетчатом слое практически не наблюдается, но следует отметить, что после ферментативной обработки образуется система тонких волоконец, связующих отдельные пучки.
Анализируя полученные результаты, можно сделать следующие предположения: в сосочковом слое после щелочной подготовки происходит разделение структуры, дополнительное освобождение от глобулярных белков и жировых образований. В пограничном слое (между сосочковым и сетчатым) в сырье после отмоки и после щелочной обработки наблюдается тенденция к увеличению количества мелких пор. Это происходит, видимо, за счет удаления неколлагеновых белков.
Сетчатый слой после щелочной подготовки сырья также характеризуется увеличением мелких пор, в то время как после ферментативной обработки возрастает число крупных пор. Это может быть связано с разделением структуры, образованием больших межпучковых пространств
На основании этого можно сделать вывод, что ферментный препарат проникает в толщу дермы и способствует частичному разделению структуры, выводу глобулярных белков. Изменений самой макроструктуры не происходит [12].
Г.А. Нестеровой и Л.П. Истрановым были проведены исследования закономерностей обезволашивания кожевенного, сырья. Обезволашивающего эффекта можно достигнуть, разрушая корень; волоса путем разрыва в щелочной среде прочных дисульфидных связей, а также разрушением веществ, выстилающих волосяную сумку, что способствует свободному выходу из нее волоса. Одной из составных частей ферментативного обезволашивания является воздействие ферментов на компоненты сложных белков, выстилающих волосяную сумку и белково-углеводистые комплексы.
Более поздние исследования подтвердили важную роль протеаз в разрушении белково-углеводистых комплексов. Для достижения эффекта обезволашивания целесообразно применение ферментов, действующих на различные классы соединений, присутствующих в дерме, белки, углеводы, жировые вещества, причем ведущее место принадлежит протеазам.
Все данные по изучению ферментативного обезволашивания показывают, что длительность процесса определяется скоростью проникания фермента к месту реакции — волосяной сумке.
Основной фактор ускорения процесса - изменение структуры, дермы, способствующее увеличению ее проницаемости и пористости.
Подготовка сырья к действию ферментных препаратов, включающая удаление консервирующих веществ, механические операции удаления подкожно-жировой клетчатки способствуют наилучшему доступу ферментов к структурным элементам дермы и повышению проницаемости ее для больших молекул ферментов. Рекомендуется также обработка щелочами, кислотами, солями. В связи с этим ферментативному обезволашиванию, как правило, предшествует щелочная или ферментативная отмока [13].
Работа С.П. Кочетовой и других посвящена исследованию протеолитической активности собственных ферментов шкур крупного рогатого скота (КРС).
Активность протеолитических ферментов в процессе автолиза в шкуре КРС исследовали независимыми методами: по воздействию экстрактов из шкуры на гидролиз сывороточного альбумина человека и по увеличению аминного азота при расщеплении белков шкуры в процессе естественного автолиза.
Протеолитические ферменты катализируют расщепление белковых веществ до пептидов и дальнейший гидролиз этих пептидов до аминокислот. В связи с этим определение активности протеолитических ферментов шкуры КРС в процессе автолиза можно учитывать по количеству освобождающихся аминных или карбоксильных групп в пробе материала за определенный отрезок времени. Исходя из этого активность определяется по накоплению аминного азота.
Установлено, что в экстрактах при рН 3,6 и 5,6 содержатся ионы магния и цинка в значительном количестве. Ионы кобальта, марганца и меди присутствуют в виде следов. Полученные данные позволяют предположить, что экстракты шкур КРС содержат протеолитические металло-ферменты.
Полученные результаты позволяют предположить, что экстрагируемые из шкуры КРС ферменты можно отнести к классу металлосодержащих тиоловых и карбоксиамидгидролаз [14,15].
Целью работы Г.В. Плешанова, С.В. Янушевской, В.С. Мальцева и В.С. Духанина являлось изучение влияния ферментативной обработки на свойства связующих и пигментных концентратов в качестве связующего используют казеин низших сортов, который по данным, имеет повышенную кислотность, содержит посторонние примеси белкового происхождения, ухудшающие оптические характеристики казеиновых клеев [ 16].
Фигуриным Ю. В. предложен метод обезжиривания свиных шкур с помощью действия комплекса липолитических и протеолитических ферментных препаратов. Установлено, что при ферментативном воздействии комплекса липолитических и протеолитических ферментных препаратов на шкуру происходит ее обезжиривание, уменьшение содержания в ней углеводных компонентов и как следствие этого – хорошее разделение структуры дермы, удаление значительной части неколлагеновых белков. Все это способствует получению кож высокого качества из свиного сырья.
Высокое содержание природного жира в свиных шкурах затрудняет выработку из них высококачественных кож, поэтому при производстве свиных кож необходимо максимальное удаление природного жира, а также хорошее разделение структуры дермы. Для выполнения данных условий наиболее целесообразным является использование комплекса липолитических и протеолитических ферментных препаратов.
Предварительное исследование, проведенные автором, показали, что при совместном использовании комплекса этих ферментных препаратов в подготовительных процессах производства свиных кож в первую очередь необходимо использование щелочной липазы.
В ходе эксперимента ферментные препараты использовались в процессах отмоки и мягчения. Концентрацию щелочных липаз в рабочих жидкостях при исследовании действия комплекса липолитических и протеолитических ферментных препаратов на природный жир свиных шкур определяли количество жира в сырье, сырье после отмоки, голье, полуфабрикате, отработанных жидкостях и в щетине. Полученные результаты, показывают, что используемые ферментные препараты хорошо обезжиривают свиные шкуры и щетину. Хорошее обезжиривающее действие щелочных липаз подтверждается высоким содержанием липидов в отработанных жидкостях в процессе отмоки и мягчения.
В результате проведенной работы установлено, что при ферментативном воздействии комплекса липолитических и протеолитических ферментых препаратов на шкуру происходит ее обезжиривание, уменьшение содержания в ней углеводных компонентов и, как следствие этого, хорошее разделение структуры дермы, удаление значительной части неколлагеновых белков. Все это способствует получению высокого кож качества из свиного сырья [17].
Применение ферментных препаратов при обработке кожевенного сырья является одним из перспективных методов совершенствования технологических процессов.
Целью работы Е.А. Пуртова, Т.Ф. Миронова и Л.М.Лупова являлось изучение возможности применения нейтральной протеазы протосубтилина Г10Х (штамм Bac. Subtilis) в производстве кожи для верха обуви из шкур крупного рогатого скота.
Оптимум действия нейтральной протеазы протосубтилина Г10Х находится в пределах рН 7-7,5, протеолитическая активность по казеину составляет 40 ед./г.
Исследования проводили на полукожнике средней (12 кг) массы мокросоленого способа консервирования.
Для выяснения характера и степени воздействия нейтральной протеазы на структуру дермы полукожника эксперимент осуществляли не препаратах дермы полукожника, приготовленных из отмоченного сырья и голья щелочно-солевой обработки и подвергнутых спирто-эфирной сушке.
Изменение структуры коллагена дермы, происходящие в процессе ферментативной обработки дермы в зависимости от ее продолжительности, концентрации ферментного препарата, предварительной обработки дермы, изучали путем исследования влияния продуктов распада и продуктов выплавления на содержание оксипролина.
В ходе эксперимента было установлено, что действие фермента на структуру коллагена дермы усиливается в случае предварительной щелочной обработки. Незначительное содержание оксипролина в продуктах распада при действие на препараты дермы (до 2,3% в зависимости от характера предварительной обработки и интенсивности ферментативной обработки) свидетельствует о том, что обработка нейтральной протеазой не приводит к распаду коллагена дермы. В продуктах выплавления препаратов дермы, подвергшихся ферментативному воздействию, наблюдается значительное содержание оксипролина, что указывает на появление в структуре дермы под действием ферментов фрагментов структурных элементов коллагена, которые могут перейти в раствор только при гидротермическом воздействии.
Таким образом исследуемая нейтральная протеаза способствует разделению структурных элементов дермы, не вызывая при этом распада коллагена.
Данные разведывательного эксперимента позволяют сделать вывод о возможности использования нейтральной протеазы протосубтилина Г10Х в процессах кожевенного производства.
Исходя из результатов разведывательного эксперимента, были разработаны варианты обработки полукожника, предусматривающие применение нейтральной протеазы протосубтилина Г10Х в процессе подготовки шкур к обезволашиванию и в процессе мягчения. В качестве контрольного варианта использовали типовую методику производства хромовых кож для верха обуви из опойка, выростка и полукожника, предусматирвающую применение в процессе мягчения панкреатина.
При проведении эксперимента в лабораторных условиях исследовали изменение основных структурных элементов шкуры под действием ферментативных обработок по содержанию в отработанных жидкостях оксипролина и общего азота, которое выражалось в процентах от содержания данных компонентов в абсолютно сухой, обезжиренной и обеззоленной шкуре.
Результаты проведенного эксперимента показали, что применение нейтральной протеазы протосубтилина Г10Х в процессе отмоки и мягчения способствует хорошему разделению структурных элементов дермы. Введение обработок данным ферментным препаратом позволяет сократить продолжительность отмоки, уменьшить загрязненность сточных вод благодаря снижению количества сульфида натрия, применяемого в процессе мягчение ферментного препарата животного происхождения панкреатина [18].
1.2 Применение ферментов в производстве меха
В технологии меха ферменты могут применяться и в других процессах, например, при обезжиривании, крашении, отбеливании.
Процесс обезжиривания необходим при обработке многих видов мехового сырья. Так, при обработке меховых и шубных овчин, шкур морского зверя, ондатры, сурка, обезжиривают как волосяной покров, так и кожевую ткань. Учитывая различие в составе жира, находящегося на волосе или в кожевой ткани, используют различные способы обезжиривания. По существующей технологии волосяной покров обезжиривают в водно-щелочных растворах поверхностно-активных веществ, кожевую ткань – в жирорастворителях. Оба эти способа довольно продолжительны и трудоемки, требуют большого расхода воды (первый способ) или специального оборудования (второй способ). Применение липолитических ферментов будет способствовать рационализации процесса, снижению трудоемкости, уменьшению производственного цикла и может быть экономически выгодно, особенно при повторном использовании растворов [19].
Ферменты могут быть также использованы при оксидационном крашении и отбеливании. В обоих случаях необходимо применение окислителей. Известно, что пергидроль – наиболее употребляемый окислитель – резко снижает прочность волоса и кожевой ткани шкур. При использовании оксидаз, которые могут направленно действовать на требуемый агент, прочность волоса не должна снижаться.
Использовать ферменты можно также и для предотвращения пожелтения волоса шкур морских животных. Шкуры морских животных быстро желтеют, что является следствием окисления кислородом воздуха непредельных жиров морских животных. Для защиты шкур от пожелтения их либо упаковывают в герметичные мешки, либо покрывают смазкой, в которую добавлены антиокислители [ 20].
При выделке меховых шкур нельзя применять сильные щелочные воздействия, так как это резко снижает качество волоса. Использование же протеолитических ферментов без предварительной щелоченной обработки малоэффективно, хотя и несколько улучшает качество кожевой ткани. Основным препятствием для использования протеолитических ферментов является их обезволашивающее действие [21].
Наиболее распространен технический панкреатин из поджелудочной железы. В состав этой вытяжки входят следующие ферменты: протеиназа (трипсин), протаминаза (карбоксилпептидаза В), пролиназа, аминопептидаза, карбоксилпептидаза А и дипептидаза, также липаза и амилаза. При обезволашивании и мягчении применяют препараты, получаемые путем выращивания микроорганизмов на питательной среде, например протосубтилин Г3х, липогаетрин Г3х и др., а так же их смеси. Для мягчения в меховом производстве используют препараты микробного происхождения мальтававморин Г10х, оболадающий гликозидазной активностью. Квашение - сложный процесс, где основную роль играют ферменты, как амилаза, расщепляющая крахмал мальтаза и протеолитические. Таким образом, в кожевенном и меховом производстве важной значение имеют гидролазы: протеазы, эстеразы и эфиразы [2].
Ферментативная обработка меховых шкур является более рациональным способом по сравнению с квашением, обеспечивает высокое качество кожевой ткани – мягкость, легкость, пластичность и, кроме того, способствует повышению производительности труда и увеличению выхода площади мехового полуфабриката. [22].
Казалось бы, не может быть и речи об использовании протеолитических ферментов для обработки меховых шкур вследствие их обезволашивающего действия. Несмотря на это, во многих исследованиях по технологии меха испытывали протеолитические препараты. Так, А. В. Раевский, Н. В. Сергеев, И. П. Стефанович показали, что мягчение меховых и шубных овчин трипсином при предварительной известковой обработке дает весьма высокий технологический эффект: происходит разрыхление кожевой ткани, что придает ей мягкость и пластичность. Но при такой обработке уменьшается прочность волоса, нарушается фиксация его в кожевой ткани. Поэтому данный метод не нашел практического применения.
При обработке меховых шкурок пепсином — ферментом, способным воздействовать на белки кожевой ткани в кислой среде, происходит резкая потеря кожевого вещества в результате перехода его в растворимое состояние и снижается прочность шкуры. Пластические свойства кожевой ткани при этом существенно не изменяются [23].
Постоянно растущий спрос на высококачественную шерсть, а также санитарные требования к сточным водам было стимулом того, что в последние годы многие кожевенные заводы Франции, а также предприятия, занимающееся съемкой шерсти с овчин не пригодных для кожевенного и мехового производства, стали применять ферментные препараты, изготовленные фирмой Рапидаз.
На фирме Рапидаз, находящейся в г. Секлен (Societe Rapidase, Seklin Nord France) ферментные препараты для кожевенного производства изготавливают на базе бактериальной протезы, получаемой путем глубинного выращивания бактериальной культуры на жидкой питательной среде, в состав которой входит картофельный крахмал.
Препараты, изготовленные из бактериальной протезы, довольно стойки при хранении, только после 10-12 месячного хранения заметно незначительное уменьшение активности [24].
Способы выполнения ферментной обработки зависит от имеющегося оборудования, производственных площадей и перерабатываемого сырья. Возможно как приспособление используемого оборудования, так и создание высокомеханизированных проходных линий ферментной обработки, особенно сырья овчины [25].
Сынкова А.В., Миронова Т.Ф., Талянского О.В. исследовали влияние температуры и рН обрабатывающей жидкости, а так же механических воздействий на каталитическую способность нейтральной протеазы в процессе обезволашивания овчины.
Отмоку овчины пресно-сухого консервирования осуществляли по известной технологии в течение 24 часов при температуре 18-200С в присутствие сульфита натрия (5 г/л), гексафторсиликата натрия (3 г/л) и ПАВ (1 г/л).
Последующее обезволашивание проводили при различных значениях температуры (18-20 0С; 30-32 0С; 38-40 0С) и рН обрабатывающей жидкости (6; 7; 8; 9) с использованием механических воздействий и в состоянии покоя.
Анализ полученных результатов позволил сделать выводы: при всех вариантах температурного режима и режима механического воздействия эффект полного обезволашивания наиболее быстро достигается при рН 7, таким образом зависимость от рН обезволашивающей способности ферментного препарата коррелирует с данными зависимостями протеолитической активности протеазы Прок.
Наибольшее количество ионогенных групп в дерме наблюдается в случае обезволашивания при рН 7, при данном рН среды протеаза Прок обеспечивает состояние дермы, близкое к изоэлектрическому, в котором набухание коллагена минимально, что облегчает удаление волоса с волосяной сумки.
При температуре обезволашивающей жидкости 30-320С обезволашивание различных топографических участков протекает более равномерно, в течение более длительного периода времени, чем мездреной, что указывает на диффузию протеазы прок в дерму с бахтармяной стороны, наличие мездры на которой препятствует протеканию этого процесса и замедляет достижение обезволашивающего эффекта.
Увеличение температуры обрабатывающей жидкости от 30-320С до 38-400С приводит лишь к незначительному сокращению продолжительности обезволашивания.
Процесс ферментативного обезволашивания протекает медленнее в случае отсутствия механических воздействий [26].
При выполнении ферментативного обезволашивания необходимо строго соблюдать температурный режим обработки не допуская снижения температуры, поскольку резкое изменение температуры обрабатывающей жидкости в сторону уменьшения может привести к инактивации ферментного препарата, в результате требуемый эффект обезволашивания может быть так и недостигнут.
Таким образом, полученные результаты будут способствовать разработке оптимальных параметров процесса ферментативного обезволашивания кожевенного сырья [27].
Целью исследования Г.И Ярецкас, Н.М. Шибаковской, О.Н. Мацевичене, А.К. Струмскене явились разработки технологии применения нового ферментного препарата мальтавоморина Г10Х для обработки шкурок кролика, определение изменений основных структурных элементов кожевой ткани шкурок после обработки ферментом и определение качественных, физико-механических и химических свойств готовых шкурок.
Исследование проводили на шкурках кролика пресно-сухого способа консервирования с толщиной кожевой ткани более 0,7 мм, одинаковых по площади, сортности (2), однородных по плотности. Ферментный препарат мальтавоморин Г10Х использовался для отмоки.
Результаты производственных опытов показали, что применение данного ферментного препарата для отмоки шкурок кролика сокращает процесс на 16-20., улучшает качество готовых шкурок за счет их мягкости и пластичности, почти полностью исключает получение грубых шкурок, снижает количество порванных шкурок и увеличивает выход готовой продукции в среднем на 3,3% по сравнению с типовой методикой выделки [28].
Таким образом, на основании литературного обзора можно сделать вывод, что ферменты для кожевенного и мехового производства имеют огромное значение, так как их применение сокращает длительность процессов, способствует меньшему загрязнению сточных вод, то есть вносит вклад в решение экологических проблем, также обеспечивает увеличение выхода площади готового полуфабриката, позволяет повысить качество готовой продукции, а значит, дает значительный экономический эффект.
2. Объекты и методы исследования
Целью дипломной работы являлось изучение свойств бактериальной суспензии, с последующим применением в подготовительных процессах переработки мехового сырья.
Для выполнения эксперимента был составлен сетевой график, представленный на рисунке 1.
|
 |
||
 |
||
Рисунок 1 – Сетевой график дипломной работы
2.1 Объекты исследования
Объектом исследования в дипломной работе являлись жировые вещества различной химической природы: синтетический – Tanning Oil G; модифицированный – сульфатированный рыбий жир; природные – нерпичий, свиной и шерстный, а также микроорганизмы, выделенные из жира нерпы и шерстного жира (H, Нв, В) и из сточных вод после проведения процесса обезжиривания меховой овчины (3, 7).
TANNING OIL G эмульгатор модифицированный, непротравляющий неокисляющий жир. Применение в процессе жирования овчин после крашения, рекомендуемая концентрация – 2 г/дм3. Преимущество – очень богат питательными жирами.
СУЛЬФАТИРОВАННЫЙ РЫБИЙ ЖИР – продукт сульфатирования жидкой фракции рыбьего жира, густая жидкость от коричневого до темно- коричневого цвета. Получают обработкой ворвани серной кислотой с последующей промывкой и нейтрализацией. Применяется в качестве основных эмульгирующих жиров при составлении смесей для жирования кож всех видов.
СВИНОЙ ЖИР мазеобразная масса от белого до темно- коричневого цвета. Получают вытапливанием, центрифугированием или прессованием. Применяют для производства мыла.
НЕРПИЧИЙ ЖИР жидкость от светло- желтого до темно- коричневого цвета. Получают вытапливанием, экстрагированием, прессованием и сепарированием.
ШЕРСТНЫЙ ЖИР густая пастообразная масса бурого цвета. Внем содержатся кроме воска свободные жирные кислоты, глицериды, белки, слизи, красящие вещества, минеральные примеси.
2.2 Методы исследования
2.2.1 Методика приготовления питательных сред для культивирования микроорганизмов
Мясопептонный агар (МПА)
При культивировании микроорганизмов большое значение имеет обеспечение их соответствующим питанием. Белковой основой для всех сред является питательный бульон. Основой для приготовления мясопептонного бульона (МПБ) является мясная вода. Ее готовят следующим образом: 15 г сухого бульона растворяют в 1 дм3 дистиллированной воды и кипятят 1-3 мин. Для приготовления плотной питательной среды МПА к 1 дм3 МПБ добавляют 2-2,5% агар-агара от объема среды и расплавляют в автоклаве.
Синтетическая среда Рана
В 1 дм3 дистиллированной воды растворяют соли следующего состава (г/дм3): K2НPO4-5,0; CaCl2-1,0; (NH4)3PO4-5,0; NaCl-следы; FeCl3*7H2O-следы; MgSO4 *7H2O-1,0. В качестве источника углерода используют жир в количестве 1 г/дм3. Для приготовления плотной синтетической среды добавляют агар-агар в количестве 2-2,5% от объема жидкой среды и расплавляют в автоклаве при давлении 1атм.
2.2.2 Выделение чистой культуры методом разведений
Разведения делают в стерильной водопроводной воде. Готовят определенный объем этого раствора и стерилизуют при 1 атм. В ходе одного опыта пользуются постоянным коэффициентом разведения, т.к. в этом случае уменьшается вероятность ошибки. Чаще всего делают десятичные разведения. Для этого берут пробирку с 10 см3 стерильного раствора и переносят стерильной пипеткой 1 см3 исследуемого материала в данную пробирку. Суспензию этого разведения тщательно перемешивают с помощью новой стерильной пипетки, вбирая в пипетку и выпуская из нее полученную смесь несколько раз. Это обеспечивает перемешивание суспензии и уменьшает адсорбцию клеток на стенках пипетки. Затем этой же пипеткой берут 1 см3 полученного разведения и переносят его во вторую пробирку. Таким образом, готовят и последующие разведения. Степень разведения определяется предполагаемым количеством микроорганизмов в образце и соответственно число разведений тем больше, чем больше микроорганизмов в исходном субстрате.
Для приготовления каждого разведения обязательно используют отдельную пипетку. Пренебрежение этим правилом может привести к получению ошибочного результата. Ошибка связана с адсорбцией микроорганизмов на стенках пипетки, в результате чего не все клетки удаляются из пипетки при приготовлении соответствующего разведения. Часть клеток, оставшаяся на стенках пипетки, может затем попасть в одно из последующих разведений, что и явится причиной получения завышенного результата.
2.2.3 Посев на агаризованные среды в чашки Петри
В стерильные чашки Петри наливают расплавленную на кипящей водяной бане агаризованную среду, по 20-30 см3 в каждую. Чашки оставляют на горизонтальной поверхности, пока не остынет агар. Для посева отбирают чашки, среда в которых осталась стерильной. Когда используют элективные среды или выделяют и учитывают микроорганизмы, требующие повышенной влажности, посев проводят сразу же или вскоре после застывания агара.
Посев делают из определенных разведений в зависимости от предполагаемого количества микроорганизмов в исследуемом субстрате. Стерильной пипеткой наносят определенный объем (обычно 0,05; 0,1 или 0,2 см3) соответствующего разведения, предварительно тщательно перемешанного, на поверхность агаровой пластинки в чашки Петри. Этот объем распределяют по поверхности среды стерильным шпателем. Затем этим же шпателем проводят по всей поверхности во второй чашке, куда посевной материале вносили. При выявлении микроорганизмов, количество которых в субстрате относительно не велико, посевной материал распределяют по поверхности среды только в одной чашке.
Из каждого исследуемого разведения делают таким образом 2 - 3 параллельных высева. Для параллельных высевов из одного разведения можно пользоваться одной пипеткой и одним шпателем. Для посевов из разных разведений используют другую стерильную пипетку и другой шпатель. Чашки с засеянными средами помещают в термостат, отрегулированный на определенную температуру, благоприятную для развития выявляемых микроорганизмов.
Подсчет выросших колоний проводят через определенное время после посева, которое зависит от скорости роста выявляемых микроорганизмов на используемой в опыте среде и данной температуре.
Подсчитывают количество колоний, выросших при высеве из определенного разведения на двух (одной) чашки Петри. Результаты параллельных высевов суммируют и определяют среднее число колоний, выросших при высеве из этого разведения. Колонии считают, как правило, не открывая чашки. Для удобства отмечают просчитанную колонию точкой на наружной стороне дна чашки, пользуясь стеклографом или чернилами по стеклу. При большом количестве колоний дно чашки делят на секторы, подсчитывают количество колоний в каждом секторе и результаты суммируют или используют полуавтоматические счетчики.
2.2.4 Изучение морфологии бактерий
Морфологические свойства изучают путем микроскопирования окрашенных мазков, приготовленных из исследуемой колонии. При этом отмечаются формы микробных клеток, характер их расположения, наличие спор, капсул, жгутиков тинкториальная способность (окрашивание по методу Грама), определяют чистоту культуры. Кроме просмотра окрашенных мазков, устанавливают наличие жгутиков путем исследования культур на подвижность в препаратах «висячая» или «раздавленная» капля, а также путем посева культуры на полужидкий мясопептонный агар (подвижные бактерии вызывают помутнение агара, а неподвижные растут по уколу).
Из колоний готовят мазки, затем окрашивают по Граму, Трухильо, проводят окраску жгутиков по Леффлеру.
Техника окраски по Граму заключается в следующем:
- На обезжиренном стекле делают мазки микроорганизмов. Мазки высушивают на воздухе и фиксируют под пламенем горелки;
- Мазки окрашивают в течение 1 мин генцианвиолетом;
- Препарат промывают в слабой струе водопроводной воды в течение 2 с.;
- Окрашивают препарат раствором Люголя в течение 1 мин.;
- Промывают препарат слабой струей водопроводной воды;
- Погружают препарат на 30 секунд в 96 %-ный спирт, взбалтывая последний, после чего препарат подсушивают промокательной бумагой;
- Окрашивают мазки раствором фуксина Пфейффера в течение 30 с.;
- Промывают препарат в слабой струе водопроводной воды до исчезновения окраски в стоке, подсушивают промокательной бумагой и микроскопируют.
Грамположительные бактерии окрашиваются в синий или фиолетовый цвет, а грамотрицательные - в красный.
Окраска по Трухильо заключается в следующем:
- Мазок фиксируют жаром;
- Наносят водный раствор малахитовой зелени (2 %) и в течение 3 мин подогревают на спиртовке до отхождения влаги;
- Промывают водой;
- Опускают на 1 мин в 0,25 % - ный водный раствор основного фуксина;
- Промывают водой;
- Высушивают фильтровальной бумагой и микроскопируют.
При таком методе окраски споры окрашиваются в зеленый цвет.
Окраска жгутиков по Леффлеру:
- Мазок заливают на 15-20 минут протравой Леффлера, необходимо следить, чтобы протрава не подсыхала;
- Препарат промывают дистиллированной водой;
- Окрашивают карболовым фуксином Циля в течении 3 минут;
- Высушивают фильтровальной бумагой и микроскопируют.
Клетки и жгутики окрашиваются в красный цвет.
2.2.5 Методика изучения культуральных свойств
Культуральные свойства определяют по характеру роста микробной культуры на плотной и жидкой питательных средах. Характер роста на плотной питательной среде изучают с подробным описанием формы, величины, цвета, поверхности, консистенции, краев и структуры колоний, образованных на синтетической питательной среде.
Микроскопическое изучение колоний проводят под микроскопом. Рассматривая колонии в проходящем свете невооруженным взглядом, описывают следующее: форму колоний; диаметр колоний; цвет, который обуславливается пигментом; рельеф колоний; поверхность; ее блеск, прозрачность; характер краев колоний; структуру колоний, ее консистенцию.
Для определения отношения микроорганизмов к кислороду делают посев уколом на мясопептонный агар (МПА). Посев уколом проводят бактериологической иглой путем прокалывания столбика агара в средней части, следя за тем, чтобы игла нигде не подходила к стенкам пробирки. Не доводя на сантиметр до дна пробирки иглу извлекают и обжигают над пламенем спиртовки.
2.2.6 Метод раздавленной капли
Применяется при исследовании морфологии и подвижности микроорганизмов.
Каплю микробной суспензии помещают на поверхность чистого обезжиренного предметного стекла. При работе с культурой, выросшей на твердой среде, на предметное стекло наносят каплю водопроводной воды, затем стерильной пипеткой берут небольшое количество культуры и перемешивают ее в капле. Покрывное стекло помещают ребром на предметное и осторожно помещают его на суспензию, следя за тем, чтобы между стеклами не было пузырьков воздуха. Избыток жидкости удаляют полоской фильтровальной бумаги.
2.2.7 Определение общего количества микроорганизмов (КОЕ)
Сущность метода заключается в определении в 1 см3 воды общего содержания мезофильных аэробов и факультативных анаэробов при культивировании на синтетической питательной среде при температуре 40 °С в течении 24 часов. Определение начинают с приготовления разведений. Для этого в несколько пробирок наливают 10 см3 стерильной воды. В первую пробирку стерильной пипеткой добавляют 1 см3 исследуемой воды. Новой стерильной пипеткой вносят пробу в пробирку со стерильной водой, после чего этой же пипеткой набирают 1 см3 из приготовленного разведения и переносят во вторую, из второй в третью и т. д. Из каждой пробы делают посев не менее двух различных объемов, выбранных с таким расчетом, чтобы на чашках выросло от 30 до 300 колоний. По истечении 24 часов при температуре 40 °С подсчитывают число выросших колоний. Если выросло большое количество колоний, то дно чашки делят на секторы и подсчет ведут в каждом отдельном секторе. Результаты подсчета выражают в количестве бактерий на 1 см3 анализируемой воды с учетом посеянного объема.
2.2.8 Приготовление бактериальной суспензии
Стерильную жидкую синтетическую среду разливают в стерилизованные конические колбы по 100 см3.
Для получения биомассы исследуемой культуры микроорганизмов, делают посев на скошенный агар.
Подготовленные таким образом культуры инкубируют в термостате 24 ч при температуре (38±5)°С, по окончании чего в пробирки с микроорганизмами вводят 5 см3 соответствующей жидкой синтетической среды, осуществляя процесс механического воздействия. Приготовленную таким образом бактериальную суспензию вносят в колбы, содержащие по 100 см3 соответствующей жидкой синтетической среды.
Культивирование микроорганизмов проводят в термостате при температуре 38±5°С, с переменным механическим воздействием, осуществляемом на Shaker Type, с частотой колебаний 200 об/мин, амплитудой 6 по 2 ч в сутки.
2.2.9 Определение протеолитических свойств микроорганизмов
Протеолитические свойства проявляются выделением во внешнюю среду протеолитических ферментов, которые расщепляют белки до промежуточных продуктов (пептоны, полипептиды, аминокислоты) или до продуктов конечного распада (индол, сероводород, аммиак и др.)
Для выявления протеолитических ферментов исследуемую культуру засевают в питательную среду, содержащую тот или иной белок (МПЖ, молоко и др.)
Посевы в МПЖ культивируют 5...7 суток при комнатной температуре, так как желатин расплавляется в термостате. Микробы, обладающие протеолитическими свойствами, разжижают желатин. Многие протеолитические микроорганизмы дают разный характер разжижения: послойное (идущее ровно, сверху вниз), воронкообразное, кратерообразное, реповидное, в форме чулка и т. д.; микроорганизмы, не обладающие протеолитической способностью, дают в МПЖ рост без разжижения желатина.
2.2.10 Определение индолообразования
Определение индола проводят по методу Морелли, путем использования полосок фильтровальной бумаги, смоченных горячим насыщенным раствором щавелевой кислоты (12 %-ным) и высушенных термостате. Бумажки помещали под пробку в пробирку с бульонной культурой. Культуру выращивают в течении трех суток в термостате, после чего определяют резуьлтаты взаимодействия продуктов жизнедеятельности микроорганизмов с щавелевой кислотой. Положительная реакция – порозовение нижней части бумажки.
2.2.11 Обнаружение сероводорода
Для обнаружения сероводорода делается посев уколом (внутрь столбика) по стенке в агар с ацетатом свинца (МПА с 5 % пептона и 0,25 % ацетата свинца) или в пробирку с МПБ, в которую под пробку над средой помещается полоска стерильной фильтровальной бумаги, пропитанной раствором ацетата свинца. Если исследуемая культура при разложении белка выделяет сероводород, то появляется темно-бурое окрашивание (почернение) по месту укола в плотной среде или на фильтровальной бумажке (в МПБ).
2.2.12 Определение аммиака
Определение аммиака начинают с того, что под пробирку с бульонной культурой помещают розовую лакмусовую бумажку, культуру термостатируют при 370С в течение 1...3 суток. При наличии аммиака лакмусовая индикаторная бумажка приобретает синюю окраску.
2.2.13 Определение редуцирующей способности
Редуцирующую способность определяют посевом культуры на молоко с метиленовым синим. К стерильному молоку добавляют по капле 1 %-ный водный раствор метиленового синего до голубого окрашивания. После культивирования засеянного материала бактерии, обладающие редуцирующей активностью, обесцвечивают лакмусовое молоко (под редукцией понимают химический процесс, заключающийся в отщеплении от вещества кислорода или присоединении к нему водорода).
2.2.14 Определение каталазы
Для определения каталазы в 3...5 суточную бульонную культуру, выращенную в пробирке, вносят 1 см3 3 %-ного раствора пероксида водорода. При наличии фермента каталазы обнаруживают обильное выделение пузырьков отщепленного кислорода, т.е. образуется так называемая “пенистая шапка”.
2.2.15 Определение сахаралитической способности («пестрый» ряд)
Микроорганизмы характеризуются неодинаковой способностью использовать различные соединения углерода для конструктивного и энергетического обмена. Для идентификации большинства гетеротрофных микроорганизмов необходимо определить, какие углеродсодержащие вещества обеспечивают рост данного организма и какими изменениями среды сопровождается его рост.
Как правило, используют следующие углеводы: арабинозу, ксилозу, глюкозу, фруктозу, галактозу, сахарозу, лактозу, мальтозу и спирты – глицерин и маннит.
Готовят среду основного состава на водопроводной воде (г/дм3): пептон – 5,0; гидрофосфат калия (К2НРО4) – 1,0 и индикатор Андреде: кислый фуксин – 0,5; вода – 100 см3; нормальный раствор гидроокиси натрия – 16,4 см3.
Среду разливают в пробирки по 9 мл в каждую и стерилизуют при 1 атм. Углеводы и спирты рекомендуется стерилизовать отдельно при давлении 0,5 атм в виде 10 %-ных водных растворов и добавлять после стерилизации к стерильной среде в количестве 1 %. Растворы дисахаридов лучше стерилизовать фильтрованием, чтобы избежать их гидролиза при высокой температуре.
Среды с углеводами и спиртами засевают одновременно 0,1-0,2 мл суспензии клеток изучаемого микроорганизма и ставят в термостат. Если микроорганизм развивается быстро, то результаты можно регистрировать через 48-96 часов, а если медленно через 7-10 суток.
Визуально по помутнению среды, образованию плёнки, осадка отмечают рост или его отсутствие на всех использованных средах. Рост на средах с этими соединениями может приводить к накоплению органических кислот, нейтральных продуктов и газов. Образование кислот отмечают по изменению рН среды; образование газов по появлению на поверхности среды пены или в толще среды “глазков”, или по газовкам” (маленьким пробиркам – ампулам, опускаемым на дно пробирок с жидкой средой и направленным закрытым концом вверх). При рН 6,0 индикатор Андреде жёлтого, а при рН 7,0 синего цвета (соответственно при восстановлении цвет раствора меняется от соломенного до розового – малинового).
Результаты сравнивают с контрольной средой, не содержащей ни углеводов, ни спиртов.
На основании полученных результатов делают заключение о том, какие углеводы и спирты использует изучаемый организм.
Также могут использоваться среды Гисса с индикатором Андреде, полужидкие среды с индикатором “ВР” (водно-голубой краситель, обесцвеченный розоловой кислотой) и различные индикаторы: нейтральный красный, лакмус, фуксин основной и т.д.
2.2.16 Определение липолитической активности
Липолитические свойства культуры исследуются на среде определённого состава (бульон Штерна). Готовят бульон следующим образом: к 100 см3 МПБ добавляют 1 см3 глицерина и приливают 2см3 свежеприготовленного 10 %-ного водного раствора сульфита натрия, затем по каплям 10 %-й спиртовой раствор основного фуксина (≈ 5 кап.).
Культуры культивируют в термостате при 37 0С. Отмечают изменение цвета среды, рН (лакмусовой бумагой), помутнение, наличие хлопков.
2.2.17 Определение активной реакции среды
Активная реакция среды, т.е. степень ее кислотности или щелочности, характеризуется качественно концентрацией водородных ионов. Концентрацию ионов водорода выражают величиной рН.
Величину рН определяют потенциометрическим методом при помощи потенциометра со стеклянными электродами.
Перед началом измерений прибор включают в сеть при помощи тумблера и дают нагреваться в течение 20 минут.
Электроды перед погружением в раствор тщательно промывают дистиллированной водой и просушивают фильтровальной бумагой.
Вначале измерение проводят по шкале от 0 до 14 (грубое определение), а затем переключают прибор на более узкий интервал.
Перед измерением рН сточную воду хорошо перемешивают и измеряют температуру для введения необходимых поправок.
2.2.18 Гидролиз (омыление) жира
В фарфоровую чашку или стакан помещают 3-4 г жира, 3-4 см3 спирта (образуя гомогенную массу с жиром и щелочью) и 5-6 см3 30%- ного раствора гидроксида натрия. Смесь нагревают на плите или спиртовке с асбестовой сеткой, постоянно перемешивая стеклянной палочкой до однородной массы. Перемешивание прекращают, нагревают еще 10 минут, без кипения смеси. Образование мыла судят по появлению пены на поверхности раствора. Омыление происходит по следующей реакции:
CH2−O −CO −R1 CH2OH
| |
CH− O −CO −R2 + 3 NaOH → CHOH + 2 R1COONa + R2COONa
| |
CH2− O −CO −R1 CH2OH
2.2.19 Определение содержания несвязанных жировых веществ (ГОСТ 26129-84 Шкурки меховые и овчина шубная выделанные. Методы определения несвязанных жировых веществ)
Навеску измельченной кожевой ткани или волоса массой 0,5-0,6 г взвешенною с погрешностью не более 0,0002 г, помещают в бумажную гильзу и закрывают тампоном. Гильзу закрепляют в предварительно доведенной до постоянной массы колбе и соединяют колбу с обратным холодильником. В колбу заливают 50 см3 хлороформа или дихлорэтана. Колбу с растворителем нагревают на электрической плитке с асбестовым покрытием. Продолжительность экстрагирования при анализе кожевой ткани - 45 минут, при анализе волоса – 15-20 минут. Растворитель должен постоянно кипеть и, охлаждаясь и стекая с холодильника, попадать в центр гильзы. В дальнейшем растворитель отгоняют и колбу с жировыми веществами доводят до постоянной массы в сушильном шкафу при температуре 128-130˚С. Продолжительность первой сушки 30 минут, последующих – по 15 минут.
Массовую долю жировых веществ вычисляют по формуле (7):
Х1
= ![]() ×100,
(7)
×100,
(7)
где Х1 массовая доля жировых веществ;
m – масса колбы с экстрагированными веществами, г;
m1 масса пустой колбы, г;
m2 масса навески кожевой ткани или волоса, г
2.2.20 Отбор проб методом асимметрической бахромы
Для сопоставимости результатов исследований различных факторов или технологических параметров необходимо исключить влияние топографии шкуры, полуфабриката или кожи. В этом случае для отбора средней пробы пользуются методом ассиметрической бахромы (МАБ), который заключается в следующем. Намечают необходимое число вариантов исследования и задаются числом образцов (полосок), входящих в группу, предназначаемую для каждого варианта (обычно не менее 4). Чем больше число образцов, тем более достоверным будет среднее значение, характеризующее вариант. Размер образца предопределяется набором физико-механических или физических испытаний, которые предполагается провести, а все образцы должны уложиться в прямоугольник, вписанный в чепрачную часть рисунок 4.
| 5 | 6 |
| 4 | 7 |
| 3 | 8 |
| 2 | 9 |
| 1 | 10 |
| 5 | 11 |
| 4 | 12 |
| 3 | 13 |
| 2 | 14 |
| 1 | 15 |
Рисунок 2 - Схема отбора проб методом асимметрической бахромы
2.2.21 Определение колористических показателей волосяного покрова
Колористические показатели волосяного покрова определяются на приборе «Пульсар». Образцы тщательно расчесываются, накрывают стеклом и фотографируют. Далее работают при установлении кнопки «режим» - 3.
Предварительно прибор прогревают в течение 30 минут, затем нажатием кнопки «сброс» очищают панели вывода.
Первоначально производят калибровку прибора, для этого устанавливают «режим» - 0 (калибровка прибора); «вывод» - 0. Белую пластину помещают на место отражающего образца; черную – на место измеряемого образца, нажимают «пуск », после загорания «Б» извлекают черную пластину. Снова нажимают «пуск», загорается «I» извлекают белую пластину. Устанавливают на индикаторе «режим» - 1; «вывод» - 0 (измерение прозрачных проб) на место прозрачного образца – дистиллированную воду, нажимают пуск.
Для измерения рабочего образца устанавливают пробу. Нажимают «пуск»,
3. Экспериментальная часть
При обработке пушно-мехового и овчинно- шубного сырья на предприятиях меховой промышленности образуется значительное количество сточных вод, характер которых определяется спецификой технологических процессов, осуществляемых в конкретном производстве. Сточные воды образуются после проведения основных жидкостных процессов: отмока, обезжиривание, пикелевание, дубление, крашение и т.д.
В них содержатся химические материалы, как вносимые для проведения технологического процесса, так и образующиеся в результате переработки мехового сырья. Так, после обезжиривания шкур овчины, сточные воды наряду с поверхностно-активными веществами, формальдегидом содержат значительное количество жировых веществ.
В настоящее время все большее применение находит биологическая очистка, основанная на способности микроорганизмов использовать загрязнения в качестве источников питания в результате своей жизнедеятельности. В связи с этим, целью дипломной работы являлось изучение свойств микроорганизмов, выделенных из жировых материалов и из сточных вод после процесса обезжиривания, исследование деструкции жиров на основе метода потенциометрического титрования, а также возможности применения бактериальной суспензии этих микроорганизмов в процессе обезжиривания меховой овчины.
3.1 Изучение морфолого-культуральных свойств микроорганизмов, деструктирующих жировые вещества
Для изучения морфологических и культуральных свойств микроорганизмов методом разведений на мясопептонном агаре (МПА) и на синтетической среде Рана (п.2.2.1), в которой в качестве источника углерода служил нерпичий жир, были выделены чистые культуры микроорганизмов в чашках Петри (п.2.2.2-2.2.3). Культивирование проводили в термостате при температуре (37±0,5)˚С в течение 24. Выделенные культуры были обозначены как: Нв – микроорганизмы, выделенные из жира нерпы; Н микроорганизмы, выделенные из жира нерпы; В – выделенные из шерстного жира; 3,7– культуры микроорганизмов, выделенные из сточных вод после проведения процесса обезжиривания меховой овчины.
По методам Грама, Трухильо (наличие спор), Леффлера (количество жгутиков) (п.п. 2.2.4), были изучены морфологические свойства путем окрашивания и микроскопирования мазков колоний.
Результаты изучения морфолого-культуральных признаков бактерий представлены в таблице 3.
Таблица 3 Сравнительная таблица морфолого-культуральных признаков исследуемых культур
| Характеристики | В | Нв | Н | 3 | 7 |
| Место выделения | Природные жиры: шерстный, нерпичий. | Сточные воды после процесса обезжиривания | |||
| Морфология | Коккобактерии | Палочки, сцепленные между собой | |||
| Подвижность | + | + | + | + | + |
| Окраска по Граму | - | - | - | - | - |
| Окраска по Трухильо | - | - | - | - | - |
| Окраска по Леффлеру | + | + | + | + | + |
| Края колонии | Ровные | ||||
| Профиль колоний | Выпуклый | ||||
| Структура колонии | Однородная | ||||
| Поверхность | Гладкая | ||||
| Прозрачность | Матовая | ||||
| Форма колоний | Круглая | ||||
Микроскопированием окрашенных мазков выявили, что все культуры грамотрицательные, расположение жгутиков перетрихиальное, спор не имеют. Культуры типа 3, 7 представляют собой палочки, сцепленные между бактерий; культуры типа Н, Нв и В по форме были отнесены к коккобактериям - мелким палочкам, близким к овальной форме.
Все культуры имеют точечные круглые колонии грязно–белого цвета, непрозрачные, матовые, с ровными краями, структура колоний однородная, профиль выпуклый.
Для изучения подвижности микроорганизмов была рассмотрена раздавленная капля бактериальной суспензии (п.2.2.6), в результате чего отмечено хаотичное движение бактерий, обусловленное перетрихиальным расположением жгутиков.
Ферментативная способность выделенных культур была определена на основе исследований протеолитической активности (п. 2.2.9), редуцирующей способности (п.2.2.13), анализа на индолообразование (п. 2.2.10), наличие сероводорода (п. 2.2.11), аммиака (п. 2.2.12), каталазы (п.2.2.14).
Результаты исследований, представленные в таблице 2, показали положительную реакцию для всех культур на наличие аммиака, на сероводород и каталазу - отрицательные. Изучение протеолитической активности показало, что все культуры растут без разжижения желатина, не выделяют индол и не обладают редуцирующей способностью, что свидетельствует о низких протеолитических свойствах исследуемых микроорганизмов.
Для изучения биохимической активности бактерий были проведены тесты на способность микробов к ферментативному расщеплению сахаров. В качестве субстратов, для определения ферментативной активности использовались такие сахара, как мальтоза, галактоза, глюкоза, сахароза. Расщепление может происходить на альдегиды, газообразные продукты, кислоты для этого был произведен посев культур на специальные среды с углеводами (п.2.2.15).
На жидкие среды, содержащие различные сахара, был произведен посев по 0,1 см3 суспензии клеток и термостатирование в течение 48 ч при температуре (37±0,5)˚С. Наблюдения показали, что уже к 24 ч окраска сред изменилась от желтой до ярко малиновой и изменение рН.
Для определения липолитической активности был произведен посев на бульон Штерна (п.2.2.16), содержащего в качестве субстрата глицерин. Посев производили следующим образом для получения биомассы исследуемой культуры микроорганизмов, производили посев на скошенную синтетическую среду и культивировали в течение 24 часов при температуре, затем производили смыв полученной биомассы 10 см3 бульона Штерна, и термостатировали при температуре (37±0,5)˚С в течение 96 часов.
На протяжении от 24 до 96 часов культивирования наблюдалось изменение окраски среды, помутнение, наличие пузырьков у поверхности среды, образование осадка и пленки. Уже к 24 часам культивирования было отмечено розовение окраски для всех сред, зараженных культурами. К 48 ч характерно образование пристеночного кольца на поверхности жидкости интенсивной розовой окраски. К 72 ч наблюдалось полное обесцвечивание растворов.
На основании проведенных исследований следует отметить, что исследуемые культуры микроорганизмов обладают липолитической активностью, что связано с вовлечением нерпичьего жира (в качестве источника углерода) в конструктивный и энергетический обмен, что подтверждается переходом окраски бульона из оранжевой в красную и изменением активной реакции среды.
3.2 Изучение деструкции жиров методом потенциометрического титрования
Метод основан на исследовании взаимодействия веществ с протонами потенциометрическим титрованием.
Кривые титрования позволяют:
- определить природу и число ионогенных групп в молекуле жира
- изучить влияние добавок щелочей на ионизацию эфирных групп жира
- оценить глубину и специфичность реакций жиров с микроорганизмами
- количественно определить деструкцию жиров.
Кривые титрования показывают зависимость числа связанных протонов омыленными жирами от рН среды. Величина рН измеряется непосредственно на приборе, число связанных протонов вычисляется. Число связанных ионов определяется по разности между общим числом добавленных ионов и числом свободных ионов в растворе.
Для изучения деструкции были выбраны следующие жиры: нерпичий, сульфатированный рыбий, шерстный, свиной и Tanning oil. Навеску жира, около 1г, взвешенную на аналитических весах, помещали в коническую колбу, в которой проводили щелочной гидролиз (п. 2.2.23), количественно переносили в мерную колбу на 250 см3 и объем доводили до метки дистиллированной водой. Затем отбирали пробу разбавленного гидролизованного жира 4 см3, переносили в стакан на 50 см3 и добавляли 33 см3 дистиллированной воды, для того чтобы мембрана стеклянного электрода была погружена в раствор. Измерение проводили на приборе рН-метр «Анион 7051» путем фиксирования значений рН раствора при добавлении по 0,1 см3 0,1 н. раствора соляной кислоты. Параллельно проводили титрование раствора чистой щелочи (5 см3 30% раствора NaOH переносили в мерную колбу на 250 см3, доводили до метки дистиллированной водой, для анализа брали 4 см3 раствора) и воды. При титровании соли жирной кислоты раствором кислоты происходит реакция обмена с образованием кислоты и соли:
RCOONa + HCl → RCOOH + NaCl
При титровании происходит помутнение раствора в момент образования жирной кислоты.
Для построения кривой титрования проводили расчет параметров по следующим формулам:
B = (CН * V1)/(V1+V) * 1000, где (1)
B – объем HCl, который добавлен к 100 см3 воды
CН – нормальная концентрация кислоты
V1 – добавленный объем,см3
V – начальный объем раствора,см3
C = (- lg B) (2)
D экспериментальное значение рН
Строим график зависимости C от экспериментальных значений рН (находим формулу по линии Тренда, для подстановки в W)
Для изучения деструкции жира микроорганизмами предварительно были приготовлены бактериальные суспензии в колбах Эрленмейера на основе жидкой синтетической среды (п.2.2.8), содержащей около 1 г жира, объемом 200 см3 каждая. Культивирование микроорганизмов проводили в термостате марки (ТС-80М-2) при температуре (37±5)°С, осуществляя переменное механическое воздействие, на встряхивателе «Shaker Type-357», с частотой колебаний 200 об/мин, амплитудой 6 по 1 ч в сутки в течение 48 часов. После чего проводили гидролиз содержимого колбы (п.2.2.23), переносили в мерную колбу на 250 см3, доводили объем до метки дистиллированной водой и тщательно перемешивали. Затем отбирали объем пробы в количестве 4 см3 в стакан на 50 см3, добавляли 33 см3 дистиллированной воды. Титровали 0,1 н раствором соляной кислоты по 0,1 см3 на приборе рН-метр «Анион 7051» при температуре 20,6 ºС. При каждом объеме добавленной кислоты фиксировали значение рН и строили графики зависимости рН от объема и количество функциональных групп (N) от значений рН.
Пример расчета параметров для построения кривых титрования жира при добавлении 3 см3 кислоты (сульфатированный рыбий жир):
B = (0,1 * 3)/(3+33) * 1000 = 8,33
C = (- lg 8,33) =0,9208
D = 12,33 (экспериментальное значение рН)
F = 3мл (количество с известной концентрацией раствора реагента, добавленное к раствору жира, см3)
G = 0,057(объем HCl, который добавлен к водному раствору жира, см3)
H = (-lg G) = 1,243
Строим график зависимости lg B от экспериментальных значений рН для воды (находим формулу по линии Тренда, для подстановки в W)
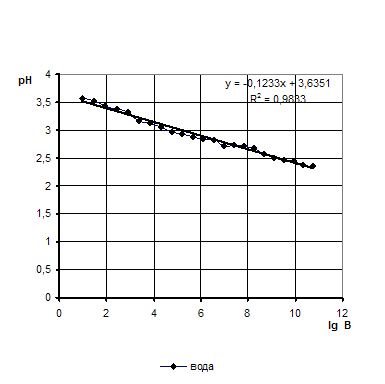
Рисунок 3- Кривая титрования воды 0,1н раствором соляной кислоты
Находим значение W при подстановки значений H в формулу, полученную по линии Тренда, вместо Х
-0,1233Х+3,6351=-0,1233*1,243+3,6351=3, 658
W = 3,658
J = 12,33
K = W- J = 3,658-12,33 = -8,061
L = 8,67
M = 1
N = (0,057*1*10)/0,139 =4,1109
Остальные расчетные данные представлены в таблице 4
Для определения количества групп СООН строим графики в координатах количество функциональных групп – рН.
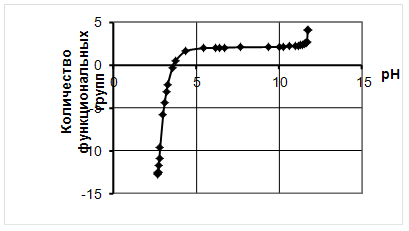
Рисунок 4- График зависимости количества карбоксильных групп от значений рН
Из рисунка 4 видно, что в диапазоне Рн 4,37 до 11,56 кривая представляет собой вид прямой при количестве функциональных групп равных 2. Поэтому данное значение принимаем равным 2.
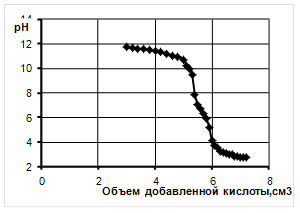
Рисунок 5 - Кривая титрования раствора сульфатированного рыбьего жира соляной кислотой
Кривая титрования омыленного жира характеризуется нейтрализацией избытка щелочи, олеатов и пальмитинатов натрия. Первой вступает в реакцию соль более слабой кислоты, так как полнее идет ее гидролиз. После полного гидролиза соли слабой кислоты в реакцию вступает натриевая соль более сильной кислоты. В результате нейтрализации образуются жирные кислоты, нерастворимые в воде, что сопровождается помутнением раствора. Качественное соотношение жирных кислот в жирах определялось по положению скачка на кривой потенциометрического титрования.
На основании обработки кривых потенциометрического титрования было определено, что исследуемые жиры – нерпичий, свиной, сульфатированный рыбий, шерстный и Tanning oil G могут содержать преимущественно олеиновую пальмитиновую и изомер пальмитиновой кислот. Кроме того в них могут содержаться незначительные количества линолевых кислот, миристиновой, пальмитолеиновой, арахидоновой.
Соли жирных кислот с одинаковым числом углеродных атомов титруются в один скачок - пальмитиновая и пальмитолеиновая. На кривой титрования четко выражены скачки, соответствующие нейтрализации солей жирных кислот. Расчетные данные показали, что количество групп СООН может составлять от 1 до 3 в расчете ммоль на г жира.
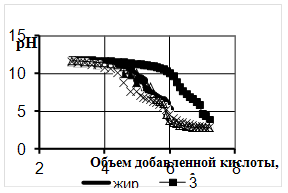
Рисунок 6 – Кривые титрования омыленного сульфатированного рыбьего жира, деструктированного микроорганизмами через 48ч
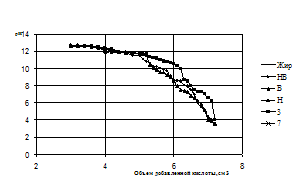
Рисунок 7 – Кривые титрования омыленного нерпичего жира, деструктированного микроорганизмами через 48ч
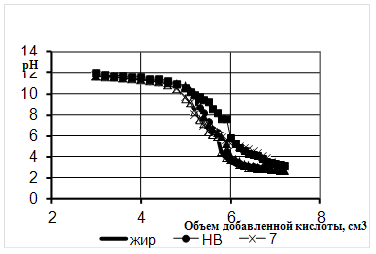
Рисунок 8 - Кривые титрования омыленного свиного жира, деструктированного микроорганизмами через 48ч
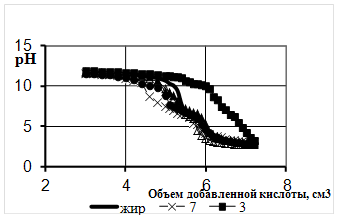
Рисунок 9 - Кривые титрования омыленного шерстного жира, деструктированного микроорганизмами через 48ч
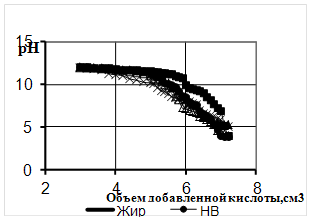
Рисунок 10 - Кривые титрования омыленного Tanning oil G, деструктированного микроорганизмами через 48ч
Деструкция жира под действием микроорганизмов приводит к изменению числа карбонильных групп, то есть происходит расщепление молекулы жирной кислоты, увеличение ее силы, уменьшение длины углеродной цепи, что сопровождается смещением кривой титрования в область меньших значений рН и появлением новых скачков.
Действие микроорганизмов на жир имеет дифференцированный характер. Так штамм 7 дает 3 группы СООН при действии на Tanning oil G, 2- на шерстный жир. Культуры 3 и В полнее всего подвергают деструкции сульфатированный рыбий жир, Нв – свиной жир.
Положение кривой титрования гидролизованного жира, деструктированного микроорганизмами левее, относительно необработанного жира, свидетельствует о том, что деструкция жира проходит замедленно, образованные кислоты расщепляются частично. Количество солей жирных кислот правее кривой титрования необработанного жира свидетельствует об уменьшении количества жирных кислот вследствие их деструкции и превращении в большее число кислот с короткой углеродной цепочкой вплоть до образования альдегидов и выделения углекислого газа.
Таким образом, на основании рисунков 6-10 можно сделать вывод о том, что наиболее активна в отношении деструкции жиров культура 3. Она не только обладает деструктивными свойствами, но и использует жирные кислоты в качестве источника питания в результате своей жизнедеятельности, о чем свидетельствует смещение кривых титрования вправо, относительно необработанного жира и содержание кислот после действия микроорганизмов составило 21,55%.
3.3 Проведение процесса обезжиривания меховой овчины с применением бактериальной суспензии
На данном этапе эксперимента изучалась возможность применения суспензии микроорганизмов для проведения процесса обезжиривания шкурок белки. Основываясь на предыдущем исследовании – изучение деструктирующей способности микроорганизмов была выбрана наиболее активная культура. В качестве продуцента биомассы использовали культуру 3. Количество вводимой биомассы – 104 кл/см3, продолжительность культивирования бактериальной суспензии – 24 часа, количество жира, используемого в качестве источника углерода - 1 г/дм3.
Для определения свойств бактериальной суспензии готовили 1000 см3 бактериальной суспензии, и в течение 120 часов увеличивали ее объем путем введения каждые 24 часа по 200 см3 синтетической среды (п. 2.2.1). Перед каждым введением новой порции синтетической среды определяли показания: кислотность (п.2.2.11), мутность (2.2.10),, активная реакция среды (п. 2.2.16), определение общего количества микроорганизмов (КОЕ) (п.2.2.7). Полученные результаты представлены в таблице 4.
Таблица 4 Влияние продолжительности культивирования на свойства бактериальной суспензии
| Показания | 0 ч | 24ч | 48 ч | 72 ч | 96 ч | 120 ч |
|
Объем бактериальной суспензии, см3 |
1,0 | 1,2 | 1,4 | 1,6 | 1,8 | 2,0 |
|
Кислотность, г/дм3 |
1,5 | 1,44 | 1,56 | 1,5 | 1,5 | 1,52 |
| Мутность | 6,0 | 6,4 | 6,6 | 6,6 | 6,8 | 7,4 |
| рН | 6,98 | 6,99 | 6,98 | 7,06 | 6,99 | 6,99 |
Анализируя полученные данные, можно сделать вывод о том, что при получении необходимого объема бактериальной суспензии значительных изменений в показаниях не происходило, а это значит, что система стабильна.
Для проведения процесса обезжиривания по типовой методике необходимо присутствие в рабочем растворе таких реагентов как, карбонат натрия – 0,5 г/дм3 формальдегид – 0,5 см3/дм3 и СПАВ – 4 г/дм3. Проведение процесса с применением микроорганизмов позволяет полностью исключить формальдегид, карбонат натрия.
Для проведения биотехнологического обезжиривания была приготовлена бактериальная суспензия с разными концентрациями: концентрированный раствор (100%) и с разбавлением 75%, 50% и 25% от объема рабочей ванны.
Таким образом, было приготовлено 5 растворов различных концентраций, состав которых представлен в таблице 5.
Таблица 5 Состав рабочих растворов
| Вид раствора | Расход бактериальной суспензии от объема рабочей ванны, % |
| Типовая методика | |
| Раствор 1 | 100 |
| Раствор 2 | 75 |
| Раствор 3 | 50 |
| Раствор 4 | 25 |
Для проведения обезжиривания образцы меховой овчины, размером 10×10 см были отобраны по методу асимметрической бахромы (п.2.2.22). Процесс обезжиривания меховой овчины проводили в течение 45 минут при температуре 40˚С с переменным механическим воздействием на основе бактериальной суспензии без введения СПАВ, карбоната натрия и формалина. Параллельно проводили обезжиривание по типовой методике.
Перед и после обезжиривания снимали такие показания, как содержание несвязанных жировых веществ в волосе и кожевой ткани, определение колористических показателей волосяного покрова на приборе «Пульсар» (п.2.2.23).
Определение содержания жира в волосе и кожевой ткани проводили на аппарате Зайченко (п.2.2.21).
Пример расчета содержания жировых веществ в кожевой ткани до процесса обезжиривания по типовой методике:
m = 110,7364 г; m1 = 110,6442 г; m2 = 0,5366г
(110,7364-110,6242) ×100%
![]() X1 = =
20,90%
X1 = =
20,90%
0,5366
Остальные данные представлены в таблице 6.
Таблица 6 Содержание жировых веществ в кожевой ткани и в волосяном покрове до и после проведения процесса обезжиривания
|
Вид раствора |
Содержание жировых веществ в кожевой ткани, % | Содержание жировых веществ в волосяном покрове, % | ||
| До обезжиривания | После обезжиривания | До обезжиривания | После обезжиривания | |
| Типовая методика | 20,90 | 12,78 | 11,93 | 5,65 |
| Раствор1 | 17,15 | 8,35 | ||
| Раствор 2 | 17,36 | 10,56 | ||
| Раствор 3 | 18,42 | 11,36 | ||
| Раствор 4 | 19,67 | 11,89 | ||
По приведенным в таблице данным видно, что все растворы обладают обезжиривающим действием. Наибольшим обезжиривающим действием обладал раствор приготовленный по типовой методике, чем остальные растворы, очевидно, причиной этого являлось отсутствие СПАВ в рабочем растворе, присутствие которого необходимо для обезжиривания.
При сравнении обезжиривающего действия между концентрированным и разбавленным рабочим растворами можно отметить, что разница содержания жира в волосе и кожевой ткани после проведения процесса в концентрированных и разбавленных растворах бактериальных суспензий не на много отличается. Таким образом, наиболее оптимальным вариантом проведения обезжиривания меховой овчины в присутствии микроорганизмов является состав ванны 1 (100% расход бактериальной суспензии от объема рабочей ванны).
Колористические показатели волосяного покрова определяли на приборе «Пульсар» (п.2.2.18). Результаты представлены в таблице 7.
Таблица 7 Колористические показатели волосяного покрова до и после процесса обезжиривания
| Вид раствора | Белизна, баллы | Желтизна, баллы | ||
| До обезжиривания | После обезжиривания | До обезжиривания | После обезжиривания | |
| Типовая методика | 80,21 | 82,48 | 25,62 | 19,64 |
| Раствор 1 | 73,90 | 80,90 | 26,95 | 25,37 |
| Раствор 2 | 60,40 | 69,33 | 49,74 | 30,25 |
| Раствор 3 | 73,60 | 77,25 | 31,47 | 26,23 |
| Раствор 4 | 63,75 | 69,21 | 32,15 | 30,37 |
Из таблицы 7 видно, что максимальная величина белизны и желтизны после проведения процесса обезжиривания характерна для образцов, обработанных по типовой методике. Очевидно, это связано с тем, что в обезжиривающей ванне присутствовало СПАВ в количестве 4 г/дм3, которое обладало обезжиривающим и моющим действием. При сравнении данных для растворов 1-4, содержащих только бактериальную суспензию можно сделать вывод, что максимальная величина белизны наблюдалась у образцов после процесса обезжиривания, обработанных в растворе 1 (100% расход бактериальной суспензии от объема рабочей ванны), а минимальная величина белизны у образцов после обезжиривания в растворе 4.
 |
|||
 |
|||
 |
|||
Рисунок 6 - Схема биотехнологического обезжиривания
4. Экономическая часть. Расчет экономической эффективности экобиотехнологического процесса обезжиривания меховой овчины
В настоящее время сложная экологическая обстановка и рыночные отношения предъявляют предприятиям легкой промышленности ряд новых требований: предприятия должны выпускать конкурентоспособную продукцию, удовлетворяющую требованиям потребителя, не оказывая при этом пагубного техногенного воздействия на экосистему.
Предприятия меховой и шубной промышленности занимают одно из первых мест в числе загрязнителей окружающей среды. На всех этапах выделки овчин образуются высокотоксичные воды, содержащие такие контаминанты, как синтетические поверхностные вещества, формальдегид, жировые вещества, минеральные кислоты и соли. В связи с этим широко проводятся научно-исследовательские работы по снижению токсичности отработанных вод после проведения различных процессов в технологическом цикле.
В данной работе предложен метод проведения процесса обезжиривания меховой овчины ферментным препаратом высокой липолитической активности, продуцируемым прокариотическими организмами. Проведение обезжиривания по указанному методу позволяет получить полуфабрикат, удовлетворяющий требованиям ГОСТа и значительно снизить токсичность образуемых сточных вод.
Экономическая эффективность данного процесса достигается за счет снижения затрат на химматериалы, транспортно-заготовительные расходы и прочие затраты.
На первом этапе были рассчитаны затраты на воду и химматериалы согласно формулы (9):
С = V×Ц, (9)
где С затраты на воду, руб;
V – расход материала на 1000 дм2;
Ц – цена за единицу материала, руб
Результаты расчета затрат на воду и химические материалы представлены в таблице 12. Расчеты были произведены на калькуляционную единицу, величина которой для меховой овчины составляет 1000 дм2.
Таблица 5 Затраты на воду и химматериалы на калькуляционную единицу
| Наименование | Единица измерения |
Расход на 1000 дм2 |
Цена за единицу, руб | Затраты, руб | ||||||||
| Типовой вариант |
Новый вариант |
Типовой вариант |
Новый вариант |
|||||||||
| СПАВ | кг | 1,890 | 0,378 | 100,00 | 189,00 | - | ||||||
| Формалин |
дм3 |
0,189 | - | 31,00 | 5,86 | - | ||||||
| Карбонат натрия | кг | 0,189 | - | 30,00 | 5,67 | - | ||||||
| Вода |
м3 |
0,378 | 0,378 | 6,21 | 2,35 | 2,350 | ||||||
|
Калий фосфорнокислый 2-замещенный |
кг | - | 0,567 | 156,00 | - | 88,452 | ||||||
| Кальций хлористый | кг | - | 0,378 | 52,00 | - | 19,656 | ||||||
|
Аммоний фосфорнокислый 1-замещенный |
кг | - | 0,567 | 91,00 | - | 51,597 | ||||||
| Магний сернокислый | кг | - | 0,378 | 38,00 | - | 14,364 | ||||||
| Нерпичий жир | кг | - | 0,378 | 50,00 | - | 18,900 | ||||||
| Итого: | 202,88 | 195,319 | ||||||||||
В представленной таблице показано, что опытный вариант проведения процесса обезжиривания при помощи микробных продуцентов значительно позволяет сократить расходы на химматериалы благодаря исключению из технологического процесса формальдегида, карбоната натрия и СПАВ. Транспортно заготовительные расходы составляют 7% от стоимости химматериалов и составляют для типового варианта 14,2 руб, для нового варианта –13,67 руб.
Прочие затраты составляют 10-15% от суммы предыдущих изменяющихся статей затрат, таким образом, для типового варианта данная величина составила – 30,43 руб., для нового – 29,3 руб.
Изменяющиеся статьи затрат представлены в таблице 13.
Таблица 6 Изменяющиеся статьи затрат на 1000 дм2 готовой продукции
| Статьи затрат | Типовой способ обработки | Предлагаемый способ обработки |
| Стоимость химматериалов | 202,880 | 195,319 |
| Транспортно-заготовительные расходы | 14,200 | 13,670 |
| Прочие затраты | 30,430 | 29,300 |
| Общий итог, руб: | 247,510 | 238,289 |
Из таблицы 13 видно, что экономическая эффективность процесса обезжиривания меховой овчины с использованием бактериальной суспензии достигается за счет снижения затрат на химматериалы с 202,88 до 195,319 руб; на транспортно-заготовительные расходы с 14,2 до 13,67 руб; на прочие затраты с 30,43 до 29,3 руб. Общий итог изменяющихся статей затрат снижается с 247,51 рублей (типовой вариант) до 238,289 руб – при использовании предлагаемой методики проведения процесса обезжиривания (9,221 руб.)
При использовании данного метода остальные статьи затрат, к которым относятся затраты на основную и дополнительную заработную плату, на амортизацию зданий и оборудования и др., остаются неизменными, что обусловлено одинаковыми параметрами проведения данного процесса по разным технологиям – в обоих случаях процесс обезжиривания проводится окуночным методом с продолжительностью – 45 минут.
Годовой экономический эффект рассчитывается по формуле (10):
Э = ![]() , (10)
, (10)
где Э годовой экономический эффект, руб;
С1 – сумма статей затрат для опытной технологии, руб;
С – сумма статей затрат по типовой методике, руб;
Мз – мощность предприятия, дм2/год.
При мощности завода 20 млн.кв.дм. составит 184420 руб, а на 1000 дм2 – 9,22 рублей.
Таким образом, был произведен расчет экономической эффективности процесса, который составил 9,22 рублей на 1000 дм2. Следовательно, применение микроорганизмов-деструкторов жировых веществ при проведении процесса обезжиривания позволит не только снизить токсичность образуемых сточных вод и получить полуфабрикат, удовлетворяющий требованиям ГОСТа, но и значительно сократить затраты на данном этапе выделки меховой овчины.
5. Безопасность жизнедеятельности
5.1 Характеристика естественного и искусственного освещения
Освещение рабочего места – важнейший фактор создания нормальных условий труда. Практически возникает необходимость освещения как естественным, так и искусственным светом. Первый случай характерен для светлого времени суток и при работе в помещениях, в которых имеются проемы в стенах и крыше здания, во втором случае применяются соответствующие осветительные установки искусственного света.
Естественное освещение по своему спектральному составу является наиболее приемлемым. Искусственное же, наоборот, отличается сложностью восприятия его зрительным органом человека. Это связано с тем, что суточные переходные режимы естественной освещенности имеют малую частоту при достаточно высокой (днем) или очень низкой (ночью) интенсивности светового потока, а искусственные – довольно большую частоту при недостаточной в целом освещенности. Поэтому при искусственном освещении начинают возникать неустойчивые зрительные процессы, которые из-за большой частоты сменяемости световых условий накладываются друг на друга, не давая глазу времени адаптироваться к новым условиям. От усиленной деятельности приспособительных механизмов глаза быстро утомляются, что вызывает физическую усталость организма.
Несмотря на это, искусственное освещение необходимо как важнейший фактор для приближения ночных условий труда к дневным. Основное отличие ночных условий труда от дневных состоит в том, что при ночных условиях труда отсутствует достаточная освещенность поля зрения работающих равномерно распределенным световым потоком. Стимулирующее действие света на организм при недостаточной освещенности снижается, поэтому ночные условия труда более тяжелые с физиологической точки зрения. Однако основа естественного и искусственного света общая энергетическая, поэтому их разделение вызвано разницей в спектре и интенсивности. Последнее предположение можно принять только в первом приближении, поскольку спектр естественного света полностью не выяснен и не воспроизведен. Более реально создание световой среды, обеспечивающей психофизиологический комфорт и заданное эмоционально- эстетическое воздействие с учетом светоцветовой доминанты в поле зрения.
Обеспечение освещенности от естественного света связано с устройством проемов для пропускания света. Конструктивно проемы могут быть различными по исполнению и по местонахождению. Поэтому и характер естественного освещения имеет свои особенности: оно может быть боковым, если световые проемы (окна) расположены в наружных стенах; верхним, если световые проемы устроены в крыше; верхнее освещение осуществляется и через фонари – специальные строительные конструктивные детали на крышах или в местах перепадов высот смежных зданий. Возможно и устройство совмещенного естественного освещения путем сочетания бокового и верхнего или фонарного пропускания света в помещение.
Естественное освещение характеризуется отношением естественной освещенности, создаваемой внутри помещения светом неба (непосредственным или отраженным), к значению наружной освещенности земной поверхности от небосвода, выраженное в процентах. Это отношение принято называть коэффициентом естественной освещенности КЕО (е).
Нормирование естественной также различается по расположению проемов и в определенной степени зависит от конструктивных особенностей самих проемов и рядом расположенных строений.
Основное отличие ночных условий труда от дневных состоит в том, что при ночных условиях отсутствует достаточная освещенность поля зрения работающего равномерно распределенным световым потоком. Поэтому необходимо создать такое искусственное освещение, при котором суммарный световой поток от всех установленных в рабочей зоне светильников распределялся равномерно.
Со светотехнической точки зрения при использовании ныне существующих источников света эта задача вполне выполнима. Трудности ее решения связаны с тем, насколько правильно выбрана система искусственного освещения, т.е. каким образом, с каких мест и какого рода установками освещается данный участок. Рекомендуется следующая последовательность осуществления мероприятий по устройству искусственного освещения:
-определение площади, подлежащей освещению, т.е. участка, рабочей зоны, района ведения работ (РВР), а также площади наибольшей концентрации работ (НКР), и установление ее размеров;
-установление нормы освещенности поля зрения в зависимости от разряда с видами освещения;
-выбор системы освещения;
-выбор источников света и расчет потребного их количества;
-выполнение проекта распределения осветительных средств по участку с учетом параметров для установки (углов разворота, склонения, утоненной по конструктивным соображениям высоты подвески) и обеспечения равномерного распределения светового потока по площади.
Площадь участка, подлежащего освещению, устанавливает главный инженер предприятия; он руководствуется правилами определения рабочих зон на каждом рабочем месте и их объединения в производственную площадь или в район работ, если площадь, на которой ведутся работы, обширная и не везде одинаково загружена технологическим процессом. В последнем случае решается вопрос о необходимости освещения всей площади равномерным светом или только мест НКР с помощью общего локализованного освещения.
В зависимости от принятых главным инженером решений рассматривается задача выбора системы освещения и последующий расчет потребного количества светильников. Однако надо иметь в виду следующее: устройство рабочего освещения обязательно во всех случаях должно быть независимым от наличия аварийного освещения; аварийное освещение для продолжения работы необходимо в помещениях и на открытых пространствах, если прекращение работы в нормальном режиме из-за отсутствия рабочего освещения может вызвать взрыв, пожар, отравление людей, опасность травматизма в местах массового из скопления, а также длительное нарушение технологического процесса и др.
Аварийное освещение должно создавать освещенность, составляющую не менее 5 % от нормируемой. Кроме того, аварийное освещение необходимо устраивать для эвакуации людей в местах, опасных для прохода; в том числе в производственных помещениях, где оборудование продолжает работать в темноте, а также по направлениям эвакуации людей из производственных и общественных зданий, где пребывает больше 50 человек. Это освещение должно создавать в проходах освещенность 0,5лк в зданиях и 0,2лк вне их.
В СНиП 23-05-95 «Естественное и искусственное освещение» предусматривается разделение всех работ, даются их характеристики и устанавливаются нормы освещенности.
Искусственное освещение по конструктивному исполнению бывает общим и комбинированным, т.е. состоящим из общего освещения помещения или производственной площади и местного освещения рабочих поверхностей в поле зрения. В свою очередь, общее освещение подразделяется на общее равномерное и общее локализованное (выполненное с учетом расположения рабочих мест). Устройство только местного освещения запрещено, кроме временного (ручными светильниками), относящегося к разряду переносного. Действующими нормами (здесь и далее имеется ввиду СНиП 23-05-95) рекомендуется комбинированное освещение в местах с работами I – IV, Vа и Vб разрядов. Однако при невозможности или нецелесообразности устройства такого освещения допускается одно общее освещение, имеющее некоторые гигиенические и эстетические преимущества.
Комбинированное освещение рекомендуется там, где нужна высокая точность выполняемых работ, где возникают специфические требования к освещению (например, к направлению светового потока), где рабочие поверхности имеют ограниченную площадь или на одно рабочее место приходится большая производственная площадь. Однако, если по нормам требуется устройство дополнительного освещения на единичных рабочих местах, то это на является причиной для отнесения всей производственной площади к виду комбинированного освещения.
Во всех других случаях целесообразно устраивать одно общее освещение. Общее освещение больших производственных площадей, имеющих отдельные участки, которые характеризуются как РВР или НКР, рекомендуется устраивать локализованным к последним, имея в виду, что для остальной площади не требуется такой же, как на участках ведения работ, интенсивности освещения.
Анализ и установление видов освещения некоторым образом определяют систему освещения, так как для различных видов освещения применяются различные источники света. Последние в свою очередь, определяют условия крепления их к рабочим местам или подвеса над площадью. Однако на выбор системы освещения наиболее существенно влияют характер выполняемых работ, т.е. место, где они производятся, возможность размещения осветительных устройств на площади, подлежащей освещению.
Таким образом, выбор системы освещения предполагает решение вопроса о размещении источников света над производственной площадью. При этом часто возникает необходимость одновременного решения вопроса выбора светильников по таким основным характеристикам, как дальность действия, допустимая высота подвеса, единичная мощность и т.п.
Например, для освещения строительных площадок и карьеров используется только группа светильников, позволяющая издалека посылать световой поток на рабочую площадь, тогда как в закрытых цехах или помещениях светильники могут свободно размещаться над местами работы на конструкциях перекрытий и стен и в этом случае нужны другие виды светильников.
При проектировании искусственного освещения система освещения должна быть выбрана до подсчета числа источников света. Этот вопрос согласуется с конструктивными особенностями зданий и сооружений, влияющих и на высоту подвеса светильников, и на их число (в случаях принятия решения крепить светильники на определенные конструктивные детали, количество которых известно), и на единичную мощность. Например, при наличии 50 мест удобного крепления вместо 70 предварительно выбранных источников света, полученных по расчету, правильнее будет отдать предпочтение удобству крепления, заменив источники света на более мощные. Таким образом, система освещения будет выбрана с учетом конструктивных особенностей здания. Равным образом, при выборе системы освещения открытой площади наличие рядом стоящих высоких зданий, труб, возвышенностей предопределит места расположения источников света и в определенной степени из тип, так как возможно понадобятся светильники со значительно большим коэффициентом усиления светового потока в данном направлении.
При выборе источников света предварительно решают вопрос о его виде. Существуют следующие виды источников света (ИС): лампы накаливания, люминесцентные лампы, разрядные лампы высокого давления, ксеноновые лампы, лампы для специального облучения.
Лампы накаливания (ЛН). Этот вид ламп все еще преобладает и производится в широком ассортименте, несмотря на имеющиеся в производстве более экономичные ИС.
Отличительная особенность ЛН состоит в том, что они включаются в сеть без дополнительных пусковых приспособлений и могут работать при значительных отклонениях напряжения сети от номинального, а также практически не зависят от условий окружающей среды и температуры, компактны, световой поток их к концу срока службы снижается незначительно (приблизительно на 15%). Однако ЛН имеют относительно низкую световую отдачу и в их спектре преобладает желто-красная часть. Характеризуются ЛН номинальными значениями напряжения, мощности и светового потока. На их выбор может оказывать влияние размер ламп: полная длина L (стеклянная колба вместе с цоколем), диаметр D и высота светового центра H (от резьбового цоколя до центра нити накаливания).
В характеристике ЛН имеет большое значение величина подводимого напряжения. С повышением напряжения возрастает температура накала нити и свет становится белее, быстро возрастает световой поток, но одновременно с этим резко уменьшается срок службы ламп.
Лампы накаливания могут быть подобраны по каталогам или по специальной справочной светотехнической литературе.
Для условий производства как зарытых рабочих площадей, так и открытых участков имеет значение направленное усиление светового потока, что наблюдается при наличии отражающих поверхностей. К такого рода ЛН относятся лампы-светильники с зеркальными или диффузными отражающими слоями на колбах. Их применение связано с предварительной оценкой распределения светового потока от таких ламп по освещаемой поверхности.
Весьма перспективной (ныне уже широко применяемой) разновидностью ЛН являются галогенные лампы накаливания. Они имеют трубчатую форму с цилиндрическими, керамическими или ножевыми металлическими цоколями по концам и отличаются от обычных ЛН особой компактностью, более белым светом, улучшенной цветопередачей и вдвое большим сроком службы. Эти лампы при эксплуатации должны находиться только в горизонтальном положении. Отклонение допускается не более 4B.
Люминесцентные лампы (ЛЛ). Они широко применяются в осветительных установках низкого давления. Эти лампы имеют высокую световую отдачу (до 75 лм/Вт), большой срок службы (до 10 000 ч), лучшую, чем у ЛН цветопередачу, относительную малую яркость (хотя и создают ослепленность). Высокая световая отдача и большой срок службы ЛЛ, как и газоразрядных ламп высокого давления, делают их в большинстве случаев более экономичными по сравнению с лампами накаливания. Однако для ЛЛ требуются более сложная схема включения, ограничения температурных условий для нормальной работы (при температурах меньше 10BС они не зажигаются) и групповое использование для снижения вредных влияний пульсации светового потока. К недостаткам ЛЛ относятся также малая единичная мощность при больших размерах ламп и значительное снижение светового потока к концу срока службы.
Большое значение имеет правильный выбор спектрального типа ламп. Люминесцентные лампы намного превосходят по качеству цветопередачи ЛН, однако не полностью приближаются к естественному свету из-за малого излучения в красной части спектра. В настоящее время ближе других к естественному спектру считаются лампы ЛХБЦ.
В последнее время при производстве ЛЛ низкого давления большое внимание уделяется экономии сырья для их изготовления. Выпущена серия энергоэкономичных ЛЛ мощностью 58 Вт различных цветностей, выполненных в колбе диаметром 26мм. В связи с этим на 7-8% уменьшилась потребляемая лампой мощность при прежнем уровне светового потока. Кроме того, существенно снизилось потребление основных материалов: стекла, алюминия, люминофора. Эти лампы предназначены для общего и местного освещения помещений промышленных и общественных зданий, лампы цветности ЕЦ для освещения жилых и общественных зданий.
Газоразрядные лампы высокого давления (ГЛВД). Эти лампы применяются в условиях, когда требуется высокая световая отдача при компактности источника света и стойкости к условиям внешней среды. Среди этих типов ламп в настоящее время расширяется производство металлогенных ламп (МГЛ) (мощность 250-2000 Вт) и натриевых ламп НЛВД (70,100,150 Вт), а также зеркальных МГЛ типа ДРИЗ (мощность 250, 400, 700 Вт).
Металлогенные лампы внешне отличаются от ламп ДРЛ отсутствием люминофорного покрытия колбы; кроме того, они имеют высокую светоотдачу (до 100 лм/Вт) и лучший спектральный состав света. Однако срок службы их меньше, чем у ДРЛ и схема включения сложнее. Основное применение ДРИ находят в качестве источников света для щелевых световодов; этому способствуют их высокая единичная мощность и малые размеры светящегося тела.
Дуговые ксеноновые трубчатые лампы (ДКСТ) применяются в основном в качестве источников света в осветительных устройствах с высокой единичной мощностью. Лампы ДКСТ выпускаются на единичные мощности от 5 до 100 тыс. Вт и имеют самый близкий к естественному спектральный состав света. Но это их достоинство практически не используется, поскольку лампы внутри зданий не используются. Кроме того, лампы ДКСТ имеют ряд существенных недостатков: большие пульсации светового потока (коэффициент пульсации может достигать 130%), избыток в спектре ультрафиолетовых лучей (при освещенности больше 150лк создается переоблученность), что приводит к необходимости создания колб, не пропускающих ультрафиолетовые лучи, а также малую надежность пусковых устройств и низкую отдачу светового потока по сравнению с современными газоразрядными источниками света (ДРЛ, ДРИ, ДНаТ) и галогенными источниками КГ повышенной мощности. Однако высокая единичная мощность и ныне существующий массовый выпуск ксеноновых ламп способствует их широкому применению.
5.2 Требования к освещению в лаборатории
1. Естественное и искусственное освещение должно соответствовать требованиям СНиП 23-05-95 “Естественное и искусственное освещение”.
2. Во всех помещениях должны быть приняты меры к максимальному использованию естественного освещения.
3. При перепланировке и изменении назначения помещения или при замене одного оборудования другим, освещенность помещения в связи с новыми условиями должна быть приведена в соответствие с нормами освещения.
4. Световые проемы не должны загромождаться производственным оборудованием, готовыми изделиями, полуфабрикатами, тарой и т.п. как внутри, так и вне помещения. Не допускается замена стекол в световых проемах непрозрачными материалами.
5. Стеклянную поверхность световых проемов окон, фонарей и т.п. следует регулярно очищать от пыли и копоти не реже 1 раза в неделю.
6. Разбитые стекла в окнах необходимо немедленно заменять целыми. Не допускается устанавливать в окнах составные стекла и заменять остекление фанерой, картоном и т.п.
7. Осветительные приборы и арматура должны содержаться в чистоте и протираться по мере загрязнения. Сбор использованных люминесцентных и ртутных ламп производить в соответствие с “Указаниями по сбору использованных люминесцентных и ртутных ламп для утилизации на спецпредприятиях”.
8. Наблюдение за состоянием и эксплуатацией осветительных установок возлагается на техническую службу предприятия.
6. Охрана окружающей среды
Сточные воды мехового производства представляют собой сложные гетерогенные многокомпонентные системы, относящиеся к группе высококонцентрированных и токсичных.
Сточные воды высокую концентрацию и большое число ингредиентов: кусочки мездры, шерсть, сгустки крови, грязь, синтетические поверхностно-активные вещества (СПАВ), консервирующие вещества, сульфиды, растворенные белки, жиры, соли хрома, алюминия и др.[]
Многие из этих ингредиентов негативно влияют на гидросферу. Например, действие поваренной соли, поступающей в сток во время отмоки, обусловлено, преимущественно, раздражающими свойствами. Теми же свойствами обладают и синтетические ПАВ, которые кроме этого способны накапливаться на поверхности водоема и препятствуют насыщению кислородом вод. Многие вещества способны накапливаться в живых организмах, тем самым, отравляя их, например, соли тяжелых металлов.
Содержание загрязнений в сточных водах кожевенно-меховой промышленности столь велико, что в случае поступления последних в водный объект, может вызвать необратимые процессы, включая полное разрушение сложившейся экосистемы.
При сравнении качественных характеристик сточных вод, образующихся при обработке различных видов мехового сырья, более загрязненные стоки возникают при обработке овчины меховой, так как в этом случае отработанные воды содержат шестивалентный хром, окислительные красители, используемые в процессах протравления и крашения. Сточные воды, образующиеся в результате переработки шубной овчины, не содержат шестивалентный хром, так как в качестве красильных компонентов в этом случае применяют кислотные или прямые красители. Менее токсичные стоки образуются в результате обработке ценных видов пушнины, где отсутствуют красильные операции, вследствие чего, в общие стоки не поступают соединения, обуславливающие высокий уровень токсического загрязнения.
Для качественной характеристики сточных вод устанавливаются нормативные требования. Для вредных веществ, приняты предельно-допустимые концентрации (ПДК), под которыми подразумевается такая максимальная концентрация вещества, которая оставляет воду при неограниченно долгом ее использовании такой же безвредной, как и при полном отсутствии этого вещества.
Если сточные воды сбрасываются в городскую систему канализации, то для предприятия устанавливаются нормативы ДК (допустимая концентрация) и ВДК (временно допустимая концентрация).
Если очищенные стоки сбрасываются в природные водоемы, то они должны отвечать « Правилам охраны поверхностных вод от загрязнения сточными водами ».
Степень загрязнения сточных вод характеризуется совокупностью физических и бактериологических показателей. К ним относятся: температура, запах, цветность, показатель водородных ионов (рН), концентрация взвешенных веществ, сухой и прокаленный остаток, биологическое потребление кислорода (БПК) и химическое потребление кислорода (ХПК), характеризующие концентрацию органических веществ, содержание компонентов, специфических для данного вида производства[].
Общие стоки кожевенных и меховых предприятий содержат до 1800-2460 мг/дм3 жиров или жироподобных веществ. В стоках от процессов отмоки и дубления их количество достигает более 4 г/дм3. Отработанные жидкости после обезжиривания, промывки свиного сырья и полуфабриката, а также после золения этого сырья содержат еще больше жира. После обезжиривания свиных шкур карбонатом натрия (15-17 г/дм3) в растворе образуется стойкая жировая эмульсия с содержанием жира 8-10 г/дм3. Значительное количество его содержится также в стоках клееварочных цехов.[]
В настоящее время помимо физических и физико-химических методов очистки широко применяется биологический метод, основанный на жизнедеятельности микроорганизмов – деструкторов жировых веществ.
С учетом того обстоятельства, что сточные воды, содержащие жировые вещества имеют в основном повышенную температуру, селектировано несколько видов термофильных микроорганизмов, способных разрушать жиры при температуре свыше 50оС. Эффект очистки при таком способе достигает 100%.[]
6.1 Типовой способ обработки сырья
Рассмотрим виды загрязнений, образующихся в подготовительных и дубильных процессах выделки меховой овчины (таблица 1).
Таблица 1 - Принципиальная схема образования сточных вод и отходы после технологических процессов
| Технологический процесс обработки |
Вид загрязнения |
| отмока первая | гексафторсиликат натрия, новость, сульфат натрия, волос, кровь, грязь, навал, жир, растворимые белки |
| отжим | вода, содержащая остаточную концентрацию веществ после процесса отмоки 1 |
| отмока вторая | фторсиликат натрия, новость, кровь, растворимые белки, жир, |
| обезжиривание первое | формалин, новость, сода, несвязанные жиры |
| отжим | вода, содержащая остаточную концентрацию веществ после процесса обезжиривания |
| стрижка | волос |
| мездрение | мездра |
| обезжиривание второе | сода, новость, формалин, жир |
| промывка первая | остаточная концентрация веществ после второго обезжиривания |
| промывка вторая | - |
| пикелевание | уксусная кислота, серная кислота, хлорид натрия, растворимые белковые вещества |
| дубление | хлорид натрия, тиосульфат натрия, оксид хрома, карбонат натрия |
| отжим | остаточная концентрация веществ после процесса дубления |
| жирование | намазной способ жирования исключает сточные воды |
6.1.1 Расчет количества сточных вод и их качественный состав
Для расчета объема водоотведения и водопотребления необходимо:
1. метод консервирования шкур – п/с;
2. общее количество шкур, перерабатываемых на производстве (за год) - 10000 шт.;
3. влажность шкур после отмоки - 65%;
4. средняя масса одной шкуры – 3,5 кг;
Расчет общей массы обрабатываемых шкурок проводят согласно формуле (2):
М = D × m, (2)
где: М масса обрабатываемых шкурок в сутки, кг; D – общее количество шкурок, перерабатываемых в сутки, шт; m - средневзвешенная масса одной шкурки, кг.
В остальных случаях при расчете водоотведения следуют учитывать только производственные потери, которые составляют до 10%, в среднем 6-7% от общего водопотребления, формула (3):
ВО = ВР-ВР×Р/100 (3)
Для расчета необходимо знать массу партии и ЖК технологического процесса.
Объем водопотребления, рассчитывают по формуле (4):
ВР = мр×ЖК (4)
где: мр масса партии, кг; ЖК – жидкостный коэффициент.
Массу партии вычисляли в зависимости от полезного объема барабана по формуле (5):
мр = Vб/ЖК+1 (5)
где: Vб полезный объем баркаса, дм3.
Пример расчета водопотребления:
Процесс- отмока, ЖК=10:
мр = 3500/11 = 313 кг,
ВР = 313×10 = 3130 дм3
Результаты расчета заносятся в таблицу (2):
Таблица 2 - Объем водопотребления на технологические процессы
| Наименование технологического процесса | ЖК | Масса партии | Объем водопотребления |
| Отмока 1 | 10 | 318,2 | 3182 |
| Отмока 2 | 7 | 437,5 | 3059 |
| Мездрение | - | - | 12 |
| Обезжиривание 1 | 10 | 318,2 | 3182 |
| Обезжиривание 2 | 7 | 437,5 | 3059 |
| Промывка 1 | 7 | 437,5 | 3059 |
| Промывка 2 | 7 | 437,5 | 3059 |
| Пикеливание | 7 | 437,5 | 3059 |
| Дубление | 7 | 437,5 | 3059 |
| Жирование | - | - | - |
Расчет общей массы обрабатываемых шкурок проводят согласно формуле (2) в зависимости от суточной мощности предприятия:
М = (10000/250) × 3,5 = 140 кг
Расчет объема водоотведения: 1 для отмоки первой:
ВО = 3182-(3182×10/100)-140×((65-14)/100)/1000 = 2863,7 дм3;
2 отжим:
ВО = (3182-2863,7) ×10/100 = 26,43 дм3;
3 для отмоки второй:
ВО = 3059-(3059×10/100) = дм3;
4 мездрение:
ВО = 12-(12×10)/100=10,8 дм3;
обезжиривание первое:
ВО = 3182-(3182×10/100) =2863,8 дм3;
5 отжим:
ВО = (3182-2863,8) ×10/100 =31,82 дм3;
6 обезжиривание второе:
ВО = 3059-(3059×10/100) =2753,1 дм3;
7 промывка первая: ВО = 2753,1 дм3;
8 промывка вторая: ВО = 2753,1 дм3;
9 пикелевание: ВО = 2753,1 дм3;
10 дубление: ВО = 2753,1 дм3;
11 отжим: ВО = (3059-2753,1) ×10/100=30,59 дм3;
Известно, что количество хозяйственно-фекальных сточных вод от общего объема сточных вод составляет 5-6%. Следовательно, необходимо выполнить расчет, определяющий количество хозяйственно-фекальных вод, образующихся в процессе переработки мехового сырья.
Исходные данные:
Численность ИТР 4 чел
Численность рабочих 9 чел
Численность сотрудников 1 чел
Количество душевых сеток 1 шт.
Продолжительность работы душа на одного работника 0,4 час
Общая площадь территории полов 540 м2
Некоторые нормативные требования представлены в таблице 3.
Таблица 3 - Нормативные требования расхода воды на хозяйственно-бытовые нужды
Показатель |
Расход воды |
| На одного ИТР |
12 дм3/сут |
| На одного рабочего |
25 дм3/сут |
| На одну душевую сетку |
0,5 м3/час |
| На мытье полов |
0,5дм3/м2 |
| На одного рабочего в химической лаборатории |
460дм3/сут |
Пример расчета расхода воды на хозяйственно-бытовые нужды представлен в таблице 4.
Таблица 4 - Расчет расхода воды на хозяйственно-питьевые нужды
| Показатель | Расчет расхода воды |
Хозяйственно-питьевые нужды |
4×12+9×25=0,273 м3/сут |
| Душевые |
0,5×1×1=0, 5 м3 |
| Мытье полов |
0,5×540/1=0,270 м3 |
| Химическая лаборатория |
460×1=0,46 м3/сут |
| Итого: |
1,503 м3/сут |
6.1.2 Определение качественных характеристик сточных вод
Для определения качества сточных вод, образующихся после переработки мехового сырья необходимы следующие исходные данные:
1 наименование технологического процесса;
2 наименование химических веществ, используемых в технологическом процессе;
3 расход химических веществ;
4 процент отхода химических материалов в сточные воды;
5 объем водопотребления;
6 объем водоотведения;
Пример расчета:
Технологический процесс: отмока1
Состав отмочной ванны: гексафторосиликат натрия 1г/дм3, новость 1г/ дм3, сульфит натрия 0,5 г/ дм3.
Отход в сточные воды, %: гексафторосиликат натрия - 96, новость - 95, сульфит натрия 30.
Объем водоотведения - 2863,7 дм3.
1 Расчет концентрации ингридиентов в сточной воде после процесса отмоки:
а) гексафторосиликат натрия: 1г/ дм3 –100%
Х - 96%, Х = 0,96 г/дм3
б) новость: 1г/ дм3 - 100%
Х - 95%, Х = 0,95 г/ дм3
в) сульфит натрия: 0,5г/дм3 – 100%
Х - 30%, Х = 0,15 г/ дм3
2 Расчет количества ингридиентов в сточной воде:
а) гексафторосиликат натрия: 0,96 г – 1дм3
х - 2863,7 дм3, х= 2749,15 г
б) новость: 0,95г – 1дм3
х - 2863,7 л, х=2584,5 г
в) сульфит натрия: 0,15г – 1дм3
х - 2863,7 дм3, х= 429,56 г
Расчет качественного состава сточных вод после остальных технологических процессов производится аналогично. Результаты расчета представлены в таблице 5.
6.1.3 Расчет коэффициентов часовой, суточной и общей неравномерности
Из-за длительности процессов обработки меховой овчины наблюдается колебание расхода сточных вод по суткам. Исходные данные по поступлению сточных вод на очистные сооружения представлены в таблице 6.
Таблица 6 – Исходные данные по поступлению сточных вод на очистные сооружения
| день | Время поступления сточных вод, час |
Расход сточной воды, м3/час |
| Понедельник-воскресение |
7-30 8-00 8-30 14-30 15-30 17-00 18-00 19-00 20-00 22-00 23-00 23-30 |
2,864 2,753 0,026 2,753 0,031 2,753 0,011 2,863 0,031 2,753 2,753 2,753 |
В данной таблице описывают неравномерность поступления сточных вод на очистные сооружения в различные часы суток. Сбрасываемый объем также отличается в разные часы и дни. Это объясняется особенностью технологических процессов при выработке меховой овчины. Т.е. водоотведение объясняется способностью кожевой ткани поглощать раствор, определенной влажностью сырья.
Поэтому, для каждого дня недели рассчитывается коэффициент часовой неравномерности по формуле (6):
Кчас = Qmaxсут / Qсрчас, (6)
где: Кчас коэффициент часовой неравномерности; Qmax - максимальный объем притока сточных вод в течение суток, м3; Qср среднечасовой приток сточных вод, м3.
Среднечасовой приток сточных вод определяют по формуле (7):
Qср = ∑Qi / 24, (7)
где: Qi приток сточных вод на очистные сооружения в i – час; 24 – количество часов в сутки.
Коэффициент суточной неравномерности определяется отношением максимального суточного расхода к среднему суточному по формуле (8):
Ксут = Qmaxнед / Qсрнед, (8)
Общий коэффициент неравномерности водоотведения на предприятиях рассчитывают по формуле (9):
Кобщ = Кчас×Ксут, (9)
Пример расчета:
День недели-вторник
а) Расчет среднесуточного притока сточных вод:
Qср = (2,863+0,026+2,753+2,863+0,032+2,753+2,753+2,753+2,753+ 2,753+0,031+ +0,02)/24=0,93
б) Расчет коэффициента часовой неравномерности:
Кчас= 2,863/0,93 = 3,1
в)Расчет коэффициента суточной неравномерности:
Ксут= 2,863/((2,863+0,026+2,753+ 2,863+0,032+2,753+2,753+2,753+2,753 +2,753+ + 0,031+0,012)/7) = 0,23
г) Общий коэффициент неравномерности:
Кобщ = 3,1×0,23=0,713
Аналогичный расчет ведется для каждого дня недели, полученные данные заносятся в таблицу 7.
Таблица 7 - Коэффициенты неравномерности поступления сточной воды на очистные сооружения в течении недели
| Коэффициент неравномерности | Дни недели | |||||
| понедельник | вторник | среда | четверг | пятница | суббота | |
|
Кчас |
3,1 | 3,1 | 3,1 | 3,1 | 3,1 | 3,1 |
|
Ксут |
0,23 | |||||
|
Кобщ |
0,713 | 0,713 | 0,713 | 0,713 | 0,713 | 0,713 |
6.1.4 Расчет удельного водопотребления и водоотведения на единицу выпускаемой продукции
Одним из показателей, характеризующих уровень воздействия предприятия на окружающую среду является оценка удельного водопотребления и водоотведения на единицу выпускаемой продукции.
Фактический расход воды при выделке меховой овчины определяется по следующим показателям:
-на производственные нужды 75-85%
-на хозяйственно-бытовые нужды 5-6%
-воды, образующиеся после осадков или ливневые воды 2-3%
-условно чистые воды, используемые для охлаждения оборудования или в холодильниках, вентиляторах, компрессорных установках 6-18%
Исходные данные:
Мощность предприятия 10000 шт.овчин в год
Количество рабочих дней 250
Объем сточных вод составляет:
Производственные 75%
Хозяйственно-бытовые 6%
Условно-чистые 16%
Ливневые 3%
Объем водоотведения с учетом производственных и хозяйственно-бытовых нужд при переработке овчины составляет: 23,84 м3/сут или 5960 м3/год из них:
-производственные 17,88 м3/сут или 4470 м3/год
-хозяйственно-бытовые 1,43м3/сут или 357,5 м3/год
-условно-чистые 3,81м3/сут или 952,5 м3/год
-ливневые 0,72 м3/сут или 180 м3/год
Известно, что в процессе выполнения технологических операций в среднем потери воды на производственные нужды не превышает 6%, тогда общий объем водопотребления составит:
23,84+(23,84×0,06) = 25,27 м3/сут или 6317,5 м3/год
Определим удельный объем водопотребления и водоотведения на единицу выпускаемой продукции:
а) удельный объем водопотребления на единицу выпускаемой продукции
Фактический объем водопотребления составит 6317,5 м3/год
Мощность предприятия в год 10000шт овчины
Тогда, 6317,5 м3/год - 10000 шт
Х м3/год - 1 единица вып.продукции, Х = 0,63 м3/год
б) удельный объем водоотведения на единицу выпускаемой продукции
Фактический объем водоотведения составляет 5960 м3/сут
5960 м3/год - 10000шт.овчин
Х м3/год -1 ед.прод., Х = 0,6 м3/год
6.1.5 Расчет удельной величины неравномерности загрязняющих веществ на выходе после основного производства
Для составления карты технологического уровня предприятия и определения категории опасности нужно рассчитать количество загрязняющих веществ (кг), образующихся при переработке мехового сырья, приходящихся на 1 кг потребляемого сырья.
Основными показателями для расчета являются: фактический сброс сточных вод, концентрация ингредиентов в сточной воде, масса одной шкурки, количество перерабатываемого сырья (кг/год).
Пример расчета.
Исходные данные:
1.Фактический расход воды на производственные нужды в год - 4470 м3
2.Концентрация пасты Новость – 15,2 мг/дм3
Тогда: 15,2×10-9 тонн – 0,001м3
Х тонн - 4470 м3 Х = 0,068 тонн/год
Количество сырья: 10000 шт. овчин × 3,5кг × 250 дней = 8750000 кг/год
Удельная величина загрязняющих веществ на выходе после основного производства: 0,068×1000/8750000 = 0,0000077 кг сброса/ кг сырья
Аналогично расчеты проводят для всех видов ингредиентов, результаты расчета представлены в таблице 8.
Таблица 8 - Оценка общего объема контаминантов, сбрасываемых предприятием
|
Наиме нование сырья |
Кол-во сырья, кг/год |
Показатели качества воды |
Концентрация ингредиентов в сточной воде, г/дм3 |
Количество загрязнений, тонн/год |
Удельные сбросы загрязненных в-в, кг сброса/кг сырья |
|
овчина меховая |
8750000 | Новость | 15,2 | 0,068 | 0,0000077 |
| Антисептик | 1,68 | 0,0075 | 0,000000857 | ||
| Сульфит натрия | 0,15 | 0,00067 | 0,0000000766 | ||
| Формалин | 0,25 | 0,00112 | 0,000000128 | ||
| Сода | 0,25 | 0,00112 | 0,000000128 | ||
| Уксусная кислота | 1,5 | 0,0067 | 0,000000766 | ||
| Серная кислота | 0,45 | 0,00201 | 0,00000023 | ||
| Хлорид натрия | 72 | 0,32184 | 0,0000367 | ||
| Тиосульфат натрия | 0,2 | 0,0009 | 0,000000102 | ||
| Оксид хрома | 0,9 | 0,004 | 0,000000457 |
6.1.6 Определение категории опасности предприятия
Классификация загрязняющих веществ для региона озера Байкал осуществляется по категориям:
Категория 1. Экологически особо опасные вещества-высокотоксичные чужеродные вещества, накапливающиеся в гидробионтах, аккумулирующиеся в пищевых цепях, медленно разлагающиеся. Сброс их не допустим.
Категория 2. Экологически высоко-опасные вещества- создаются в природном фоне в воде озера, представляющие опасность для гидробионтов в концентрациях, превышающих фоновые. Сброс их возможен в количествах, не приводящих к повышению концентрации примеси в воде озера.
Категория 3. Экологически опасные вещества- токсичные чужеродные вещества, быстро разлагающиеся, умеренно летучие либо другим путем достаточно быстро удаляемые из воды. Сброс их нормируется.
Категория 4. Экологически умерено-опасные вещества- присутствующие в воде озера и его притоков, не обладающие острой токсичностью для гидробионтов. Сброс их возможен соответственно установленным нормативам.
В соответствии с категориями следует провести классификацию загрязняющих веществ, которые присутствуют в сточных водах исследуемого предприятия.
Для определения категории опасности предприятия необходимо использовать следующие показатели: объем сбрасываемых загрязняющих веществ(М), кг/год, предельно-допустимые концентрации (ПДК) для вод хозяйственно-питьевого и культурно-бытового водопользования, мг/дм3, коэффициент(к), зависящий от категории опасности загрязняющих веществ.
Таблица 9 - Зависимость коэффициента (к) от категории опасности загрязняющего вещества
| Категория опасности | Значение коэффициента |
| Экологически особо опасные вещества(1 кат) | 1,7 |
| Экологически высоко-опасные вещества(2 кат) | 1,3 |
|
Экологически опасные вещества (3 кат) |
1,0 |
| Экологически умерено-опасные вещества(4 кат) | 0,9 |
По отношению (М/ПДК)к определяется категория опасности предприятия:
1 Если ∑(М/ПДК)к <100, то предприятие относится к 4 категории опасности
2 Если 100 < ∑(М/ПДК)к < 1000, то предприятие относится к 3 категории опасности
3 Если 1000 < ∑(М/ПДК)к < 10000, то предприятие относится к 2 категории опасности
4 Если 10000 < ∑(М/ПДК)к, то предприятие относится к 1 категории опасности
Таблица 10 - Определение категории опасности мехового предприятия
| Показатели качества | Коэффициент токсичности |
ПДК г/дм3 |
Объем сбрасываемых загрязняющих веществ, г/дм3 |
(М/ПДК)к |
| Новость | 1,7 | 0,1 | 15,2 | 5118,0 |
| Уксусная кислота | 0,9 | 0,4 | 1,5 | 3,28 |
| Серная кислота | 0,9 | 10 | 0,45 | 0,06 |
| Хлорид натрия | 0,9 | 30 | 72 | 2,2 |
| Оксид хрома | 1,3 | 0,001 | 0,9 | 347 |
| Итого: | 5470,54 | |||
Таким образом, исследуемое предприятие при использование типовой методике выделки меховой овчины относится к 3 группе опасности, т.к. 1000 < ∑(М/ПДК)к < 10000, т.е. оно является экологически опасным по отношению к району, располагающемуся вблизи озера Байкал.
6.2 Рекомендуемый способ обработки сырья
Предлагаемый способ обработки мехового сырья с использованием бактериальной суспензии микроорганизмов- деструкторов жировых веществ позволяет снизить расход СПАВ и исключить из рабочей ванны формальдегид и карбонат натрия.
Рассмотрим виды загрязнений, образующихся в подготовительных и дубильных процессах выделки меховой овчины (таблица 10).
Таблица 11 - Принципиальная схема образования сточных вод и отходы после технологических процессов
| Технологический процесс обработки |
Вид загрязнения |
| отмока первая | гексафторсиликат натрия, новость, сульфат натрия, волос, кровь, грязь, навал, жир, растворимые белки |
| отжим | вода, содержащая остаточную концентрацию веществ после процесса отмоки 1 |
| отмока вторая | фторсиликат натрия, новость, кровь, растворимые белки, жир, |
| обезжиривание первое | Микроорганизмы, остаточную концентрацию солей |
| отжим | вода, содержащая остаточную концентрацию веществ после процесса обезжиривания |
| стрижка | волос |
| промывка | остаточная концентрация веществ после обезжиривания |
| пикелевание | уксусная кислота, серная кислота, хлорид натрия, растворимые белковые вещества |
| дубление | хлорид натрия, тиосульфат натрия, оксид хрома, карбонат натрия |
| отжим | остаточная концентрация веществ после процесса дубления |
| жирование | намазной способ жирования исключает сточные воды |
6.2.1 Расчет количества сточных вод и их качественный состав
Рассчитаем количества сточных вод, образующихся при переработке мехового сырья с использованием биотехнологического метода выделки. Результаты занесены в таблицу 12.
Таблица 12 - Объем водопотребления на технологические процессы при использование биотехнологического метода выделки
| Наименование технологического процесса | ЖК | Масса партии | Объем водопотребления |
|
Отмока Мездрение Обезжиривание Промывка Пикеливание Дубление Жирование |
10 - 10 - 7 7 - |
318,2 - 318,2 437,5 437,5 437,5 - |
3182 12 3182 3059 3059 3059 |
Расчет объема водоотведения:
1 отмока: ВО = 3182-(3182×10/100)-140×((65-14)/100)/1000 = 2863,7 дм3;
2 отжим: ВО = (3182-2863,7) ×10/100 = 26,43 дм3;
4 мездрение: ВО = 12-(12×10)/100 = 10,8 дм3;
обезжиривание: ВО = 3182-(3182×10/100) = 2863,8 дм3;
5 отжим: ВО = (3182-2863,8) ×10/100 = 31,82 дм3;
7 промывка: ВО = 2753,1 дм3;
9 пикелевание: ВО = 2753,1 дм3;
10 дубление: ВО = 2753,1 дм3;
11 отжим: ВО = (3059-2753,1) ×10/100=30,59 дм3;
Расчет качественного состава сточных вод при применении данного метода описывается в таблице 13.
6.2.2 Расчет коэффициентов часовой, суточной и общей неравномерности
Исходные данные по поступлению сточных вод на очистные сооружения представлены в таблице 14.
Таблица 14 Исходные данные по поступлению сточных вод на очистные сооружения
| День | Время поступления сточных вод, час |
Расход сточной воды, м3/час |
| Понедельник-воскресение |
7-30 8-00 9-00 10-00 11-30 12-30 21-00 3-30 4-30 |
2,864 0,026 0,011 2,863 0,031 2,753 2,753 2,753 0,031 |
В данной таблице описывают неравномерность поступления сточных вод на очистные сооружения в различные часы суток. Сбрасываемый объем также отличается в разные часы и дни. Это объясняется особенностью технологических процессов при выработке меховой овчины. Т.е. водоотведение объясняется способностью кожевой ткани поглощать раствор, определенной влажностью сырья.
Пример расчета:
День недели-вторник
а) расчет среднесуточного притока сточных вод:
Qср= (2,863+0,026+0,011+2,863+0,031+2,753+2,753+2,753+0,031)/24 = 0,59
б) расчет коэффициента часовой неравномерности:
Кчас=2,863/0,59=4,85
в) расчет коэффициента суточной неравномерности:
Ксут=2,863/((2,863+0,026+0,011+2,863+0,031+2,753+2,753+2,753+0,031)/7) = =0,16
г)общий коэффициент неравномерности:
Кобщ = 0,16×4,85 = 0,776
Аналогичный расчет ведется для каждого дня недели, полученные данные заносятся в таблицу 15.
Таблица 15 - Коэффициенты неравномерности поступления сточной воды на очистные сооружения в течении недели
| Коэффициент неравномерности | Дни недели | |||||
| понедельник | вторник | среда | четверг | пятница | суббота | |
|
Кчас |
4,85 | 4,85 | 4,85 | 4,85 | 4,85 | 4,85 |
|
Ксут |
0,16 | |||||
|
Кобщ |
0,776 | 0,776 | 0,776 | 0,776 | 0,776 | 0,776 |
6.2.3 Расчет удельного водопотребления и водоотведения на единицу выпускаемой продукции
Объем водоотведения с учетом производственных и хозяйственно-бытовых нужд при переработке овчины составляет:
V = 10,56+0,84 = 11,4 м3/сут или 2850 м3/год из них:
-производственные 8,55 м3/сут или 2137,5 м3/год
-хозяйственно-бытовые 0,684 м3/сут или 171 м3/год
-условно-чистые 1,824 м3/сут или 456 м3/год
-ливневые 0,684 м3/сут или 171 м3/год
Известно, что в процессе выполнения технологических операций в среднем потери воды на производственные нужды не превышает 6%, тогда общий объем водопотребления составит:
11,4+(11,4×0,06)=12,084 м3/сут или 3021 м3/год
Определим удельный объем водопотребления и водоотведения на единицу выпускаемой продукции:
а) удельный объем водопотребления на единицу выпускаемой продукции
Фактический объем водопотребления составит 3888,25 м3/год.
Мощность предприятия в год 10000шт овчины Тогда, 3888,25 м3/год - 10000 шт
Х м3/год - 1 единица вып.продукции, Х = 0,389 м3/год
б) удельный объем водоотведения на единицу выпускаемой продукции
Фактический объем водоотведения составляет 3522,06 м3/год
3522,06 м3/год - 10000шт.овчин
Х м3/год - 1 ед.прод., Х = 0,352 м3/год
Расчет удельной величины неравномерности загрязняющих веществ на выходе после основного производства
Пример расчета.
Исходные данные:
1.Фактический расход воды на производственные нужды в год - 2137,5 м3
2.Концентрация карбоната натрия – 25 мг/дм3
Тогда: 25×10-9 тонн – 0,001м3
Х тонн - 2137,5 м3 Х = 0,053 тонн/год
Количество сырья: 10000шт.овчин×3,5кг×250дней=8750000 кг/год
Удельная величина загрязняющих веществ на выходе после основного производства: 0,053×1000/8750000=0,000006 кг сброса/ кг сырья
Аналогично расчеты проводят для всех видов ингредиентов, результаты расчета представлены в таблице 16.
Таблица 16 Оценка общего объема контаминантов, сбрасываемых предприятем
|
Наиме нование сырья |
Кол-во сырья, кг/год |
Показатели качества воды |
Концентрация ингредиентов в сточной воде, г/дм3 |
Количество загрязнений, тонн/год |
Удельные сбросы загрязненных в-в, кг сброса/кг сырья |
|
овчина меховая |
8750000 | Сода | 0,25 | 0,053 | 0,00000011 |
| Хлорид натрия | 36 | 0,142 | 0,000016 | ||
| Тиосульфат натрия | 0,2 | 0,0008 | 0,00000009 | ||
| Оксид хрома | 0,9 | 0,0036 | 0,00000041 |
6.2.4 Определение категории опасности предприятия
Таблица 17 - Определение категории опасности мехового предприятия
| Показатели качества | Коэффициент токсичности |
ПДК г/дм3 |
Объем сбрасываемых загрязняющих веществ, кг/год |
(М/ПДК)к |
| Хлорид натрия | 0,9 | 30 | 36 | 1,2 |
| Оксид хрома | 1,3 | 0,001 | 0,9 | 347 |
| Итого: | 348,2 | |||
Заключение
Рассмотрены современные методы проведения подготовительных процессов выделки меховой овчины, современные способы очистки сточных вод меховой промышленности после первичной обработки сырья.
Наиболее эффективным методом очистки сточных вод, содержащих жировые вещества, является биологический способ, который применяется для удаления жиров с помощью микроорганизмов-деструкторов.
Изучены морфолого-культуральные и физиологические свойства исследуемых культур микроорганизмов. Рассмотрено влияние внешних факторов на динамику роста и развития микроорганизмов. Показана возможность применения микроорганизмов, обладающих липолитической активностью для проведения процесса обезжиривания меховой овчины.
Установлено, что ферментативное проведение процесса приводит к получению обезжиренного полуфабриката. Разработаны маточные растворы, способствующие получению обезжиренного полуфабриката с минимальными затратами. Наиболее оптимальным является вариант, в котором при проведении процесса используется рабочая ванна с 100% расходом бактериальной суспензии от объема рабочего раствора, при продолжительности культивирования 24 часа.
Применение данной бактериальной суспензии обеспечило оптимальное удаление жировых веществ с поверхности кожевой ткани и волосяного покрова меховой овчины. Замена типовой методики проведения процесса обезжиривания позволяет значительно сократить расход химических материалов при проведении процесса и снизить токсичность образуемых сточных вод.
Список использованных источников информации
1 Шестакова И.С. Ферменты в кожевенном и меховом производстве. - М.: Легпромбытиздат, 1990 - 128 с.
2 Цыбикова Д.Ц. Белки, ферменты, дубители и красители. - Улан-Удэ: ВСГТУ, 2002 - 164 с.
3 Бабакина В.Г. Применение ферментов в производстве кожи. - М: Ростехиздат,1972 – 248с.
4 Feigel T.H. The role of soaking enzymes on collagen destruction in bovin hide. World Leather. 2001 №9. Р.66-72
5 Страхов И.П. и др. Химия и технология кожи и меха / И.П. Страхов, И.С. Шестакова, Д.А. Куциди. - М.: Легпромбытиздат, 1985 – 496 с.
6 Применение ферментов для обезволашивания кожевенного сырья.-М.:1973 – 23 с.
7 Интенсификация ферментного обезволашивания / Т.А. Кузнецова, А.В. Черкасова, Т.Ф. Миронова, Т.Ю. Тихонюк // Кожевенно-обувная промышленность 1994 № 9-10 стр. 20-21
8 Оросын, Батменх. Оптимальные условия культивирования ВАС. mesentericus для получения протеолитических ферментных препаратов и испытание их при обезволашивании кожевенного сырья. - М.:1978-25 с.
9 Чурсин В.И., Шапкарина Н.П. Влияние ферментативной обработки на свойства голья и полуфабриката // Кожевенно-обувная промышленность 2005 №5 стр.35-36
10 Субач О.В. и др. Шкуры угря как новое кожевенное сырье // Кожевенно-обувная промышленность 1997 №5 стр.30-31
11 Харчуткина Е.М., Болдовская О.В., Дормидонтова О.В. Особенности ферментативной отмоки-обезжиривания шкур угря // Кожевенно-обувная промышленность 2003 №2 стр.38-39
12 Кочетова С.П. и др. Влияние ферментных обработок кожевенного сырья на связь волоса с дермой / С.П. Кочетова, Н.В.Зыкова, Н.П. Омельяненко // Кожевенно-обувная промышленность 1996 № 4 стр. 30-31
13 Нестерова Г.А. Эффективность использования ферментных препаратов в подготовительных процессах // Кожевенно-обувная промышленность 1995 № 4 стр.31-32
14 Кочеткова С.П. Структура голья, выработанного по бессульфидной технологии // Кожевенно-обувная промышленность 1998 № 6 стр.32-34
15 Исследование гидролитических ферментов шкур крупного рогатого скота / С.П. Кочетова, Н.В. Зыкова, А.И. Котельников, В.Р. Рогель // Кожевенно-обувная промышленность 1997 № 2 стр. 30-31
16 Влияние ферментативной обработки на свойства связующих и пигментных концентратов / В.Г. Плешаков, С.В. Янушевская, В.С. Мальцева, В.С. Духанин // Кожевенно-обувная промышленность 1991 № 7 стр. 26-28
17 Фигурин Ю.В., Изменение структурных элементов свиной шкуры под действием комплекса ферментных препаратов // Кожевенно-обувная промышленность 1993 № 3 стр. 23-25
18 Пуртова Е.А. и др. Изучение возможностей использования нейтральной протеазы протосубтилин Г10Х в производстве кож для верха обуви / Е.А Пуртова., Т.Ф.Миронова, Л.М.Лупова // Кожевенно-обувная промышленность 1986 № 9 стр. 39-41
19 Рохваргер О.Д. Ферменты в меховом производстве. - М.: Легкая индустрия, 1997 - 224 с.
20 Kazlauskaite E., Balciunine J., Beleska K. Influence of the enz matic soaking process on the properties of lime-free leather. Przemysl lekki na przelomie tysiacleci. Materialy Miedzynarodnej Konferencji Naukowej. Radom. 2001.l.61-66
21 Brady D., Duncan J.R., Rassel A.E. Model for proteolytic depilation hears of skins. JALKA.V.85.1990.P.334-342
22 Миронова Т.Ф. Использование ферментных препаратов в производстве кожи и меха // Кожевенно-обувная промышленность 1989 №6 стр.31-32
23 Раевский А.В., Сергеев Н.В., Стефанович И.П. Новое в обработке меховой и шубной овчины химическими и ферментными реагентами. М.: Легкая индустрия, 1968- 38 с.
24 Применение ферментов на кожевенных предприятиях Франции.-М.:1970-25 с.
25 Миронова Т.Ф. Возможности использования в меховом производстве нового ферментного препарата протеазы Прок // Новое в меховом производстве М.: 1999 – стр. 33-36
26 Сынкова А.В. и др.. Влияние некоторых факторов на каталитическую активность протеазы прок / А.В. Сынкова, Т.Ф. Миронова, О.В. Талянский // Кожевенно-обувная промышленность 2003 № 2 стр. 43-44
27 Пучкова Н.В. и др. Основные требования к ферментным препаратам для обработки мехового сырья / Н.В. Пучкова, А.М.Ерошевич, Н.И. Патенко // Кожевенно-обувная промышленность 1985 № 5 стр. 50-51
28 Применение ферментного препарата мальтавоморина Г10Х для обработки шкурок кролика / Г.И. Ярецкас, Н.М. Шибаковский, О.Н. Мацевичене, А.К. Струмскине // Кожевенно-обувная промышленность 1985 № 6 стр. 44-46
© 2010 Интернет База Рефератов