
Рефераты по сексологии
Рефераты по информатике программированию
Рефераты по биологии
Рефераты по экономике
Рефераты по москвоведению
Рефераты по экологии
Краткое содержание произведений
Рефераты по физкультуре и спорту
Топики по английскому языку
Рефераты по математике
Рефераты по музыке
Остальные рефераты
Рефераты по авиации и космонавтике
Рефераты по административному праву
Рефераты по безопасности жизнедеятельности
Рефераты по арбитражному процессу
Рефераты по архитектуре
Рефераты по астрономии
Рефераты по банковскому делу
Рефераты по биржевому делу
Рефераты по ботанике и сельскому хозяйству
Рефераты по бухгалтерскому учету и аудиту
Рефераты по валютным отношениям
Рефераты по ветеринарии
Рефераты для военной кафедры
Рефераты по географии
Рефераты по геодезии
Рефераты по геологии
Рефераты по геополитике
Рефераты по государству и праву
Рефераты по гражданскому праву и процессу
Рефераты по делопроизводству
Рефераты по кредитованию
Рефераты по естествознанию
Рефераты по истории техники
Рефераты по журналистике
Рефераты по зоологии
Рефераты по инвестициям
Рефераты по информатике
Исторические личности
Рефераты по кибернетике
Рефераты по коммуникации и связи
Курсовая работа: Определение способности почвенных бактерий к разложению синтетических моющих средств
Курсовая работа: Определение способности почвенных бактерий к разложению синтетических моющих средств
Курсовая работа
по дисциплине «промышленная микробиология»
на тему:
"Определение способности почвенных бактерий к разложению синтетических моющих средств"
Оглавление
Введение. 4
1.1 Поверхностно-активные вещества и их применение. 6
1.2 Общая характеристика синтетических моющих средств. 9
1.3 Поверхностно-активные вещества как компоненты СМС.. 12
1.4 Влияние поверхностно-активных веществ на микроорганизмы.. 17
1.5 Микробиологическая деструкция поверхностно-активных веществ. 21
1.6 Действие СМС на экосистемы и здоровье человека. 26
2. Объекты и методы исследований. 32
2.1 Методы исследований. 32
2.2 Материалы и оборудование. 35
3. Экспериментальная часть. 41
3.1 Культурально-морфологическая характеристика микроорганизмов. 41
3.2 Физиолого-биохимическая характеристика микроорганизмов. 42
3.3 Определение активности микроорганизмов-деструкторов ПАВ.. 43
3.4 Определение способности роста микроорганизмов на средах с добавлением различных ПАВ.. 45
Выводы.. 47
Литература. 48
Питательный агар (ПА) (г/л): 50
Введение
Одна из причин современного экологического кризиса состоит в том, что практически вся хозяйственная и производственная деятельность человека ведут к нарушению важнейших функций почвы. Утрата почвой ее функций, деградация почвы, деградация экосистемы – события взаимосвязанные. Аналогичная ситуация наблюдается и в отношении водоемов. Загрязнение водоемов, эвтрофикация так же ведут к нарушению природного равновесия в водных экосистемах.
Деградация почв может быть вызвана природными факторами (климатическими или гидрологическими), но преимущественно она связана с техногенными причинами. К ним относятся нерациональное ведение земледелия, чрезмерный выпас скота, уничтожение почвенного и растительного покрова промышленным, коммунально-бытовым, ирригационным строительством и горными разработками, истощительное землепользование, переуплотнение техникой, подтопление, нарушение режима полива, нарушение режима внесения органических и минеральных удобрений, технологические и аварийные промышленные выбросы твердых веществ (Новиков, 2002).
Сточные воды – один из главных источников попадания в окружающую среду вредных веществ. Опасными загрязнителями окружающей среды являются искусственные органические вещества, которые находятся в стоках предприятий синтетической химии и производств, применяющих эти соединения. Такие вещества представляют наибольшую угрозу для природы, так как многие из них трудно разлагаются и в течение длительного времени сохраняются в окружающей среде, оказывая неблагоприятное действие на живые организмы (Ставская, 1981).
Такие соединения как ПАВ, пестициды, различные органические соединения, содержащие нитрогруппу, галоидорганические соединения, фосфорорганические соединения, пластмассы, синтетические смолы и некоторые другие продукты промышленности органического синтеза, разрушаются в природе медленно и с большим трудом, они отличаются высокой устойчивостью к действию микроорганизмов. Такие синтетические вещества кумулируются в водоемах и почве, загрязняют окружающую среду. Самое важное, то, что они способны накапливаться в пищевых цепях и таким образом оказывать неблагоприятное воздействие на животных и человека.
Для того чтобы разрушать синтетические органические соединения, организм должен либо поглощать и усваивать их в качестве источника питания, либо вызывать ферментативную деструкцию, утилизируя химическую энергию, освобождающуюся при упрощении органического соединения. Такие процессы вызываются микроорганизмами и в очень ограниченной степени макроорганизмами (Ротмистров, 1975).
Для специалистов, занимающихся вопросами интенсификации процессов разрушения веществ-загрязнителей, задача состоит в том, чтобы обнаружить микроорганизмы-деструкторы и найти способ усилить их деструктивную активность с целью использования для очистки окружающей среды.
Работ по микробиологическому разложению таких синтетических веществ как ПАВ, пестициды, пластмассы в настоящее время не так уж много, поэтому работа по изучению разложения поверхностно-активных веществ микроорганизмами является актуальной.
В связи с этим целью данной работы является определение способности чистых культур почвенных бактерий к разложению ПАВ.
Для достижения поставленной цели необходимо решить ряд задач:
– изучение физиолого-биохимических свойств, и идентификация выделенных штаммов;
– определение активности чистых культур микроорганизмов по отношению к СМС.
1. Особенности загрязнения почвенных экосистем поверхностно-активными веществами
1.1 Поверхностно-активные вещества и их применение
Загрязняющие вещества – это химические вещества, поступающие в окружающую среду из антропогенных источников в количествах, опасных для живых организмов. Критерии определения этих количеств неоднозначны. При разнообразии загрязняющих веществ, среди них можно выделить вещества, встречающиеся в природе и чуждые ей. Превышение природного уровня содержания химических веществ в почве, воде, воздухе может представлять опасность для живых организмов, так как является результатом поражения экосистемы, нарушения свойственных ей сбалансированных потоков вещества. Количество поступающих в экосистему химических веществ из антропогенных источников зависит от степени вовлечения их человеком в производственный процесс (Глазовская, 1979).
В древности человек использовал лишь 8 элементов периодической системы Менделеева, в XVIII веке число их увеличилось до 28, в XIX веке достигло 62. Добыча основных металлов за XIX век увеличилась на два порядка. В настоящее время человеком используются не только все химические элементы, но и радиоактивные изотопы известных элементов и неизвестные природе трансурановые элементы (Яковлев, 1998).
В настоящее время в мире производится около 80 тысяч видов химических продуктов. Каждый год на рынок поступает более тысячи новых. В мире используется около 250 млн. т органических химических веществ, значительная часть которых после использования бесконтрольно попадает в окружающую среду. Колоссальные количества веществ антропогенной природы не могут не изменять состав природных сред на планете (Королев, 2001).
Влияние на здоровье человека загрязняющих веществ имеет свои особенности. Химические вещества, как правило, поступают в организм человека не непосредственно, а по пищевым цепочкам; почва – вода – человек, почва вода – растения – человек, почва – растения – животное – человек (Новиков, 2002).
ПАВ, вступая во взаимодействие с клетками, способствуют развитию атеросклероза, интенсификации белкового и углеводного обмена, нарушению функции печени, почек, иммунной и репродуктивной систем. При совместном присутствии ПАВ, металлов, пестицидов, других веществ, токсичность их усиливается (www.ecocoop.ru).
Отходы поступают в окружающую среду в твердом, жидком состоянии, а также в форме аэрозольных выбросов. Почвы загрязняются как непосредственно, так и через атмосферу и гидросферу. Загрязнение воздуха и вод неизбежно сопровождается загрязнением почв.
В последнее время среди загрязняющих веществ все чаще встречаются поверхностно-активные вещества. Это связано с широким использованием синтетических моющих средств (Королев, 2001). Поверхностно-активные вещества (ПАВ) – вещества, которые используются в промышленности и в быту как моющие средства, загрязняют окружающую среду с отходами коммунально-бытовой деятельности. В состав ПАВ обычно входят одна или несколько групп поверхностно-активных агентов и несколько связывающих центров. Эти группы снижают поверхностное натяжение жидкости, в которой они растворяются, образуют стабильную эмульсию с частицами удаляемых веществ, снижают жесткость воды (Ставская, 1981).
В состав ПАВ входят также связывающие компоненты. Они могут взаимодействовать с ионами кальция и магния, присутствующими в виде солей в жесткой воде, а также в составе твердых веществ. Наиболее распространено использование в качестве связывающих компонентов смеси полифосфатов с триполифосфатом натрия.
Мировое производство ПАВ составляет 2–3 кг на душу населения в год. Примерно 50% производимых ПАВ используется для бытовой химии, остальное в промышленности и сельском хозяйстве. Одновременно с ежегодным ростом производства ПАВ соотношение между их применением в быту и промышленности изменяется в пользу промышленности.
ПАВ находят применение более чем в 100 отраслях народного хозяйства. Большая часть производимых ПАВ используется в составе моющих средств, в производстве тканей и изделий на основе синтетических и природных волокон. К крупным потребителям ПАВ относятся нефтяная, химическая промышленности, промышленность строительных материалов и ряд других (Новиков, 2002).
Применение ПАВ определяется их поверхностной активностью, структурой адсорбционных слоев и объемными свойствами растворов. Поверхностно-активные вещества используют в качестве диспергаторов при измельчении твердых тел, бурении твердых пород (понизители твердости), для улучшения смазочного действия, понижения трения и износа, интенсивности нефтеотдачи пластов и т.д. Другой важный аспект использования ПАВ – формирование и разрушение пен, эмульсий, микроэмульсий. Широкое применение ПАВ находят для регулирования структурообразования и устойчивости дисперсных систем с жидкой дисперсионной средой (водной и органической). Широко используются мицеллярные системы, образуемые ПАВ как в водной, так и в неводной среде, для которых важны не поверхностная активность ПАВ и не свойства их адсорбционных слоев, а объемные свойства: резко выраженные аномалии вязкости с повышением концентрации ПАВ вплоть до образования, например в водной среде, кристаллизации структур твердого мыла или твердообразных структур (в пластичных смазках на основе нефтяных масел) (Абрамзон, 1981).
Водные растворы ПАВ в большей или меньшей концентрации поступают в стоки промышленных вод и, в конечном счете – в водоемы. Очистке сточных вод от ПАВ уделяется большое внимание, так как из-за низкой скорости разложения ПАВ вредные результаты их воздействия на природу и живые организмы непредсказуемы. Сточные воды, содержащие продукты гидролиза полифосфатных ПАВ, могут вызвать интенсивный рост растений, что приводит к загрязнению ранее чистых водоемов: по мере отмирания растений начинается их гниение, а вода обедняется кислородом, что в свою очередь ухудшает условия существования других форм жизни в воде.
Имеются убедительные данные о том, что ПАВ, содержание которых в сточных водах в настоящее время значительно, способны стимулировать рост и сохранение ряда патогенных микроорганизмов. В.В. Шелакова (1975) в эксперименте установила, что такие вещества, как хлорный сульфонел, синтанол ДС‑10, алкамон ОС‑2 и ряд других при определенных условиях обладают способностью стимулировать развитие сальмонелл (S.typhimurium). Г.А. Багдасарьян с соавт. (1977) отмечают, что алкилосульфат в концентрациях 5–10 мг/л (что соответствует среднему уровню загрязнения речной воды у места выпуска стоков) стимулирует рост шигелл Зонне и Флекснера, другие концентрации этого вещества активировали S. typhi S. paratyphi В, S. typhimurium (Хотько, Дмитриев, 2006).
Особенностью этой группы загрязнителей является то, что от других продуктов органического синтеза они, так же как и пестициды, полностью попадают в окружающую среду, и, прежде всего в воду, и почву (Ставская, 1981).
1.2 Общая характеристика синтетических моющих средств
Синтетические моющие средства (CMC, детергенты) – многокомпонентные композиции, применяемые в водных растворах для интенсификации удаления загрязнений с различных твердых поверхностей – тканей, волокон, металлов, стекла, керамики. В более узком смысле под СМС обычно понимают бытовые средства для стирки белья и одежды.
По товарной форме СМС разделяют на сыпучие (порошкообразные, хлопьевидные), пастообразные, жидкие и кусковые; по назначению – на бытовые и технического назначения; по сфере применения и специфике отмываемого субстрата – на универсальные средства для стирки, средства для машинной стирки сильно загрязненного белья, стирки изделий из тонких, чувствительных к повреждению и усадке тканей, стирки и отбеливания с кипячением, для предварительного, замачивания, средства с ферментами для низкотемпературной стирки, средства с противоусадочным, смягчительным, антистатическим, освежающим цвет или иным эффектом, специальные СМС для детского белья и т.д.
СМС обычно включают мицеллообразующие поверхностно-активные вещества (ПАВ), обладающие моющим, смачивающим и антистатическим действием, различные электролиты, комплексоны, добавки, обеспечивающие антиресорбционное действие (предотвращают повторное отложение частиц загрязнения), парфюмерную отдушку, маскирующую специфический запах композиции и ароматизирующую белье, а также всевозможные специальные добавки: оптические и пероксидные отбеливатели, ферменты, активаторы и стабилизаторы, растворители, гидротропы, ингибиторы коррозии, консерванты, пеногасители, красители, пигменты, антиоксиданты и др.
Основа многих СМС – анионные ПАВ, например алкилбензолсулъфонаты (преимущественно линейные, обладающие хорошей биоразлагаемостью), алкилсульфаты, алкилэтоксисульфаты, мыла, алкансулъфонаты, олефинсульфонаты натрия.
В связи с общемировой тенденцией к снижению температуры стирки и использованию СМС с ферментами и катионными смягчителями-антистатиками повысилась роль неионогенных ПАВ – оксиэтилированных спиртов, оксиэтилированных алкилфенолов, оксиэтилированных алкиламинов. В качестве вспомогательных ПАВ, усиливающих тот или иной эффект и смягчающих нежелательное дерматологическое действие, в СМС могут вводиться в небольших количествах алкил- и алкилэтоксифосфаты, таураты, сульфосукцинаты, соли сульфокарбоновых кислот, эфирокарбоксилаты, оксиалкиламиды жирных кислот и их этоксилаты, N‑оксиды третичных аминов, блоксополимеры алкиленоксидов, амфогерные производные аминокислот, имидазолина и бетаина. Некоторое распространение (особенно в США) получили СМС на базе анионных и неионогенных ПАВ с добавками катионных ПАВ или полимеров, способные в процессе полоскания вследствие адсорбции на волокнах снижать электростатический заряд и усадку ткани.
Примеры таких катионных ПАВ – диалкилдиметиламмонийхлорид, 1 – (2‑алкиламидоэтил) 2‑алкил‑3‑метилимидазолинийметилсульфат, катионное производное гидроксиэтилцеллюлозы. Оптимальным моющим действием при 25–35 °С обычно обладают ПАВ с алкильной цепью С12‑С14, с ростом температуры стирки оптимум отмечается у гомологов С14‑С16.
При составлении рецептур СМС часто используют сочетания 2–3 ПАВ – синергетиков, различающихся растворимостью, устойчивостью к солям жесткости и моющей эффективностью в отношении твердых, жировых и белковых загрязнений. Количество ПАВ различных типов в СМС достигает 35% по массе.
Хорошее моющее действие анионных и неионогенных ПАВ обычно достигается в щелочной области рН и в присутствии различных электролитов. Практически все порошкообразные СМС содержат минеральные соли, из которых наиболее применяемы фосфаты: триполисфосфат Na, тринатрийфосфат, тетракалийпирофосфат и др., способные образовывать комплексы с поливалентными катионами. В жидких рецептурах преимущественно используют тринатрийфосфат, триполифосфат К и хлорированный тринатрийфосфат (в дезинфицирующих моющих средствах для посуды), в ферментсодержащих – небольшое количесво солей Са или Mg. Полностью или частично функцию фосфатов в СМС могут выполнять комплексоны – Na‑соли нитрилотриуксусной кислоты (трилон А) и этилендиаминтетрауксусной кислоты (трилон Б), соли этилидендифосфоновой и лимонной кислот, а также цеолиты. Использование эффективных заменителей фосфатов в СМС весьма актуально в связи с загрязнением водоемов биогенными элементами. Количество комплексообразователей в СМС составляет до 40% по массе.
В качестве электролитов-активаторов моющего действия в стиральные порошки вводят Na2SO4, Na2CO3 и Na2SiO3 (или жидкое стекло). Последние два (в количестве до 10% по массе) обеспечивают щелочную среду; Na2SiO3, кроме того, ингибирует корродирующее действие моющей композиции.
В качестве антиресорбентов в СМС обычно используют карбоксиметилцеллюлозу, полимеры или сополимеры акриловой кислоты в количестве от 0,5 до 2% по массе.
1.3 Поверхностно-активные вещества как компоненты СМС
Поверхностно-активные вещества получили свое название благодаря общему свойству – способности накапливаться (адсорбироваться) на поверхности раздела сред. Это свойство обусловлено строением ПАВ: их молекулы наряду с неполярной (гидрофобной) присутствует полярная (гидрофильная) группа. Будучи, таким образом, дифильными (биполярными), молекулы или ионы ПАВ адсорбируются из воды на поверхности раздела, ориентируясь при этом так, что гидрофильные группы остаются в водной, а гидрофобные выталкиваются в неводную фазу. При этом образуется мономолекулярный слой вещества и поверхностное натяжение снижается. Важной особенностью ПАВ является, то, что они способны к мицеллообразованию. Большая часть ПАВ используется в качестве компонентов моющих средств (МС) или детергентов. Детергенты помимо ПАВ содержат целый ряд добавок, усиливающих их моющее действие (Ставская, 1981). ПАВ принято делить на следующие группы: ионогенные, диссоциирующие в воде на ионы, и неионогенные (НПАВ), растворимость, в воде обусловлена не диссоциацией, а образованием водородных связей между молекулами воды и кислородом ПАВ.
Существуют природные поверхностно-активные вещества неионогенного характера, но так как они мало известны, обычно под термином ПАВ подразумевают синтетические поверхностно-активные вещества (СПАВ).
К ионогенным относятся анионные ПАВ (АПАВ), катионные поверхностно-активные вещества (КПАВ) и амфолитные ПАВ. АПАВ диссоциируют с образованием микроаниона, обуславливающего поверхностную активность соединения, и противоиона металла, например Na, K. У КПАВ поверхностной активностью обладает микрокатион. Амфолитные ПАВ ведут себя в растворах как амфотерные соединения. В кислой среде благодаря наличию аминогрупп они диссоциируют как КПАВ, в щелочной – за счет имеющихся в их составе карбоксильных групп данные вещества распадаются на ионы аналогично АПАВ. Среди анионных ПАВ наиболее широко применяют алкилсульфаты, алкилсульфонаты и алкиларилсульфонаты. К этой группе относятся так же мыла (Ставская, 1981).
Неионогенные ПАВ более разнообразны по своей химической структуре чем анионные. Они представляют собой продукты присоединения окиси этилена к веществам, содержащим активный водород, например, к алкилфенолам, жирным спиртам, меркаптанам. Практически любое соединение, молекула которого наряду с гидрофобным радикалом содержит корбоксильную, гидроксильную, амидную или аминную группу с подвижным атомом водорода, может реагировать с окисью этилена, образуя неионогенное ПАВ.
Их растворимость обусловлена наличием в молекулах гидрофильных эфирных и гидроксильных групп, чаще всего полиэтиленгликолевой цепи. По-видимому, при растворении образуются гидраты вследствие образования водородной связи между кислородными атомами полиэтиленгликолевого остатка и молекулами воды. Вследствие разрыва водородной связи при повышении температуры растворимость неионогенных ПАВ уменьшается.
Характерная особенность неионогенных ПАВ – жидкое состояние и малое пенообразование в водных растворах.
Неионогенные ПАВ разделяют на группы, различающиеся строением гидрофобной части молекулы, в зависимости от того, какие вещества послужили основой получения полигликолевых эфиров. На основе спиртов получают оксиэтилированные спирты RO(C2H4O) nH; на основе карбоновых кислот – оксиэтилированные жирные кислоты RCOO(C2H4O) nH; на основе алкилфенолов и алкилнафтолов – оксиэтилированные алкилфенолы RC6H4O(C2H4O) nH; на основе аминов, амидов, имидазолинов-оксиэтилированные алкиламины RN[(C2H4O) nH]2; на основе сульфамидов и меркаптанов – ПАВ типа RSO2NC(C2H4O) nH]2 и RS(C2H4O) nH.
Гидрофильную группу в молекуле НПАВ могут образовывать, помимо окиси этилена, и другие соединения. Так, довольно широко применяются НПАВ – сложные эфиры маннита и сорбита, которые называют соответственно маннитаты и сорбитаты или спаны. Оксиэтилированные эфиры сорбита и маннита нашли распространение под названием «твины». Хорошо известны НПАВ, в состав которых, наряду с окисью этилена, входят остатки окиси пропилена – так называемые блок-сополимеры. Токсическое действие неионогенных поверхностно-активных веществ определяется главным образом неполярной частью молекулы, при этом оно более выражено при наличии в последней ароматического кольца (Ставская, 1981).
Неионогенными ПАВ являются продукты конденсации гликозидов с жирными спиртами, карбоновыми кислотами и этиленоксидом.
Получение неионогенных ПАВ в большинстве случаев основано на реакции присоединения этиленоксида при повышенной температуре под давлением в присутствии катализаторов (0,1–0,5% CH3ONa, KOH или NaOH).
Неионогенные ПАВ менее чувствительны к солям, обусловливающим жесткость воды, чем анионактивные и катионактивные ПАВ. Смачивающая способность неионогенных ПАВ зависит от структуры; оптимальной смачивающей способностью обладает ПАВ разветвленного строения:
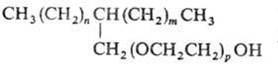
Неионогенные ПАВ хорошо совмещаются с другими ПАВ и часто включаются в рецептуры моющих средств.
Разнообразие химического строения НПАВ, создает трудности при анализе этих веществ и приводит к получению противоречивых результатов при изучении их биоразлагаемости (Ставская, 1981).
В данной работе проводились исследования микроорганизмов-деструкторов ПАВ. Используемые микроорганизмы выделялись из почвы. В качестве селективного агента использовался полиакриламид (ПАА). Полиакриламид – твердое аморфное белое или частично прозрачное вещество без запаха, растворимое в воде. Молекулярная масса составляет до 5500000. ПАА используется как флокулянт при осветлении сточных вод, коагулянт в металлургии, флотореагент, диспергатор, загуститель. Он содержится в сточных водах сульфатцеллюлозных заводов и обогатительных фабрик. В воде ПАА постепенно гидролизуется до аммониевой соли полиакриловой кислоты. Молекулярный вес полиакриламида зависит от степени гидролиза. Бывает жидкий, в виде сухих порошков и в форме эмульсии.
Химическая структура полиакриламида
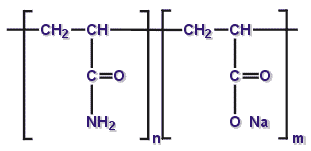
Способность ПАА к химическим превращениям с образованием различных ионных производных, разветвленных и сшитых продуктов расширяет области применения полимеров. Рассмотрим наиболее важные химические свойства ПАА (Савицкая, 1969).
ПАА легко гидролизуется в присутствии кислот и щелочей. Взаимодействует с формальдегидом в щелочной среде (рН 8–10) при 20 оС с образованием полиметилолакриламида, который применяется для аппретирования тканей (пропитка или обработка поверхности с целью придания несминаемости и жесткости), обезвоживания осадков сточных вод и обогащения железных руд.
При обработке ПАА формальдегидом и вторичным амином в щелочной среде образуется аминометилированный полимер, который по флокулирующей способности превосходит исходный полимер.
Реакция сульфометилирования необходима для получения анионных производных ПАА при взаимодействии его с формальдегидом и бисульфитом натрия в щелочной среде (рН 13).
В составе макромолекул наряду с сульфометилированными группами могут содержаться карбоксилатные группы (вследствие щелочного гидролиза амидных групп), а также непрореагировавшие амидные группы. В этом случае получаются эффективные структурообразователи грунтов, антистатические агенты для текстильных материалов и флокулянты для различных типов суспензий (Савицкая, 1969).
Реакции сшивки ПАА применяют для получения водопоглощающих изделий, пленок, защитных покрытий и капсул для лекарств, семян, удобрений. Образование трехмерных структур возможно также при действии на ПАА кислотами (Петрянова-Соколова, 1987).
1.4 Влияние поверхностно-активных веществ на микроорганизмы
Многие синтетические поверхностно-активные вещества обладают антимикробными свойствами. (Ставская, 1981).
Кроме природной устойчивости некоторых микроорганизмов к биоцидным препаратам, микроорганизмы быстро адаптируются к неблагоприятным факторам, в том числе и к воздействию антимикробных средств. Этот феномен объясняется, в первую очередь, выживанием в условиях контакта с биоцидом наиболее устойчивых (резистентных) штаммов бактериальной популяции. В итоге, вследствие мутации, выживают клетки, имеющие измененный ген. Описаны случаи размножения потенциально патогенных микроорганизмов в растворах, предназначенных для дезинфекции, адаптации к терапевтическим дозам антибиотиков и полирезистентности к десяткам антимикробных средств.
Антимикробное действие ПАВ зависит, прежде всего, от типа соединения. Наиболее высокое бактерицидное действие проявляют катионные вещества, неионогенные – слабое, анионактивные занимают промежуточное положение.
Анионные ПАВ влияют главным образом на грамположительные бактерии (Ставская, 1981, цит. Kaminski, 1963). Антимикробный эффект АПАВ зависит от их химического строения. Чем больше атомов углерода, тем сильнее действие соединения. Активность анионных соединений усиливается при снижении рН среды (Ставская, 1981, цит. Flett, 1945).
Неионогенные вещества характеризуются более слабым антимикробным действием; некоторые из них совсем не обладают активностью. Характер влияния на микроорганизмы зависит от химического строения НПАВ. Твины не только не угнетают микроорганизмы, но даже стимулируют их рост (Ставская, 1981, цит. Stinson, 1971). В присутствии неионогенных ПАВ в значительных концентрациях не наблюдается спороношения у мицелиальных грибов, хотя и происходит их рост (Ставская, 1981, цит. Furuta 1945).
Катионные ПАВ активны по отношению к грамположительным и грамотрицательным микроорганизмам. По отношению к грибам катионные вещества наиболее активны (Ставская, 1981, цит. Furuta, 1945). В присутствии полисахаридов (агар-агара, крахмала, целлюлозы) и белковых веществ (казеина, сыворотки крови, пептона, желатины, альбумина) снижается антимикробная активность ряда катионных и амфотерных ПАВ. Причем бактериостатическое действие на грамотрицательные бактерии снижается в большей степени, чем на грамположительные, в то время как бактерицидное действие уменьшается одинаково (Ставская, 1981, цит. Koppensteiner, 1974).
Для катионных ПАВ мишенями являются карбоксильные группы аминокислот и кислых полисахаридов бактерий, а для анионных ПАВ – кетонные группы белков, аминогруппы соответствующих углеводов и липидов, а также фосфатные группы тейхоевых кислот.
В естественных условиях микробные клетки обладают общим отрицательным зарядом, поэтому наиболее широкое практическое применение нашли катионные ПАВ, которые губительно действуют на грамположительные и грамотрицательные бактерии, дрожжевые и нитчатые грибы. Но в клетке также имеются молекулы, несущие положительные заряды, поэтому и анионные ПАВ губительно действуют на микроорганизмы, но при более высоких концентрациях.
Сильное дестабилизирующее действие на мембраны клеток оказывают низкомолекулярные катионные ПАВ (цитилпиридиний хлорид, хлоргексидин, алкилди-метил бензил аммоний хлорид) (Поликарпов, 2005).
Много исследований посвящено изучению механизма антимикробного действия ПАВ. Известно, что химические вещества могут влиять на микроорганизмы специфически и неспецифически. Специфически – при очень низких концентрациях антимикробного соединения, которое может реагировать с определенными компонентами клетки, нарушая их нормальное функционирование. Неспецифическое действие на клетку обычно проявляется при достаточно высоких концентрациях веществ. Оно может быть связано с неблагоприятным для микроорганизма изменением поверхностного натяжения, рН, с установлением высокого осмотического давления и т.д. Что касается ПАВ, то до сих пор не существует единого мнения, как – специфически или неспецифически – влияют они на микроорганизмы.
Большинство исследователей предполагают, что ПАВ действуют на микроорганизмы специфически. Эту мысль подтверждает тот факт, что неионогенные ПАВ, которые понижают поверхностное натяжение, почти не обладают антимикробной активностью (Ставская, 1981).
Все работы, посвященные изучению механизма антимикробного действия ПАВ, проводились в таких основных направлениях: изучение адсорбции ПАВ и образования комплексов на поверхности микробной клетки, изучение электрохимических свойств поверхности клетки в присутствии ПАВ, наблюдение изменения проницаемости микробных клеток под влиянием этих соединений и определение их действия на физиологические процессы и ферментативную активность микроорганизмов (Ставская, 1981).
Адсорбцию ПАВ на поверхности микробной клетки считают первым этапом взаимодействия микроорганизмов с химическим соединением.
Методом микроэлектрофореза показано, что ионные ПАВ, адсорбируясь на клеточной поверхности бактерий, изменяют ее заряд. При этом катионактивные вещества уменьшают отрицательный заряд и даже могут изменять его на положительный, тогда как анионные соединения, как правило увеличивают отрицательный заряд (Ставская, 1981, цит. Dyar 1946).
В результате взаимодействия ПАВ с компонентами поверхности микробной клетки изменяются ее свойства. Некоторые ПАВ вызывают удлинение, утолщение и искривление бактериальных клеток (Ставская, 1981, цит. Schweisfurth, 1959).
ПАВ связываются с компонентами ЦПМ и нарушают ее нормальное функционирование, в том числе свойство полупроницаемости. Показано, что под влиянием этих веществ из клеток в окружающую среду выделяются низкомолекулярные метаболиты. Под влиянием ПАВ может происходить потеря плазмид бактериальными клетками (Ставская, 1981).
Возможно, именно нарушением проницаемости объясняется повышение чувствительности резистентных штаммов бактерий к антибиотикам в присутствии ПАВ. Так, некоторые ПАВ при их совместном использовании с антибиотиками в 2–3 раза увеличивает активность хлортетрациклина в отношении устойчивых штаммов бактерий (Ставская, 1981, цит. Suling, 1966).
Конечным результатом действия ПАВ на микробную клетку является деструктуризация клеточной оболочки. Механизм этого действия изучил Цапф (Ставская, 1981), который с помощью электронной микроскопии показал, что ПАВ проникают внутрь клетки, нарушая деятельность протеаз, что приводит к автолизу клеточного содержимого (Ставская, 1981).
Некоторые авторы наблюдали угнетение некоторых физиологических процессов и ферментативной активности микроорганизмов (Ставская, 1981, цит. Sevcik, 1957). В то же время имеются сообщения о стимуляции активности дыхания и некоторых ферментов в присутствии ПАВ. Исследователи предполагают, что ферментные системы клеток повреждаются вторично, в то время как первично изменяются поверхностные и внутренние мембранные структуры, с которыми связано много ферментов. Одновременно может наблюдаться непродолжительная стимуляция активности ферментов, растворенных в жидкой части цитоплазмы. При этом клетка как бы пытается заменить поврежденную ферментную систему неповрежденной (Ставская, 1981).
Согласно имеющимся литературным данным, микроорганизмы могут приобрести резистентность, как к катионным, так и к анионным ПАВ.
Можно предположить, что некоторые из резистентных к ПАВ микроорганизмов в процессе адаптации приобретают способность трансформировать эти соединения, а потом использовать их как источник энергии и углерода. Сведения о механизме антимикробного действия ПАВ, и в особенности о характере приобретения устойчивости к этим веществам, могут пролить свет на проблему изучения биологических особенностей микроорганизмов, осуществляющих в природе трансформацию и деструкцию синтетических соединений – загрязнителей окружающей среды (Ставская, 1981).
1.5 Микробиологическая деструкция поверхностно-активных веществ
Большую угрозу загрязнения окружающей среды представляют анионные и неионогенные поверхностно-активные вещества, широко используемые в качестве компонентов моющих средств или детергентов (от англ. «deterge» – очищать).
Наряду с моющим действием ПАВ характеризуются эмульгирующими, диспергирующими, солюбилизирующими и другими полезными свойствами, в связи, с чем находят самое разнообразное применение в промышленности, сельском хозяйстве, быту, медицине и т.д.
При попадании в водную среду и почву молекулы ПАВ подвергаются деструкции в результате биохимических и физико-химических процессов, и «потребляются» (разрушаются) микроорганизмами, присутствующими в воде, почве и активном иле (Алексеева, 1998).
По стадийности деструкции и потребления молекул ПАВ в процессе их биоразложении различают:
– первичную биоразлагаемость – разрушение структуры молекулы с «отщеплением» гидрофильных групп, и, обусловленную этим потерю поверхностно-активных свойств молекул ПАВ, что проявляется, в первую очередь, исчезновением пенообразования;
– полную биоразлагаемость – дальнейшее усвоение осколков молекул ПАВ микробными сообществами вплоть до разложение на СО2 и Н2О.
Первые методы определения биоразлагаемости ПАВ появились более 50 лет назад в связи с повсеместными загрязнениями водоемов в европейских странах и появлением большого количества пены на поверхности водных объектов. Это было обусловлено сбросом стоков, не очищенных от синтетических моющих средств на основе тетрапропи-ленбензолсульфонатов.
Химические и физико-химические методы очистки стоков не решают проблемы борьбы с загрязнением окружающей среды ПАВ, так как при использовании этих методов ПАВ, как правило, только концентрируются или разрушаются частично, но не разлагаются полностью до углекислого газа и воды и других простейших продуктов. Полная деструкция детергентов осуществляется микроорганизмами, на использовании которых основаны все биологические методы очистки сточных вод. Однако очистка стоков от ПАВ общепринятыми биологическими методами затруднена, поскольку многие из этих веществ сравнительно устойчивы к микробному разложению и проходят через очистные сооружения, не изменяясь.
По этим причинам объективная оценка биоразлагаемости ПАВ, являющихся основными компонентами синтетических моющих средств и товаров бытовой химии, на которые используется до половины всего объема их производства, чрезвычайно актуальна.
В практике в настоящее время наиболее широко используются анионные ПАВ.
Процессы деструкции многих ПАВ в природе происходят очень медленно, так как у микробного населения водных объектов отсутствует адаптация к этим веществам. Тем не менее, они подвержены процессам биохимического окисления, скорость которых зависит от структуры их молекул, температуры воды (чем выше температура, тем интенсивнее идет окисление), рН, содержания взвешенных веществ и т.д. К числу наиболее легко окисляющихся ПАВ относятся первичные и вторичные алкилсульфаты нормального строения, а наиболее трудно разрушаются алкилбензолсульфонаты, приготовленные на основе тетрамеров пропилена. Единственной группой организмов, вносящей реальный вклад в разрушение ПАВ в окружающей среде, являются бактерии.
Большой интерес представляют исследования разложения ПАВ чистыми культурами микроорганизмов. Первые работы на эту тему проводились в 50-х годах. Так, Ризен (Ротмистров, 1978, цит. Risen, 1956) показал, что Ps. aeruginosa, Serratia marcescens, Escherichia coli, Aerobacter aerogenes, Salmonella enteritidis, Paracolobactrum aerogenoides при выращивании на синтетической среде могут использовать различные анионные ПАВ в качестве единственного источника углерода. Обнаружено, что на скорость биоразложения влияет минеральный состав питательной среды.
Пейн с сотрудниками (Ротмистров, 1978, цит. Payne, 1963) из почвы, взятой, в районе очистного сооружения методом накопительных культур выделил 2 штамма Pseudomonas – С12 и С12В, которые активно разрушали АПАВ. Представители рода Pseudomonas особенно часто выделяются из накопительных культур на средах с АПАВ. Методом накопления, ими также были получены один штамм Ps. fluorescens и два штамма Nocardia sp., способные использовать в качестве единственного источника углерода линейные АПАВ. В процессе исследования Пейн с сотрудниками установили, что способность разрушать ПАВ широко варьирует у микроорганизмов, даже среди представителей одного рода.
Авторы высказывают предположение о том, что выращивание Azotobacter на детергентсодержащих сточных водах, может иметь в будущем большое значение, так как благодаря фиксации атмосферного азота вода обогащается азотными соединениями, а это в свою очередь способствует развитию других микроорганизмов – деструкторов.
В литературе есть указания (Ставская, 1978; Ротмистров, 1978) на возможность биодеградации серусодержащих детергентов путем гидролиза в анаэробных условиях, однако биохимическая сторона этого процесса не изучена. Установлено только, что синтетические ПАВ с разветвленной алкильной цепью практически не разлагаются, в то время как прямоцепочечные за 3–6 ч. разрушаются на 20% (Ротмистров, 1978).
О биоразлагаемости неионогенных ПАВ, применяемых в качестве деэмульгатаров эмульсий нефти с водой есть сведения в работе В.В. Булатникова с соавт. Большинство этих соединений плохо поддаются биохимическому окислению. Авторы показывают, что деэмульгаторы – блок-сополимеры окиси этилена и пропилена относятся к «биологически жестким». Легко и быстро разрушаются НПАВ, полученные на основе первичных жирных спиртов и сахаров (Ротмистров, 1978).
Работы по изучению деструкции НПАВ чистыми культурами микроорганизмов немногочисленны. Показано, что твины могут служить питательным субстратом для бактерий, а так же способствовать использованию других соединений, облегчая их транспорт в клетку (Ротмистров, 1978, цит. Ксандопуло, 1971). Ps. aeruginosa, Aspergillus niger и Penicillium notatum способны расти в растворах сложных эфиров жирных кислот (Ротмистров, 1978). Образуя эстеразы, эти микроорганизмы расщепляют эфирные связи с освобождением жирных кислот. Способностью разлагать полиоксиэтиленолеат обладают некоторые штаммы непатогенных микобактерий, которые окисляют его до углекислоты и воды. Микобактерии используют данное соединение в качестве единственного источника углерода.
Работами проводимыми в Институте коллоидной химии и химии воды АН УССР канд. Биол. Наук В.М. Удодом (Ставская, 1978), показано, что додециловый эфир полиэтиленгликоля в концентрации 50–100 мг/л полностью разрушается микроорганизмами родов Pseudomonas, Bacillus и Candida в течение 18 ч. Увеличение концентрации приводит к замедлению деструкции, и разложение наступает на 2–7 сутки.
Анализ литературных данных показал, что в природе довольно часто встречаются микроорганизмы, способные разрушать биологически «мягкие» поверхностно-активные вещества, в том числе неионогенные, такие как оксиэтилированные спирты и кислоты, и гораздо реже – «жесткие», например оксиэтилированные алкилфенолы. Известно, что чем больше ксенобиотик отличается от природных субстратов и метаболитов основного обмена, тем меньше вероятность широкого распространения штаммов, способных к его утилизации. Лишь там, где имеет место длительный контакт микроорганизмов, обладающих высокой гибкостью метаболических реакций, с соответствующим веществом, возможно формирование штаммов деструкторов (Ставская, 1978). Такими объектами являются загрязненные почвы, сточные воды и активные илы очистных сооружений. Тем не менее, даже из таких источников не всегда удается выделить интересующий микроорганизм.
Накопившиеся в последние годы, данные о биоразлагаемости ПАВ свидетельствуют, о необходимости, с одной стороны, синтеза и внедрения в производство легко биоразрушаемых соединений, а с другой – разработки новых, более интенсивных методов очистки окружающей среды от ПАВ. Эти методы должны основываться на использовании специально полученных высокоактивных чистых культур микроорганизмов, деструкторов ПАВ. Применение таких культур в микробном методе очистки будет способствовать защите окружающей среды от загрязнения синтетическими соединениями, и сохранению окружающей человека природы.
1.6 Действие СМС на экосистемы и здоровье человека
1.6.1 Действие СМС на экосистемы
Неуклонное увеличение количества химических соединений, используемых в промышленности, сельском хозяйстве, медицине и быту, создает принципиально новую по своей опасности экологическую ситуацию для человечества, состояния окружающих человека флоры и фауны. Детергенты – синтетические поверхностно-активные вещества (ПАВ) являются также «детищем» научно-технической революции XX века. Они широко используются для производства СМС. Прогнозируемая необходимость ПАВ на ближайшие годы для стран СНГ составляет свыше 1,206 млн. т. По сравнению с 1985 г. применение детергентов в Украине, например, увеличилось почти в 2 раза. Естественно, это может отрицательно повлиять на качество окружающей среды. Основной причиной такого влияния является, с одной стороны, несовершенство существующих методов очистки промышленных, бытовых стоков и производственных выбросов в атмосферный воздух, с другой – отсутствие в ряде населенных пунктов, а также на некоторых предприятиях очистных сооружений.
Преобладающее большинство ПАВ (более 95%) относится к 3‑му и 4‑му классам опасности (умеренно- и малотоксичные). Пороговые концентрации их биологического действия, как правило, в 30–50 раз выше установленных ПДК (0,1–0,5 мг/л), что обеспечивает надежную защиту человека и окружающей среды. Коммунальные стоки содержат в среднем от 2 до 5 мг/л ПАВ (в 4 – 50 раз выше ПДК). В промышленных стоках содержание ПАВ может достигать от 10 до 100 мг/л.
В случае если уровни загрязнений ПАВ в воде превышают ПДК в 10–20 раз, это приводит к ухудшению, в первую очередь, органолептических качеств воды, не повышая существенно гигиенической опасности по ее токсичности для человека, животных и птиц. Однако при этом возможно появление на поверхности воды пены, в которой концентрируются и активно размножаются полезные и патогенные микроорганизмы.
Они распространяются течением и ветром на значительные расстояния, и тем самым стабильные молекулы ПАВ создают угрозу здоровью населения. Присутствие ПАВ повышает также степень опасности других вредных веществ, находящихся в воде и почве при последующих их перемещениях по пищевым цепочкам (www.aquaria.com.ua/coretra.html).
Учитывая уровень производства, распространенность в объектах окружающей среды, широкомасштабное применение в различных отраслях промышленности и быту, можно утверждать, что наиболее значимыми являются анионные ПАВ. При значительном загрязнении почвы тяжелыми металлами, нитратами и присутствии детергентов последние повышают подвижность токсикантов по вертикальному профилю почвы и их переходу с почвы в растениеводческую продукцию. При этом сами детергенты в присутствии в почве других загрязнителей, в частности металлов, также мигрируют в грунтовые воды и транслоцируются в сельхозкультуры в больших количествах, чем в случае присутствия ПАВ в почве в изолированном виде. При значительном поступлении детергентов в почву (свыше 15 мг на кг) создаются наилучшие условия для размножения и длительного выживания микрофлоры, в том числе и патогенной, что может представлять, особенно в летний период, эпидемическую опасность и угрозу здоровью населения. Токсичность детергентов по гигиеническим критериям сравнительно невысока, однако наличие целого ряда специфических свойств (пенообразование, эмульгирование, солюбилизация, влияние на поведение веществ в окружающей среде и др.) у данных загрязнителей позволяет отнести их к разряду вредных веществ, которые способны спровоцировать конфликтную экологическую ситуацию и оказать неблагоприятное влияние на здоровье человека (Голубева, 2006).
В состав многих СМС помимо ПАВ входят разнообразные добавки. К числу наиболее вредных добавок относятся фосфаты.
Они представляют собой большую угрозу для окружающей нас среды. Попадая после стирки вместе со сточными водами в водоемы, фосфаты принимаются действовать как удобрения. «Урожай» водорослей в водоемах начинает расти не по дням, а по часам. Водоросли, разлагаясь, выделяют в огромных количествах метан, аммиак, сероводород, которые уничтожают все живое в воде. Зарастание водоемов и засорение медленнотекущих вод приводят к грубым нарушениям экосистем водоемов, ухудшению кислородного обмена в гидросфере и создают трудности в обеспечении населения питьевой водой. Еще и по этой причине во многих странах законодательно запретили применение фосфатных СМС (Голубева, 2006).
1.6.2 Действие ПАВ на организм человека
Очень многих волнуют вопросы, связанные с вредным влиянием на организм химикатов, входящих в состав широко рекламируемых в печати и по телевидению синтетических моющих средств (СМС), с качеством и безопасностью использования в быту различных видов стиральных порошков. Повсеместное использование СМС привело к формированию нового, постоянно действующего химического фактора среды обитания человека. И это при явном дефиците гигиенических знаний о безопасности употребления СМС.
Основные действующие вещества всех стиральных порошков – это поверхностно активные вещества (ПАВ), которые представляют собой чрезвычайно активные химические соединения. Обладая некоторым химическим родством с определенными компонентами мембран клеток человека и животных, ПАВ, при попадании в организм, скапливаются на клеточных мембранах, покрывая их поверхность тонким слоем, и при определенной концентрации способны вызвать нарушения важнейших биохимических процессов, протекающих в них, нарушить функцию и саму целостность клетки.
Синтетические ПАВ могут оказывать вредное действие на организм человека, т. к. обладают способностью проникать через гисто-гематические, в том числе плацентарные, барьеры, проявлять репродуктивную токсичность, нарушать липидный обмен, ПАВ усиливают проникновение других химических веществ в организм (Алексеева, 1998).
Многие химические соединения, входящие в рецептуру СМС и товаров бытовой химии, обладают кожно-резорбтивным действием, сенсибилизирующим действием, влияют на функции воспроизводства, обладают слабым кумулятивным действием. Отдельные компоненты СМС трансформируются в окружающей среде с образованием опасных для окружающей среды и здоровья людей соединений.
В экспериментах на животных ученые (Голубева, 2006) установили, что ПАВ существенно изменяют интенсивность окислительно-восстановительных реакций, влияют на активность ряда важнейших ферментов, нарушают белковый, углеводный и жировой обмен. Особенно агрессивны в своих действиях анионные ПАВ. Они способны вызвать грубые нарушения иммунитета, развитие аллергии, поражение мозга, печени, почек, легких. Это одна из причин, по которым в странах Западной Европы наложены строгие ограничения на использование АПАВ в составах стиральных порошков. В лучшем случае их содержание не должно превышать 2–7%.
На Западе уже более 10 лет назад отказались от применения в быту порошков, содержащих фосфатные добавки. На рынках Германии, Италии, Австрии, Голландии и Норвегии продаются только бесфосфатные моющие средства. В ФРГ применение фосфатных порошков запрещено федеральным законом. В других странах, таких как Франция, Великобритания, Испания, в соответствии с правительственными решениями, содержание фосфатов в СМС строго регламентировано (не более 12%) (www.aquaria.com.ua/coretra.html).
Это объясняется тем, что наличие фосфатных добавок в порошках приводит к значительному усилению токсических свойств АПАВ. С одной стороны, эти добавки создают условия для более интенсивного проникновения АПАВ через неповрежденную кожу, способствуют усиленному обезжириванию кожных покровов, более активному разрушению клеточных мембран, резко снижают барьерную функцию кожи. ПАВ проникают в микрососуды кожи, всасываются в кровь и распространяются по организму. Это приводит к изменению физико-химических свойств самой крови и нарушению иммунитета. У АПАВ есть способность накапливаться в органах. Например, в мозге оседает 1,9% общего количества АПАВ, попавших на незащищенную кожу, в печени – 0,6% и т.д. Они действуют подобно ядам: в легких вызывают гиперемию, эмфизему, в печени повреждают функцию клеток, что приводит к увеличению холестерина и усиливает явления атеросклероза в сосудах сердца и мозга, нарушает передачу нервных импульсов в центральной и периферической нервной системах (www.aquaria.com.ua/coretra.html).
Они не только усиливают проникновение АПАВ через кожу, но и увеличивают накопление этих веществ на волокнах тканей, подвергающихся стирке. Они способствуют такому прочному сцеплению АПАВ с тканью, что даже 10-кратное полоскание в горячей воде не приводит к полному освобождению одежды от АПАВ. Причем чем сложнее и разветвленнее структура волокна, тем большее количество молекул АПАВ могут к нему «прилипнуть». Сильнее всего держат ПАВ шерстяные, полушерстяные и хлопчатобумажные ткани. В среднем, потенциально небезопасные концентрации ПАВ сохраняются на тканях до 4 суток. Таким образом, создается очаг постоянной интоксикации внутри самого организма. Прочно закрепившись на одежде, молекулы АПАВ при соприкосновении с кожей относительно легко переносятся на ее поверхность и быстро всасываются внутрь, начиная свой разрушительный маршрут по организму (www.ecocoop.ru).
Говорят, что капля никотина убивает лошадь. Вот научный факт: 100 г. ПАВ убивают лошадь весом в 300 кг в течение 24 часов (Голубева, 2006).
2. Объекты и методы исследований
Объектом исследования являются чистые культуры микроорганизмов, выделенные из почв. В работе использовано 13 культур микроорганизмов, большинство из которых является Г+ спорообразующими аэробными палочками. Чистые культуры хранились в холодильнике в пробирках со скошенным питательном агаром. Перед началом исследований было произведено обновление штаммов, путем подращивания их на МПБ с последующим пересевом на ПА.
2.1 Методы исследований
2.1.1 Исследование физиолого-биохимических свойств
Для исследования физиолого-биохимических свойств микроорганизмов использовались дифференцировочные пластины. Пластина представляет собой панель с 20 конусообразными лунками, на дно которых нанесены соответствующие субстраты с индикаторами, стабилизированные поливиниловым спиртом. Панель закрывается крышкой. Панель и крышка изготовлены из полистирола. Субстрат с индикаторами вносят в лунки в жидком виде, затем высушивают и стерилизуют.
Специфическое действие препарата заключается в возможности дифференцировать бактерии на основе определения ферментативных систем по их действию на соответствующие субстраты.
Биохимические дифференцировочные пластины предназначены для определения ферментативной активности бактерий, выделяемых в ходе микробиологических исследований. Это может помочь при дальнейшей идентификации до рода и возможно вида.
Подготовка исследуемых образцов
Перед проведением исследования выделенные культуры подлежат изучению на чистоту.
Идентификацию культур, непосредственно из нативного материала, производят со скошенного мясо-пептонного агара (МПА). Используют культуры выращенных в течение 18–24 часов при температуре при температуре 37 оС, без предварительного подращивания их на МПБ (мясо-пептонном бульоне).
Если выделенная культура микроорганизма находилась какое-либо время на хранении при комнатной температуре или в холодильнике, производят предварительный посев ее на МПБ на 2–4 часа при температуре 37 оС, затеи осуществляют пересев культуры на скошенный МПА. Посевы инкубируют в течение 18–24 часов при температуре 37 оС.
Культуру с МПА используют для приготовления суспензии в стерильной 1% пептонной воде рH 7,2–7,4 и доводят мутность суспензии до 10 единиц по отраслевому стандартному образцу мутности бактериальных взвесей, стеклянному. При отсутствии отраслевого стандартного образца в 4,0 мл стерильной 1% пептонной воды вносят 2–3 петли исследуемой культуры до образования видимой мутности.
Проведение исследования
1. Вскрывают упаковку пластин.
2. Регистрируют на крышке панели номер засеваемого штамма.
3. Открывают крышку и располагают панель на столе.
4. Добавляют пипеткой по 0,15 мл микробной суспензии в стерильной 1% пептонной воде во все лунки панели, кроме 17,18,19 которые оставляют свободными.
5. Для создания анаэробных условий добавляют 1–2 капли стерильного вазелинового масла в лунки для определения аргининдегидрогеназы и уреазы (№№11,20).
6. Закрывают крышку панели.
7. Выдерживают пластины в течение 18–24 часов при температуре 37 оС.
Учет результатов
Учет результатов производят визуально в соответствии с цветовым указателем, приложенным к пластинам, 18–24 часа инкубации при 37 оС.
После окончания инкубации открывают крышку панели и в лунки для выявления ацетилметилкарбинола (№10) добавляют 1 каплю 6%-го раствора альфа нафтола и затем 1 каплю 40% раствора гидроокиси калия; для определения фосфатазы (№8) – 1 каплю 20% раствора гидроокиси натрия; для выявления нитратредуктазы (№9) добавляют 1 каплю реактива Грисса. Реакции учитывают немедленно в лунках №8,9, выявление ацетилметилкарбинола (№10) осуществляют через 15–20 минут после закапывания реактивов.
2.1.2 Определение способности роста на средах с добавлением поверхностно-активных веществ
Для определения способности роста на средах с добавлением различных ПАВ использовался чашечный метод. Производился глубинный посев по 1 мл бактериальной суспензии. Использовалось 2 среды: питательный агар и среда М9 (рецепты сред см. в приложении). В качестве селективных агентов использовались СМС на основе АПАВ и КПАВ, а также полиакриламид (ПАА) (НПАВ). ПАВ в количестве 1 мл вносились в среды перед стерилизацией (Турковская, 1997).
2.1.3 Определение активности
Определение способности штаммов подвергать деградации ПАВ определяли с помощью модифицированного нами метода лунок Турковской (Турковская, 1997,): в центре застывшей среды ПА/10 в чашках Петри стерильным пробочным сверлом вырезали лунку. Микроорганизмы высевались штрихом по радиусу от лунки к периферии чашки (посев производится секторами). Затем в лунку стерильно вносили исследуемое ПАВ. Контролем служили чашки с посевами без субстратов. Инкубирование проводили в термостате при 34 оС в течении 3 сут.
Результаты оцениваются через 2–3 суток. Отмечается рост от края чашки к центру, к лунке с ПАВ. Степень активности характеризуется количеством баллов по сравнению с контролем.
2.2 Материалы и оборудование
Культуры микроорганизмов, пробирки, колбы, чашки Петри, шпатели, штативы, предметные и покровные стекла, красители, спиртовка.
При любой микробиологической работе: при посевах, пересевах, выделении, сохранении чистых культур используются стерильные среды, стерильная посуда, стерильные инструменты, чтобы предотвратить возможность попадания посторонней микрофлоры. Посевы производятся в стерильных боксах.
Для обработки посуды применяется стерилизация сухим жаром. Она производится нагреванием в течении 2 часов, при температуре 170 0С в электросушильных шкафах.
Вся посуда перед стерилизацией должна быть вымыта, высушена и завернута в бумагу. Для заворачивания посуды используют газетную бумагу (которая не размокает).
Большинство питательных сред стерилизуют насыщенным паром под давлением в автоклавах. Повышение давления в автоклаве повышает температуру пара, образуемого внутри автоклава и, следовательно, температуру стерилизации (Теппер, 2004).
Среды. В работе использованы полноценные питательные среды: МПА, МПБ. В качестве селективной среды использовалась среда М9 (состав см. в приложении). В качестве селективных агентов использовались СМС на основе АПАВ и КПАВ, а также ПАА (НПАВ).
3. Экспериментальная часть
3.1 Культурально-морфологическая характеристика микроорганизмов
В работе использовалось 13 культур микроорганизмов. Культуральные и морфологические признаки исследуемых микроорганизмов представлены в таблице 1.
Таблица 1. Культурально-морфологичесие признаки микроорганизмов
|
№ штамма |
Признаки |
Окраска по Граму |
|
|
культуральные |
морфологические |
||
|
1 |
гладкая, светло-фиолетового цвета, полусухая, блеск слабый, полупрозрачная | мелкие, толстые палочки и споры | + |
|
3 |
полупрозрачная, светло-фиолетового цвета, шершавая, с блеском, слизистая | толстые споровые палочки, прямые и изогнутые, одиночные, по 2, цепочками, с овальными концами | + |
|
4 |
светло-фиолетового цвета, шершавая, с блеском, слизистая | толстые споровые палочки, одиночные, по 2, цепочками, с овальными концами | + |
|
5 |
слизистая, гладкая, с блеском, сероватого цвета, выделяет черный пигмент | мелкие, споровые палочки, одиночные и по 2 | + |
|
14 |
молочного цвета, бугорчатая, с блеском, гладкая, слизистая | очень длинные споровые палочки, изогнутые, овальные концы | + |
|
15 |
полупрозрачная, с блеском, шершавая, светло-фиолетового цвета, слизистая | короткие споровые палочки | + |
|
17 |
светло-малинового цвета, гладкая, блестящая, полусухая | крупные палочки, неравномерно прокрашенные, фрагментированные палочки, споры | + |
|
19 |
культура желтоватого цвета, слизистая консистенция, гладкая | мелкие, неспоровые палочки, тонкие, овальные концы | + (–) |
|
ХХ |
серовато-бежевая колония, блестящая, прозрачная, точечный рост, слизистая консистенция, очень слабый | очень длинные палочки, неспоровые, прямые и изогнутые, с чехлами | + |
|
с |
кремового цвета, гладкая, слизистая, с блеском | кокки, разные | + |
|
b |
кремового цвета, бугорчатая, блестящая, слизистая | мелкие палочки, одиночные, по 2, слабо прокрашенные | + |
|
а1 |
сероватого цвета, гладкая, слизистая, с блеском | мелкие, короткие палочки | + |
|
а2 |
полупрозрачная, с блеском, ризоидная поверхность, слизистая | очень мелкие палочки, неярко прокрашенные | + |
Из таблицы видно, что большинство из исследуемых микроорганизмов являются Г+ спорообразующими аэробными палочками, за исключением штаммов b, а1, а2 которые являются Г+ неспоровыми аэробными палочками.
Штамм «с» это Г+ кокки. Однако в более молодой культуре он был представлен Г+ палочками. Также можно отметить, что штамм 19 это грамвариабельные неспоровые палочки.
3.2 Физиолого-биохимическая характеристика микроорганизмов
В работе использовано 13 культур микроорганизмов. Были исследованы физиолого-биохимические свойства по 17 тестам. Результаты приведены в таблице 2.
Таблица 2. Физиолого-биохимические свойства микроорганизмов
|
№ штамма |
1 |
3 |
хх |
5 |
4 |
14 |
15 |
17 |
19 |
а1 |
а2 |
b |
с |
|
тест |
|||||||||||||
| утилизация глюкозы | + | + | + | + | - | + | + | - | + | - | - | + | - |
| утилизация фруктозы | + | + | + | + | - | + | + | + | - | - | + | + | - |
| утилизация маннозы | + | + | + | + | + | + | + | + | + | + | + | + | - |
| утилизация мальтозы | + | + | + | + | - | + | + | + | - | - | - | - | - |
| утилизация лактозы | - | - | - | - | - | - | - | - | - | - | - | - | - |
| утилизация трегалозы | + | + | + | + | - | + | + | + | - | - | - | - | - |
| утилизация маннита | + | + | + | + | - | + | + | + | + | - | - | - | - |
| наличие фосфатазы | + | + | + | + | + | + | + | + | + | + | + | + | + |
| наличие нитратредуктазы | + | + | + | + | - | + | + | + | + | - | + | - | - |
| образование ацетилметилкарбинола | + | + | + | + | - | + | + | + | - | - | - | - | - |
| наличие аргининдегидролазы | - | - | - | - | - | - | - | - | - | - | + | - | - |
| утилизация ксилозы | + | - | - | - | - | - | - | - | - | - | + | - | - |
| утилизация сахарозы | + | + | + | + | - | + | + | + | - | - | - | - | - |
| утилизация арабинозы | + | + | -+ | - | - | + | + | + | + | -+ | + | + | - |
| утилизация галактозы | +- | - | -+ | - | - | + | - | - | + | -+ | + | + | - |
| утилизация салицина | + | + | + | - | - | + | + | + | - | - | - | + | - |
| наличие уреазы | -+ | - | + | - | - | - | + | + | - | - | + | - | + |
Примечания: «+» – реакция положительная, «–» – реакция отрицательная, «-+», «+-» – цвет не полностью соответствует стандарту.
Все исследованные штаммы микроорганизмов обладают фосфатазой, аргининдегидролаза обнаружена только у одного штамма (с), утилизируют маннозу все штаммы за исключением штамма с. Утилизирует ксилозу только штамм с. Утилизация лактоза не обнаружена ни у одного из исследованных штаммов.
По итогам проведения микроскопических исследований можно предположить, что большинство из исследованных культур микроорганизмов относится к р. Bacillus.
3.3 Определение активности микроорганизмов-деструкторов ПАВ
Определение способности штаммов подвергать деградации различные ПАВ осуществляли с помощью метода лунок (Турковская, 1997).
В ходе эксперимента установлено, что выделенные штаммы характеризуются большей активностью по отношению к НПАВ (оценка не менее 4). Менее интенсивный рост отмечался в экспериментах с АПАВ и КПАВ (оценки от 2 до 5). Несмотря на это, отмечаются штаммы, имеющие высокую активность (оценка 4,5) в каждом варианте эксперимента (1,4,15, а2, а1) (см. приложение 2).
Таблица 3. Оценка активности штаммов-деструкторов ПАВ методом лунок
|
№ штамма |
НПАВ |
АПАВ |
КПАВ |
|
Оценка |
|||
| 1 | 5 | 4 | 5 |
| 3 | 5 | 4 | 3 |
| 4 | 5 | 4 | 5 |
| 5 | 5 | 4 | 3 |
| 14 | 4 | 5 | 3 |
| 15 | 5 | 4 | 5 |
| 17 | 5 | 5 | 3 |
| 19 | 4 | - | - |
| а1 | 5 | 4 | 4 |
| а2 | 5 | 4 | 5 |
| b | 5 | 4 | 4 |
| с | 5 | 2 | 3 |
| хх | 5 | 4 | 3 |
Примечание: 5 баллов – очень хороший рост; 4 балла – хороший рост; 3 балла – рост средней интенсивности; 2 – слабый рост.
Микроорганизмы, характеризующиеся высокой активностью в присутствии ПАВ всех классов могут иметь большое значение в процессах очистки окружающей среды от загрязнения синтетическими моющими средствами.
3.4 Определение способности роста микроорганизмов на средах с добавлением различных ПАВ
Определение способности роста исследуемых штаммов микроорганизмов на питательном агаре (ПА) с добавлением СМС на основе АПАВ и КПАВ, а также с добавлением ПАА (НПАВ) производилось чашечным методом. Учет результатов производился через 2 суток. Результаты приведены в таблице 4.
Таблица 4. Результаты роста микроорганизмов на среде с различными ПАВ
|
№ штамма |
Наличие роста, КОЕ/мл |
||
|
КПАВ |
АПАВ |
НПАВ |
|
| 1 | - | + | + |
| 3 | - | + | + |
| 4 | - | + | + |
| 5 | + | + | + |
| 14 | - | + | + |
| 15 | - | + | + |
| 17 | - | + | + |
| 19 | - | + | + |
| хх | - | + | + |
| а1 | + | + | + |
| а2 | + | + | + |
| b | + | + | + |
| с | + | + | + |
В ходе эксперимента рост микроорганизмов отмечался на средах с добавлением АПАВ и НПАВ. На среде с добавлением КПАВ только 5 штаммов обнаружили рост.
Выводы
1. В ходе работы исследовано 13 культур микроорганизмов. Все культуры способны расти на средах с добавлением НПАВ и АПАВ. В эксперименте с использованием КПАВ обнаружен рост только 5‑ти культур (а1, а2, b, с, 5).
2. Наибольшей активностью исследуемые штаммы обладают по отношению к НПАВ.
3. Все исследуемые штаммы обладают фосфатазой, не утилизируют лактозу. Только штамм а2 обладает аргининдегидролазой. Большинство исследованных штаммов являются аэробными Г+ споровыми палочками. Это позволяет отнести их к роду Bacillus.
Литература
1. Абрамзон А.А. Поверхностно-активные вещества. Свойства и применение. – 2 изд. – Л., 1981. – 330 с.
2. Алексеева А.В. Коллоидная химия. – СПб: «Наука», 1998 – 290 с.
3. Аналитический обзор Комитета по природопользованию за 2005 год. / под ред. Голубева Д.В. и др. / – М.: «Сезам», 2006 – 25 с.
4. Вербина Н.М. Деградация микроорганизмами неприродных органических соединений в окружающей среде. – М.: Микробиология, 1978. – т. 7.
5. Глазовская М.А. Способность окружающей среды к самоочищению // Природа, 1979. – №3.
6. Градова Н.Б., Бабусенко Е.С. Лабораторный практикум по общей микробиологии. – М.: ДеЛи принт, 2001. – 232 с.
7. Елинов М.Н. Руководство к лабораторным занятиям по микробиологии. – М.: Медицина, 1998. – 190 с.
8. Королев В.А. Очистка грунтов от загрязнений. – М.: МАИК Наука // Интерпериодика, 2001. – 365 с.
9. Никитин Д.П., Новиков Ю.В. Окружающая среда и человек: Учеб. пособие для студентов вузов. – М.: Высш. школа, 1980. – 424 с.
10. Новиков Ю.В. Экология, окружающая среда и человек: Учеб. пособие для вузов, средних школ и колледжей. – М.: Фаир-пресс, 2002. – 560 с.
11. Поликарпов Н. Действие ПАГов на микро- и макроорганизмы. Аналитический обзор. 2005 г.
12. Ротмистров М.Н., Ставская С.С. Микробиология очистки воды. – К.: Наук. думка, 1978 г. – 268 с.
13. Рубан Е.Л. Физиология и биохимия представителей р. Pseudomonas. – М.: Наука, 1986 г. 352 с.
14. Савицкая М.Н., Холодова Ю.Д. Полиакриламид. – Киев: Техника, 1969. -188 с.
15. Ставская С.С. Биологическое разрушение АПАВ. – К.: Наук. думка, 1981 г. – 116 с.
16. Таубман А.Б., Маркина 3. H. Коллоидные поверхностно-активные вещества. / пер. с англ. / M. – 1966 г. – 199 с.
17. Теппер Е.З. и др. Практикум по микробиологии / Шильникова В.К., Переверзева Г.И. – М.: Агропромиздат, 2004. – 233 с.
18. Турковская О.В. Биологические и технологические аспекты микробной очистки сточных вод и природных объектов от поверхностно-активных веществ и нефтепродуктов: Авт. дис. д.б.н. – Саратов, 2000. – 360 с.
19. Успехи коллоидной химии / под ред. И.В. Петрянова-Соколова, К.С. Ахмедова. – Ташкент, 1987.
20. Хотько Н.И., Дмитриев А.П. Водный фактор в передаче инфекций. / Материалы странички ПАВ. – М. – 2006 г.
21. Яковлев С.В. и др. Охрана окружающей среды: Учебник / С.В. Яковлев и др. – М.: Изд-во АСВ, 1998. – 180 с.
22. ГОСТ 17.4.4.02–84. Охрана природы. Почва. Методы отбора и подготовки проб для химического, бактериологического и гельминтологического исследования. – М.:Изд-во стандартов, 1981. – 6 с.
23. www.aquaria.com.ua/coretra.html
24. www.ecocoop.ru
Приложение
Среда М9 (г/л):
Na2HPO3 – 6,0
KH2PO4 – 3,0
NaCl – 0,5
NH4Cl – 1,0
НПАВ – 0,2–1,0
рН – 7,0–7,2
Питательный агар (ПА) (г/л):
Панкреатический гидролизат рыбной муки – 24
Агар-агар 12–14
NaCl – 4
Дистиллированная вода – 1 л
рН среды 7,3 7,5
Способ приготовления
38,0 г порошка размешать в 1 л дистиллированной воды, кипятить 2 мин. До полного расплавления агара, фильтровать через ватно – марлевый фильтр, разлить в стерильные флаконы и стерилизовать при температуре 121 °С в течение 15 мин.
Среду охладить до температуры 45–50 °С, разлить в стерильные чашки Петри слоем 4–6 мм. После застывания среды чашки подсушить при температуре 37–38 °С в течение 40–60 мин (Теппер, 2004).
© 2010 Интернет База Рефератов