Рефераты по сексологии
Рефераты по информатике программированию
Рефераты по биологии
Рефераты по экономике
Рефераты по москвоведению
Рефераты по экологии
Краткое содержание произведений
Рефераты по физкультуре и спорту
Топики по английскому языку
Рефераты по математике
Рефераты по музыке
Остальные рефераты
Рефераты по авиации и космонавтике
Рефераты по административному праву
Рефераты по безопасности жизнедеятельности
Рефераты по арбитражному процессу
Рефераты по архитектуре
Рефераты по астрономии
Рефераты по банковскому делу
Рефераты по биржевому делу
Рефераты по ботанике и сельскому хозяйству
Рефераты по бухгалтерскому учету и аудиту
Рефераты по валютным отношениям
Рефераты по ветеринарии
Рефераты для военной кафедры
Рефераты по географии
Рефераты по геодезии
Рефераты по геологии
Рефераты по геополитике
Рефераты по государству и праву
Рефераты по гражданскому праву и процессу
Рефераты по делопроизводству
Рефераты по кредитованию
Рефераты по естествознанию
Рефераты по истории техники
Рефераты по журналистике
Рефераты по зоологии
Рефераты по инвестициям
Рефераты по информатике
Исторические личности
Рефераты по кибернетике
Рефераты по коммуникации и связи
Курсовая работа: Производство бета-каротина
Курсовая работа: Производство бета-каротина
Витамины (от лат. vita - жизнь), группа органических соединений разнообразной химической природы, необходимых для питания человека, животных и других организмов в ничтожных количествах по сравнению с основными питательными веществами (белками, жирами, углеводами и солями), но имеющих огромное значение для нормального обмена веществ и жизнедеятельности.
Первоисточником
В. служат главным образом растения. Человек и животные получают В.
непосредственно с растительной пищей или косвенно - через продукты животного
происхождения. Важная роль в образовании В. принадлежит также микроорганизмам.
Например, микрофлора, обитающая в пищеварительном тракте жвачных животных,
обеспечивает их витаминами группы В. Витамины поступают в организм животных и
человека с пищей, через стенку желудочно-кишечного тракта, и образуют
многочисленные производные (например, эфирные, амидные, нуклеотидные и др.),
которые, как правило, соединяются со специфическими белками и образуют многие
ферменты, принимающие участие в обмене веществ. Наряду с ассимиляцией в
организме непрерывно совершается диссимиляция В., причём продукты их распада (а
иногда и малоизменённые молекулы В.) выделяются наружу. Недостаточность
снабжения организма В. ведёт к его ослаблению, резкий недостаток В. - к
нарушению обмена веществ и заболеваниям - авитаминозам, которые могут
окончиться гибелью организма. Авитаминозы могут возникать не только от
недостаточного поступления В., но и от нарушения процессов их усвоения и использования
в организме.
Основоположник учения о В. русский врач Н. И. Лунин установил (1880), что при
кормлении белых мышей только искусственным молоком, состоящим из казеина, жира,
молочного сахара и солей, животные погибают. Следовательно, в натуральном
молоке содержатся и другие вещества, незаменимые для питания. В 1912 польский
врач К. Функ, предложивший само название "В.", обобщил накопленные к
тому времени экспериментальные и клинические данные и пришёл к выводу, что
такие заболевания, как цинга, рахит, пеллагра, бери-бери, - болезни пищевой
недостаточности, или авитаминозы. С этого времени наука о В. (витаминология)
начала интенсивно развиваться, что объясняется значением В. не только для
борьбы со многими заболеваниями, но и для познания сущности ряда жизненных
явлений. Метод обнаружения В., примененный Луниным (содержание животных на
специальной диете - вызывание экспериментальных авитаминозов), был положен в
основу исследований. Было выяснено, что не все животные нуждаются в полном
комплексе В., отдельные виды животных могут самостоятельно синтезировать те или
иные В. В то же время многие плесневые и дрожжевые грибы и различные бактерии
развиваются на искусственных питательных средах только при добавлении к этим
средам вытяжек из растительных или животных тканей, содержащих витамины. Таким образом,
витамины необходимы для всех живых организмов. Изучение В. не ограничивается
обнаружением их в естественных продуктах с помощью биологических тестов и
другими методами. Из этих продуктов получают активные препараты В., изучают их
строение и, наконец, получают синтетически. Исследована химическая природа всех
известных В. Оказалось, что многие из них встречаются группами по 3-5 и более
родственных соединений, различающихся деталями строения и степенью
физиологической активности. Было синтезировано большое число искусственных
аналогов В. с целью выяснения роли функциональных групп. Это способствовало
пониманию действия В. Так, некоторые производные В. с замещенными
функциональными группами оказывают на организм противоположное действие, по
сравнению с В., вступая с ними в конкурентные отношения за связь со
специфическими белками при образовании ферментов или с субстратами воздействия
последних.
В. имеют буквенные обозначения, химические названия или названия, характеризующие их по физиологическому действию. В 1956 принята единая классификация В., которая стала общеупотребительной.
Наличие химически чистых В. дало возможность подойти к выяснению их роли в обмене веществ организма. В. либо входят в состав ферментов, либо являются компонентами ферментативных реакций. При отсутствии В. в организме нарушается деятельность ферментных систем, в которых они участвуют, а следовательно, - и обмен веществ. Известно несколько сот ферментов, в состав которых входят В., и огромное количество катализируемых ими реакций. Многие В. - преимущественно участники процессов распада пищевых веществ и освобождения заключённой в них энергии (витамины B1, В2, PP и др.). Участвуют они и в процессах синтеза: B6 и В12 - в синтезе аминокислот и белковом обмене, В3 (пантотеновая кислота) - в синтезе жирных кислот и обмене жиров, Вс (фолиевая кислота) - в синтезе пуриновых и пиримидиновых оснований и многих физиологически важных соединений - ацетилхолина, глутатиона, стероидов и др. Менее изучено действие жирорастворимых В., однако несомненно их участие в построении структур организма, например в образовании костей (витамин D), развитии покровных тканей (витамин А), нормальном развитии эмбриона (витамин Е и др.). Таким образом, витамины имеют огромное физиологическое значение. Выяснение физиологической роли В. позволило использовать их для витаминизации продуктов питания, в лечебной практике и в животноводстве. Особенно широко стали применяться В. после освоения их промышленного синтеза.
Витаминная промышленность, вырабатывает синтетические витамины, коферменты в виде чистых кристаллических веществ и готовых к применению форм (драже, таблетки, ампулы, капсулы, гранулы, концентраты) и в небольших количествах витаминные препараты из растительного и животного сырья. Витамины повышают пищевую ценность продуктов питания, применяются в лечебной практике и для витаминизации кормов с целью повышения продуктивности животноводства.
Производство витаминов в нашей стране организовано в начале 30-х гг. Вначале выпускались витаминные препараты из натурального сырья. Затем было освоено производство синтетических витаминов С и K3. С 1949 по технологии, разработанной советскими учёными, в промышленном масштабе стал осваиваться синтез других витаминов, например тиамина (витамин B1). В 1950 производство витаминов в СССР увеличилось по сравнению с 1940 в 5,6 раза. К 1955 в СССР были разработаны схемы синтеза всех известных основных витаминов. Дальнейшее развитие витаминной промышленности связано главным образом с разработкой и внедрением синтетических методов производства витаминов. Эти методы по характеру технологических процессов значительно сложнее, чем метод извлечения витаминов из натурального сырья, но они позволяют получать продукцию в химически чистом виде, что имеет большое значение для их лечебного применения и точных дозировок при изготовлении кормовых концентратов. Кроме того, издержки на производство синтетических витаминов ниже издержек на получение соответствующих витаминов из натурального сырья. За 1959-65 в промышленном масштабе освоен синтез всех известных витаминов и витаминных препаратов, введены в строй крупные витаминные предприятия: Белгородский витаминный и Болоховский (Тульская область) химические комбинаты, а также значительно увеличены мощности ранее действовавших предприятий. В 1965 объём производства витаминной продукции в СССР увеличился по сравнению с 1958 в 2,8 раза, а в 1970 по сравнению с 1965 в 2,6 раза. В 1970 выпуск синтетических витаминов и их готовых форм составил более 99% всего объёма производства витаминной продукции.
К специфическим особенностям синтеза витаминов относятся: многостадийность процессов; значительная материалоёмкость, обусловливающая необходимость размещения предприятий В. п. вблизи сырьевых баз; применение специальной аппаратуры, предназначенной для работы с агрессивными средами; необходимость выработки высокочистой продукции. Витаминные заводы - специализированные предприятия. Преобладает предметная специализация - осуществление синтеза витаминов на каждом предприятии по полной схеме их производства, включая и выпуск всех полупродуктов. С конца 60-х гг. расширяется более эффективная - технологическая специализация производства полупродуктов.
Научно-технические проблемы получения витаминов и их применения разрабатываются в СССР в основном во Всесоюзном научно-исследовательском витаминном институте, а также в научно-исследовательских организациях АМН СССР, АН СССР и АН союзных республик, министерств и ведомств. Вопросы совершенствования действующих производств решаются центральными заводскими лабораториями.
Главные направления развития витаминной промышленности в России:
- создание новых высокоэффективных препаратов;
- совершенствование технологии производства и разработка новых, улучшенных схем синтеза, основанных на использовании дешёвых видов отечественного сырья;
- увеличение выработки витаминов, коферментов и их готовых форм до уровня, обеспечивающего полное удовлетворение потребностей народного хозяйства, расширение ассортимента продукции;
- строительство новых и реконструкция действующих производств;
- механизация и автоматизация технологических процессов;
- совершенствование и организация производства отдельных полупродуктов на предприятиях других отраслей промышленности;
- повышение качества продукции;
- углубление технологической специализации;
- внедрение автоматизированных систем управления отраслью промышленности и производством.
В наиболее развитых странах, особенно в США, Японии, Великобритании, Германии, Франции, Швейцарии, производство витаминов достигло больших размеров.
Как правило, оно сосредоточено в руках химико-фармацевтических фирм.
Производство витаминов из дрожжей
В настоящее время чистые препараты витаминов получают главным образом синтетически, в некоторых случаях отдельные стадии их образования выполняются методами микробиологического синтеза. Распространенное ранее производство концентратов витаминов из продуктов растительного или животного происхождения сейчас почти полностью потеряло свое значение.
В то же время, некоторые витамины получают с помощью экстракции и очистки культуральной жидкости или биомассы микроорганизмов. Наряду с использованием непосредственно дрожжевой биомассы как источника витаминов в виде дрожжевых гидролизатов и пивных дрожжей, некоторые дрожжи используются для микробиологического производства чистых витаминов.
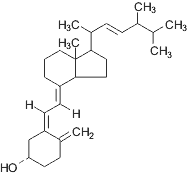
|
|
| Витамин D2, кальциферол |
Использование дрожжей для производства чистых витаминов началось в 1930-х годах с получения витамина D. С использованием специальных рас Saccharomyces cerevisiae получают эргостерол, который после облучения ультрафиолетом модифицируется в витамин D2 (кальциферол).
Существуют штаммы сахаромицетов, обладающие способностью к гиперсинтезу витамина B2 (рибофлавина), которые могут быть использованы для получения этого витамина.
Из базидиомицетовых дрожжей, обладающих способностью к интенсивному синтезу каротиноидов, получают препараты β-каротина, являющегося предшественником витамина A, и астаксантина.
Питьевые дрожжи
Дрожжевой осадок, остающийся после сбраживания пивного сусла, издавна используют для получения различных полезных веществ, в частности дрожжевых гидролизатов и автолизатов. Гидролизаты дрожжей получают, нагревая дрожжевую биомассу при 100°C в кислой среде. Большая часть белков при этом гидролизуется до аминокислот. Затем препарат нейтрализуют и концентрируют в виде густой пасты или высушивают. При получении дрожжевых автолизатов разрушение клеточных компонентов происходит под действием ферментов самой дрожжевой клетки. Этот процесс протекает в обычных условиях в или при небольшом нагревании дрожжевого осадка без питательных веществ до 50°C и обычно продолжается в течение 1-2 сут. За это время около половины всех белков в дрожжевых клетках расщепляется до аминокислот.
Дрожжевые гидролизаты широко применяются в качестве источника витаминов и аминокислот в медицине, в микробиологии при составлении питательных сред. Дрожжевые гидролизаты и автолизаты обладают способностью придавать пищевым продуктам привкус мяса, или усиливать такой вкус, поэтому они широко используются в пищевой промышленности для приготовления различных приправ, в качестве вкусовых добавок в готовые продукты (например, в картофельные чипсы).
Большой популярностью пользуются пивные (питьевые) дрожжи, приготовляемые на основе частично гидролизованной дрожжевой биомассы. Они используются в качестве источника витаминов (в первую очередь В1 и В2, а также РР, В3, В4, В6, Н), незаменимых аминокислот и жирных кислот и широко применяются в медицине, ветеринарии, косметологии, диетологии.
Красные дрожжи
Многие дрожжи синтезируют большое количество каротиноидов, придающих их колониям красную, розовую, оранжевую или желтую окраску. Способность к образованию каротиноидов и формирование окрашенных колоний встречается только среди базидиомицетовых дрожжей, то есть относится к признакам аффинитета. Наиболее характерно образование каротиноидов для родов Rhodosporidium, Cystofilobasidium, Sporidiobolus, и их анаморф Rhodotorula, Cryptococcus, Sporobolomyces. К наиболее распространенным каротиноидам относится β-каротин.
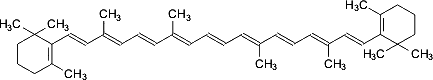
β-Каротин
Это широко распространенное соединение, встречающиеся также во многих растениях и грибах. β-Каротин является предшественником витамина A и его промышленное получение представляет интерес для медицины и некоторых других облестей. Разработаны и применяются биотехнологические процессы получения β-каротина с использованием красных дрожжей, например Rhodotorula glutinis.
У базидиомицетовых дрожжей встречаются и другие виды каротиноидов. Например, красные дрожжи Phaffia rhodozyma образуют каротиноид астаксантин.
Астаксантин
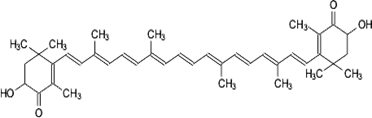
Астаксантин - широко распространенный в природе каротиноидный пигмент ярко-красной окраски. В отличие от β-каротина имеет два дополнительных атома кислорода на каждом из колец. Впервые был выделен из омаров в 1938 году, сейчас обнаружен в тканях многих растений и животных. Особенно в большом количестве содержится в тканях креветок, крабов, лососевых рыб, придавая им красный цвет.
Астаксантин является одним из наиболее активных антиоксидантов и используется в медицине для лечения ряда заболеваний. Препараты астаксантина широко используются в качестве кормовой добавки в рыбоводстве, особенно при выращивании лососей, и аквариумоводстве.
Основным источником для получения астаксантина служит водоросль Haematococcus инцистированные клетки которой содержат до 4% каротиноида. Астаксантин был обнаружен также в дрожжах Phaffia rhodozyma (телеоморфа Xanthophyllomyces dendrorhous). Генетически модифицированные штаммы Phaffia содержат до 1-2% астаксантина и могут также использоваться для промышленного получения этого каротиноида.
Клетки овальные или круглые, иногда удлиненные. Почкование истинное, многостороннее. Может формироваться примитивный псевдомицелий, но истинного мицелия не образуют. Диплоидизация происходит в результате слияния двух гаплоидных клеток (гологамия). Вегетативно размножаются в основном диплоидные клетки. Аски образуются преимущественно из вегетативных диплоидных клеток. Аски круглые или овальные, при созревании спор не вскрываются. Аскоспоры круглые или слабоовальные, бесцветные, гладкие, 1-4 в аске. Все виды активно сбраживают сахара. Дрожжи этого рода с давних времен распространены в кустарном виноделии и широко используются в разных отраслях бродильной промышленности, в связи с чем они более всех других дрожжей изучены в разных аспектах. Их систематика, однако, многократно пересматривалась. Центральный вид - Saccharomyces cerevisiae известен в десятках синонимов, которые в настоящее время рассматриваются как производственные расы, но не самостоятельные виды.
Потребность дрожжей в витаминах
Одна из характеристик, используемых для таксономического описания дрожжей - потребность в витаминах. Более 80% всех известных видов дрожжей не способны к росту на среде, не содержащей витамины (ауксотрофны). Наибольшее число видов (около 65%) нуждается в биотине и тиамине. Из других витаминов в таксономии дрожжей используется определение потребности в рибофлавине, пантотеновой кислоте, пиридоксине, инозите и никотиновой кислоте.
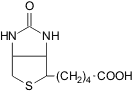
|
Биотин, витамин H (B7) |
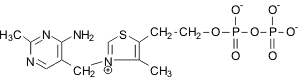
Тиаминпирофосфат, витамин B1 |
|
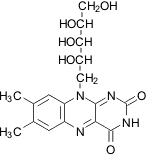
Рибофлавин, витамин B2 |
Пантотеновая кислота, витамин B5 |
|
|
мио-Инозит, витамин B8 |
Никотиновая кислота, Ниацин, витамин PP |
Для определения потребности исследуемого штамма в том или ином витамине его выращивают на стандартной среде, содержащей определенный витамин, и сравнивают с ростом на этой же среде, не содержащей витаминов. В случае, если добавление витамина приводит к существенному увеличению роста, делают вывод о ауксотрофности штамма по этому витамину. Тесты на способность к росту на безвитаминной среде и определение потребности в конкретных витаминах входят в стандартное описание вида дрожжей.
Зависимость скорости роста ауксотрофных штаммов дрожжей от содержания определенных витаминов была использована для разработки методов определения концентрации витаминов в различных средах по измерению прироста дрожжевой биомассы.
Стандартные среды для физиологических тестов
Разделение дрожжей на виды базируется на многих характеристиках, среди которых важное место занимают как морфологические, так и физиологические признаки - способность к росту на различных органических соединениях в качестве единственного источника углерода и энергии, способность к усвоению различных источниках азота, потребность в различных витаминах и т.п. Все эти характеристики сильно зависят от состава среды и условий культивирования, поэтому в систематике дрожжей разработаны и применяются среды стандартного состава. Полный набор таких сред выпускается в готовом виде фирмой Difco (Difco Laboratories, в 1997 г. вошедшая в состав BD Diagnostic Systems). Среди этих сред наиболее популярны: морфологический агар - для описания макро- и микроморфологических характеристик дрожжевой культуры, азотная основа - для определения способностей к росту на различных источниках углерода, углеродная основа - для определения способности к усвоению различных источников азота, базвитаминная среда - для определения потребностей в витаминах.
Состав этих сред приведен в таблице:
| Ингредиенты (на 1 л воды) | Морфологи-ческий агар | Азотная основа | Углеродная основа | Среда без витаминов |
| Источники углерода и азота, г | ||||
| Глюкоза | 10 | — | 10 | 10 |
| (NH4)2SO4 | 3.5 | 5 | — | 5 |
| Аспарагин | 1.5 | — | — | — |
| Макроэлементы, г | ||||
| КH2РO4 | 0.85 | 0.85 | 0.85 | 0.85 |
| К2НРО4 | 0.15 | 0.15 | 0.15 | 0.15 |
| MgSO4 | 0.5 | 0.5 | 0.5 | 0.5 |
| NaCl | 0.1 | 0.1 | 0.1 | 0.1 |
| СаСl2 | 0.1 | 0.1 | 0.1 | 0.1 |
| Аминокислоты, мг | ||||
| L-Гистидин НСl | 10 | 10 | 1 | 10 |
| DL-Метионин | 20 | 20 | 2 | 20 |
| DL-Триптофан | 30 | 20 | 2 | 20 |
| Витамины. мкг | ||||
| Пантотенат кальция | 2000 | 2000 | 2000 | — |
| Фолиевая кислота | 2 | 2 | 2 | — |
| Инозит | 10000 | 10000 | 10000 | — |
| Никотиновая кислота | 400 | 400 | 400 | — |
| Парааминобензойная кислота | 200 | 200 | 200 | — |
| Пиридоксин НСl | 400 | 400 | 400 | — |
| Рибофлавин | 200 | 200 | 200 | — |
| Тиамин НСl | 400 | 400 | 400 | — |
| Биотин | 20 | 20 | 20 | — |
| Микроэлементы, мкг | ||||
| Н3РО3 | 500 | 500 | 500 | 500 |
| CuSO4 | 40 | 40 | 40 | 40 |
| KJ | 100 | 100 | 100 | 100 |
| FeCl3 | 200 | 200 | 200 | 200 |
| MnSO4 | 400 | 400 | 400 | 400 |
| Na2MoO4 | 200 | 200 | 200 | 200 |
| ZnSO4 | 400 | 400 | 400 | 400 |
| Промытый агар, г | 18 | — | — | — |
| Количество сухой готовой среды фирмы «Difco» на 1 л, г | 35 | 6.7 | 11.7 | 16.7 |
ПРОИЗВОДСТВО КРИСТАЛЛИЧЕСКОГО β-КАРОТИНА ИЗ
МОРКОВИ
Исходным сырьем для получения кристаллического β-каротина является морковь, содержащая среди каротиноидов 85—90% β-каротина. Наоборот, в тыкве содержание β-каротина составляет лишь 60—70%. Производство кристаллического каротина включает следующие стадии: 1) экстракция каротина из сухого коагулята белков органическим растворителем; 2) омыление концентрата; 3) экстракция каротина из омыленной массы и 4) кристаллизация каротина.
Экстракция каротина. Большинство исследователей сходятся на применении в качестве органического растворителя для экстракции р-каротина хлорированных углеводородов (в основном дихлорэтан). Существует мнение о целесообразности предварительной экстракции белкового коагулята спиртом для удаления стеринов, фосфатидов, свободных жирных кислот и других веществ. Однако дополнительная экстракция спиртом сильно осложнит технологию производства, поэтому необходимость этого процесса нуждается в технико-экономическом обосновании. Экстракцию осуществляют дихлорэтаном в экстракторах непрерывного действия (при крупном производстве) или в аппаратах типа Сокслета при небольших масштабах производства. Дихлорэтана в реактор загружают 400% к массе сухого коагулята. Экстракцию ведут в течение 1—1,5 ч. Содержание каротина в шроте не должно превышать 5% к введенному каротину с белковым коагулятом. Затем в испарителе 2 в присутствии СО2 отгоняют дихлорэтан (температура не должна быть выше 50° С).
Омыление концентрата. Омыление производят 10%-ным раствором едкого кали, которого добавляют около 10% к массе концентрата. Процесс проводят в реакторе 3 с обратным холодильником в течение 20 мин при 50° С. При омылении образуется осадок, содержащий до 80% каротина и жидкое мыло. Осадок отфильтровывают на нутч-фильтре 4 и промывают спиртом от мыла и красящих веществ.
Б. Савинов и А. Свищук указывают на образование нерасслаивающихся эмульсий при омылении липоидных экстрактов в хлорированных углеводородах. Это явление ими было успешно устранено совмещением стадии омыления со стадией экстракции.
Экстракция каротина из омыленной массы. Каротин экстрагируют дихлорэтаном в количестве, необходимом для растворения каротина при комнатной температуре, исходя из того, что в 100 мл дихлорэтана (ДХЭ) растворяется при температуре 25° С 1,16 г каротина.
Экстракцию ведут при комнатной температуре в реакционном аппарате 5, снабженном обратным холодильником и мешалкой. Затем массу фильтруют на нутч-фильтре 6, промывают осадок чистым ДХЭ. Экстракт с промывным ДХЭ сгущают в вакуум-перегонном аппарате 7 до получения пересыщенного раствора.
Первая кристаллизация. Пересыщенный раствор спускают в кристаллизатор 8, где в течение 8 ч идет процесс кристаллизации вначале при комнатной температуре, а затем через 4 ч при охлаждении, к концу процесса температуру доводят до 5° С.
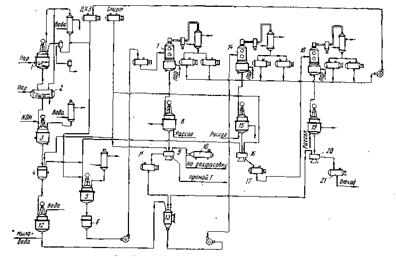
Для увеличения выхода каротина на первой кристаллизации в пересыщенный раствор вводят этиловый спирт в отношении 1:2. Затем отфуговывают в центрифуге 9 выделившиеся кристаллы, промывают их спиртом и высушивают в вакуум-сушилке 10. Маточный раствор I поступает в сборник 11.
Вторая кристаллизация. Маточный раствор 1 перерабатывают совместно с промывными и мыльной массой. Для этого мыльную массу экстрагируют два раза ДХЭ в нутч-фильтре 4, а экстракт промывают водой в смесителе 12. Экстракт и маточник I направляют в сборник 13, откуда они поступают в вакуум-аппарат 14 для упаривания в концентрат П. Последний поступает в кристаллизатор 15, где кристаллизуется 24 ч. Фуговку производят при температуре 5° С в центрифуге 16. Кристаллы каротина II промывают спиртом и направляют на переработку совместно с экстрактом омыленной массы (до первой кристаллизации). Маточный раствор II поступает в сборник 17.
Третья кристаллизация. Маточный раствор II совместно с промывными второй кристаллизации упаривают в вакуум-аппарате 18, кристаллизуют 72 ч в кристаллизаторе 19, фугуют в центрифуге 20. Кристаллы промывают спиртом. Получают кристаллы каротина III, направляемые на переработку в маточный раствор I и в виде отхода маточный раствор II — в сборник
Нормы качества готовой продукции. Кристаллический каротин должен быть однородным, мелкокристаллическим сухим порошком без слежав19, фугуют в центрифуге 20. Кристаллы промывают спиртом. Получают кристаллы каротина III, направляемые на переработку в маточный раствор I и в виде отхода маточный раствор II — в сборник
Нормы качества готовой продукции. Кристаллический каротин должен быть однородным, мелкокристаллическим сухим порошком без слежав шихся комков лилово-красноватого цвета с металлическим блеском. Точка плавления каротина должна быть не ниже 160° С. Содержание β-каротина в кристаллах не менее 90%.
Вопросы усовершенствования технологии производства каротина из моркови. Интересные исследования в этой области были проведены Б. Савиновым и его учениками. Исходя из факта локализации каротина на хромопластах, им было предложено заменить процесс прессования мезги моркови процессом вымывания пластид из клеток интенсивным перемешиванием мезги с водой в суспензионном экстракторе. Им же был разработан метод получения масляных концентратов каротина из влажного белкового коагулята путем применения центробежного смесителя. Разработан метод получения каротина из моркови и тыквы методом термической коагуляции белков в клетке, изучены вопросы экстракции каротина в многочленной батарее. К сожалению, эти методы не нашли широкого применения в связи с развитием химического синтеза витаминов.
ХИМИЧЕСКИЙ СИНТЕЗ β–КАРОТИНА
Метилгептенон (6-метилгептен-5-он-2). Получают его конденсацией диметилвинилкарбинола и ацетоуксусного эфира при температуре 160—165° С по следующей химической схеме:
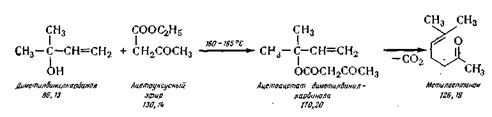
В реактор 29 из нержавеющей стали, снабженный колонкой с дефлегматором и конденсатором, из мерника загружают вазелиновое масло (высококипящий разбавитель) и при температуре 210° С (в масле) загружают диметилвинилкарбинол и ацетоуксусный эфир так, чтобы температура реакционной массы была не ниже 160—165° С. Затем нагревание продолжают при температуре 160—180° С 3 ч до прекращения выделения газа (СО2). В сборник после конденсатора собирают отгон (спирт с примесью ацетона). Кубовый остаток разгоняют при остаточном давлении 5—6 мм рт. ст. в вакуум-перегонном аппарате 30. Готовый продукт поступает в приемник. Выход 60%.
Метилгептенон — бесцветная жидкость, температура кипения 52—53°С при остаточном давлении 5 мм рт. ст. C8H14О, молекулярная масса 126,19; п2о = 1,4404; d20=0,8616, хорошо перегоняется с водяным паром; Хтах = 243 нм (в спирте), lgs =2,54.
Дегидролиналоол (3,7-диметилоктаен-6-ин-1-ол-3). Дегидролиналоол синтезируют по следующей химической реакции:
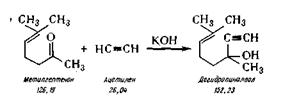
В реактор из эмалированной стали 31, снабженный мешалкой, барботером для подвода ацетилена загружают толуол из мерника 32 и порошкообразное едкое кали, нагревают до 80° С и из баллона 33 пропускают ацетилен при перемешивании в течение 2 ч. После прекращения нагревания уменьшают ток ацетилена, охлаждают рассолом до —12—10° С и постепенно в течение 3 ч приливают метилгептенон из мерника 34. Затем добавляют воды и после перемешивания разделяют слои в делительной воронке 35. Толуольный раствор переводят в реактор 36, в котором нейтрализуют углекислотой. В перегонном аппарате 37 отгоняют толуол, а затем при остаточном давлении 12—14 мм рт. ст. собирают фракцию, кипящую при температуре 89—91С. Выход 76—80%.
Дегидроналоол — бесцветная жидкость, температура кипения 78—80°С при остаточном давлении 8 мм рт. ст.; Cl0H12O, молекулярная масса 152,23; плотность ==1,4632. Хорошо растворим в органических растворителях, плохо — в воде.
Псевдоионон. Псевдоионон получают из дегидролиналоола путем аци-лирования его, изомеризации ацетата, омыления его и конденсации с аце тоном в присутствии едкого натра. Синтез протекает по следующей схеме
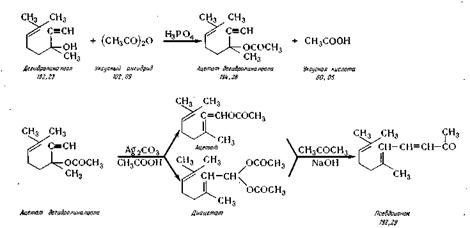
В реактор из нержавеющей стали 38 загружают из мерника 39 дегидролиналоол, из мерника 40уксусный ангидрид и из мерника 41 каталитическое количество фосфорной кислоты, перемешивают (температура не выше 50° С) и выдерживают 14—15 ч при температуре 18° С. Затем вводят в реактор из баллона 42 азот, нагревают реакционную массу до 90° С и добавляют каталитическое количество карбоната серебра, продолжая перемешивание 1,5 ч при температуре 90° С. Далее реакционную массу охлаждают до 20° С и передают под давлением в реактор 43, в который из мерника 44 загружают 20%-ный водный раствор хлористого натрия. После перемешивания разделяют слои в делительной воронке 45. В ней же промывают верхний слой раствором хлористого натрия до нейтральной реакции. Затем верхний слой переводят в реактор 46 и вводят в него из мерника 47 ацетон и из мерника 48,8%-ный водный раствор едкого натра, нагревают до 40° С и перемешивают 2,5—3 ч. Реакционную массу при температуре 20° С нейтрализуют уксусной кислотой из мерника 49. В делительной воронке 50 разделяют слои: нижний слой поступает в сборник 51, откуда далее направляют на регенерацию. Верхний слой промывают в колонке 52 раствором хлористого натрия. Промытый слой (технический псевдоионон) передают в сборник 53 и далее в вакуум-перегонный аппарат 54, снабженный колонкой, дефлегматором и конденсатором. Перегонку ведут при остаточном давлении 6—7 мм рт. ст., отбирают фракцию, кипящую при 131—135°С в сборник 55. Выход 54—55%.
Псевдоионон — желтоватая маслянистая жидкость, хорошо растворима в органических растворителях, плохо — в воде, температура кипения при остаточном давлении 5 мм рт. ст.— 120° С; С13Н10О, молекулярная масса 192,29; n2D°=l,5300, df = 0,8954; Xmax = 291 нм, Е= 1205; содержание не ниже 95%.
СИНТЕЗ β-ИОНОНА
β-Ионон получают процессом циклизации псевдоионона под влиянием смеси концентрированной серной кислоты и ледяной уксусной кислоты в среде толуола по химической схеме:
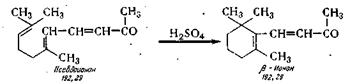
В реактор 1 из сборника 2 загружают псевдоионон и из сборника 3 толуол и перемешиванием получают толуольный раствор псевдоионона (плотность 890—900 кг/м3), подаваемый насосом 4 в мерник 5. В реактор из эмалированной стали 6 сливают концентрированную серную кислоту из мерника 7, которую в реакторе 6 охлаждают до 0°, а затем медленно загружают из мерника 8 ледяную уксусную так, чтобы температура не поднималась выше 15° С. Смесь кислот насосом 8 подают в мерник 9. В аппарат для циклизации 10 из нержавеющей стали, снабженный мешалкой и рубашкой, подают из мерника 9 смесь кислот, а из мерника 5 толуольный раствор псевдоионона. Реакция протекает при температуре минус 7—10° С в течение 1 ч. Для нейтрализации реакционной массы применяют 18—20%-ный раствор углекислого натрия. В реактор // загружают углекислый натрий, из мерника 12 воду и при перемешивании насыщенный раствор насосом 13 подают в мерник 14. Из аппарата циклизации 10 нейтрализованная реакционная масса поступает в делительную воронку 15, где промывается раствором карбоната натрия и далее поступает в сборник 16 и в перегонный аппарат 17. В нем отгоняют толуол в сборники 18 и 19 при остаточном давлении 20 мм рт. ст. Остаток перегоняют при остаточном давлении 1 мм рт. ст. в перегонном аппарате 20 и собирают в приемнике. Выход 75%.
β-Ионон — желтоватая маслянистая жидкость, температура кипения 118—120°С при остаточном давлении 5 мм рт. ст. и 132° С при остаточном давлении 12 мм рт. ст., С13Н2оО, молекулярная масса 192,29; по =1,5210; хорошо растворим в органических растворителях, плохо в воде; Xmах= 296 нм, E=557.
СИНТЕЗ АЛЬДЕГИДА С14 [4(2',6',6'-ТРИМЕТИЛЦИКЛОГЕКСЕН-
Г-ИЛ)-2-МЕТИЛБУТЕН-З-АЛЬ-1]
Синтез альдегида С14 осуществляют по реакции Дарзана путем конденсации (3-ионона с метиловым или этиловым эфиром монохлоруксусной кислоты в присутствии метилата натрия. Реакции протекают по следующей схеме:
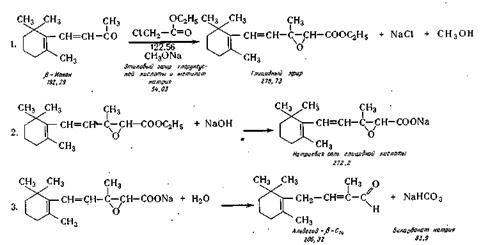
Реакция конденсации. В реактор 21, снабженный охлаждающей рубашкой и мешалкой, загружают (3-ионон из сборника 22 и в течение 2—3 ч при ливают из мерника 23 этиловый эфир хлоруксусной кислоты, а из сборника 24 сухой метилат натрия. Температуру при этом поддерживают минус 5—7° С. В результате реакции конденсации получается глицидный эфир, который из раствора не выделяют.
Омыление. Глицидный эфир омыляют раствором едкого натра в водном метаноле, который добавляют из смесителя 25 в тот же реактор в течение 1,5—2 ч при температуре 18—20°С. В результате омыления получают натриевую соль глицидного эфира.
Декарбоксилирование. В реактор 21 добавляют воду и дихлорэтан, перемешивают, а затем направляют реакционную массу в делительную воронку 26. Нижний дихлорэтановый слой отделяют в воронке и в смесителе 27 промывают водным раствором поваренной соли, приготовленном в смесителе 28. Нижний слой спускают в смеситель 29, затем добавляют в этот смеситель сульфат натрия и перемешивают. Сухой экстракт переводят в вакуум-перегонный аппарат 30, отгоняют дихлорэтан, а затем под глубоким вакуумом (0,1 мм рт. ст. при температуре около 100° С) отгоняют альдегид С14. При необходимости альдегид подвергают ректификации при остаточном давлении 0,3—0,5 мм рт. ст.
Альдегид С14 — светло-желтая маслянистая жидкость с температурой кипения 103—106° С при остаточном давлении 0,2 мм рт. ст., хорошо растворим в органических растворителях, плохо—в воде. При хранении неустойчив. Формула С14Н220, молекулярная масса 206,14.
ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПРОИЗВОДСТВА СИНТЕТИЧЕСКОГО
р-КАРОТИНА
Технология производства базируется на однокомпонентном методе синтеза, разработанном Ингоффеном и усовершенствованном Излером с их соавторами. Этот метод нашел свое дальнейшее развитие в исследованиях Н. Преображенского, Г. Самохвалова и Л. Вакуловой. Метод заключается в конденсации двух молекул альдегида С19 с молекулой ацетилена по реакции Гриньяра. Технология включает следующие стадии синтеза: синтез (3-С16-альдегида из β-С14-альдегида; синтез β-С)9-альдегида из (3-С16-альдегида; синтез 15,15-дегидро-(3-каротина изС19-альдегида и ацетилена; синтез транс-β-каротипа из 15,15-дегидро-β-каротина.
СИНТЕЗ β-С14-АЛЬДЕГИДА-[9-МЕТИЛ-6-(1,1,5-
ТРИМЕТИЛЦИКЛОГЕКСЕН-5 ИЛ)-ГЕКСАДИЕН-8, 10-АЛЬ-12]
Химические реакции получения альдегида С16 заключаются в ацеталировании альдегида-С14, конденсации полученного ацеталя с виниловым эфиром в присутствии хлористого цинка и омыления алкоксиацеталя альдегида С16. Химизм реакций синтеза альдегида С16 основан на склонности виниловых эфиров присоединяться к ацеталям а, (3-непредельных карбонильных соединений, причем одна алкоксигруппа [OR] перемещается от ацеталя к двойной связи винилового эфира. Остаток ацеталя присоединяется к β-углеродному атому винилового эфира. Конденсация и перегруппировка протекает по схеме:
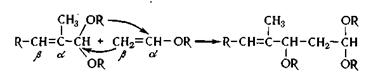
По этой схеме протекает следующий синтез.
Схема реакций синтеза С16-альдегида.
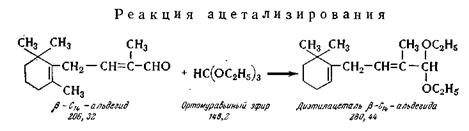
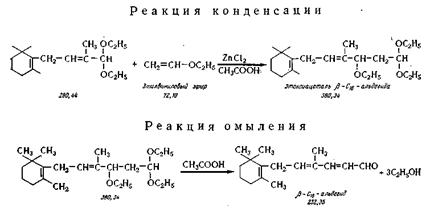
Для успешного протекания реакций ацетализирования и конденсации важно, чтобы влажность реагентов была минимальной (в %): абсолютного спирта — 0,15; этилвинилового эфира — 0,2; ортомуравьиного эфира — 0,09; альдегида-С14 0,04. Хлористый цинк предварительно должен быть сплавлен и высушен в вакуум-эксикаторе над концентрированной серной кислотой.
Ацетализирование. В реактор 1 из нержавеющей стали, снабженный мешалкой, обратным холодильником и барботером для азота, загружают через мерник 2 альдегид-С14, из мерника 3 ортомуравьиный эфир (температура кипения 144—145° С, плотность 897 кг/м3), из мерника 4 — раствор паратолуолсульфокислоты в абсолютном этаноле. Реакцию ведут в присутствии азота, вводимого в реактор из баллона 5. Перемешивают в течение 20—24 ч при комнатной температуре. Затем в реакционную массу вводят из мерника 6 лигроин и нейтрализуют 2,5%-ным раствором бикарбоната натрия, загружаемым из мерника 7. После этого отделяют органический слой в делительной воронке 8 и после просушки поташом направляют в сборник 9, а из него в перегонный аппарат 10, где при температуре около 50°С и остаточном давлении 3—5 мм рт. ст. отгоняют растворитель. Технический продукт содержит около 95% ацеталя. Выход ацеталя из (3-С14-альдегида составляет около 75 %. На выход ацеталя из альдегида-С 16 значительно влияет чистота альдегида-С14. Диэтилацеталь β-С14-альдегида С18Н3202 представляет собой маслянистую жидкость желтого цвета с температурой кипения 87—96°С при остаточном давлении 0,2 мм рт. ст.; df =0,9279; n™ =1,4773.
Конденсация с этилвиниловым эфиром. В реактор 11, снабженный холодильником, загружают из мерника 12 диэтилацеталь-β-С14-альдегида, затем из мерника 13 медленно добавляют при температуре 35 —40°С этилвиниловый эфир (температура кипения 35°С, остаточная влажность не выше 0,2%), а из мерника 14 — 10%-ный раствор сплавленного хлористого цинка в ледяной уксусной кислоте. Реакцию проводят в присутствии азота, вводимого из баллона 15, при температуре 35—40°С в течение 1 ч. В результате реакции образуется этоксиацеталь β-С 16-альдегида (см. химическую схему), представляющий собой (перегонка при остаточном давлении 0,02 мм рт. ст.) вязкое светло-желтое масло, d0 = 0,9315. Выход 66—70%.
Омыление этоксиацеталя. В процессе омыления ацетальной группы происходит также отщепление молекулы спирта. В реактор 11 из мерника 16 добавляют смесь ледяной уксусной кислоты, ацетата натрия, воды и гидрохинона (небольшое количество). Реакционную массу медленно нагревают до 90—95° С и перемешивают 3 ч. Затем раствор (темно-вишневого цвета) переводят в реактор-охладитель 17. Охлаждают до 0°, выкристаллизовывают технический β-С 1б-альдегид и отфуговывают его в центрифуге 18.
Перекристаллизация технического альдегида С1б. Процессы ведут в этаноле в реакторе 19 по двухступенчатой схеме. После обработки активированным углем раствор фильтруют через нутч-фильтр 20. Кристаллизуют в кристаллизаторе 21, отфуговывают кристаллы в центрифуге 22. Маточный раствор I поступает в сборник 23. Сгущение его производят в вакуум-аппарате 24 и далее кристаллизуют в кристаллизаторе 25. Кристаллы второй кристаллизации отфуговывают в центрифуге 26, а маточный раствор II направляют в сборник 27. Он является отходом производства. Кристаллы второй кристаллизации поступают на перекристаллизацию в реактор 19 совместно с техническим продуктом.
Альдегид-β-С16 (С1бН240) представляет собой светло-желтые кристаллы с температурой плавления 77—78° С, хорошо растворим в органических растворителях, плохо в воде; Хгаах—276—280 нм (в спирте).
СИНТЕЗ β-С19-АЛЬДЕГИДА [9,13-ДИМЕТИЛ-7-(1,1,5-
ТРИМЕТИЛЦИКЛОГЕК-СЕН-5-ИЛ)-ОКТАТРИЕН-8,10,12- АЛЬ-14]
Химические реакции получения альдегида-С19 заключаются в ацетали-зировании альдегида С16, конденсации полученного ацеталя с виниловым эфиром в присутствии хлористого цинка и омыления алкоксиацеталя альдегида С19 по следующей химической схеме.
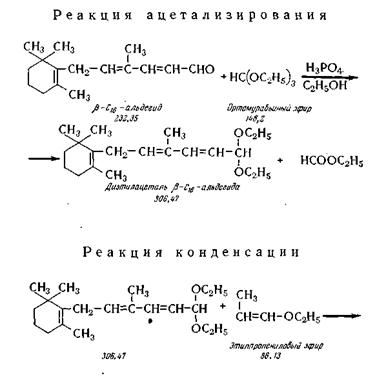
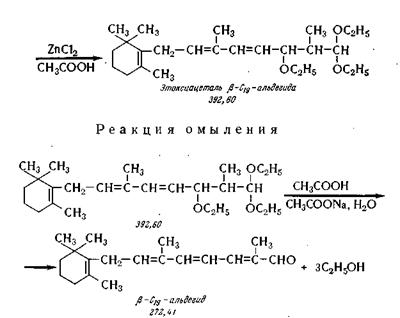
Для успешного протекания указанных реакций необходимы те же условия обезвоживания химических реагентов, как и в синтезе β-С16-альдегида.
Ацетализирование. Процессы проводят так же, как и для синтеза β -С16-альдегида и в аналогичной аппаратуре. К ней относятся реактор 28 и сборники: для альдегида-С16 29, ортомуравьиного эфира 3, катализатора 4, лигроина 6, нейтрализующего раствора бикарбоната натрия 7. Азот в реактор подается из баллона 30. Разделение слоев осуществляют в делительной воронке 31 и после просушки органического слоя поташом направляют его в сборник 32 и далее в перегонный аппарат 33, где отгоняют растворитель и не вошедший в реактор ортомуравьиный эфир (при температуре 50—55° С и остаточном давлении 2—3 мм рт. ст.). Получают технический диэтилацеталь (3-С,6-альдегида с содержанием основного вещества 95—97%, n° = 1,5026—1,5070; маслянистая жидкость, температура кипения около 145° С при остаточном давлении 0,05 мм рт. ст. Выход 75—80% (в пересчете на альдегид – С16).
Конденсация с этилпропениловым эфиром. Процесс осуществляют в реакторе 34, в который загружают диэтилацеталь альдегида-С16 из мерника 35, а из мерника 14 раствор (10%) сплавленного хлористого цинка в ледяной уксусной кислоте. Масса принимает темно-вишневый цвет. Затем при температуре 25—30°С из мерника 36 медленно добавляют этилпропени-ловый эфир (температура кипения 69—71° С, остаточная влага не выше 0,15%). Масса постепенно окрашивается в желтый цвет. Реакция протекает в' присутствии азота, вводимого из баллона 37, при перемешивании.
Омыление этоксиацеталя. В реактор 34 из мерника 16 добавляют смесь ледяной уксусной кислоты, ацетата натрия, воды и гидрохинона. Реакционную массу медленно нагревают до 90—95°С и перемешивают 3 ч. Затем раствор темно-вишневого цвета направляют в реактор-охладитель 38, охлаждают до минус 5—7° С и кристаллизуют. Кристаллы технического продукта отфуговывают в центрифуге 39. Получают желтые кристаллы с содержанием основного вещества около 95%. Маточный раствор направляют в сборник 40; он является отходом.
Перекристаллизация технического альдегида С19. Процессы ведут в этаноле по схеме перекристаллизации альдегида С16 в следующей аппаратуре:
для первого продукта — реактор-растворитель 41, нутч-фильтр 42, кристаллизатор 43, центрифуга 44. для маточного раствора I — сборник 45;
для второго продукта — вакуум-аппарат 46, кристаллизатор 47, центрифуга 48, сборник маточного раствора II-—отхода производства — 49.
Выход альдегида на диэтилацеталь составляет 55—57% (от теоретического). Альдегид β-С19 представляет собой ярко-желтые ромбические кристаллы с температурой плавления 63—65°С; хорошо растворим в органических растворителях, плохо — в воде; Хтах=325 нм (в спирте).
СИНТЕЗ 15, 15'-ДЕГИДРО-β-КАРОТИНА
Вещество получают конденсацией альдегида С19 с ацетиленовым комплексом Иоцича с последующей дегидратацией образующегося диола С40. Реакцию конденсации начинают с приготовления реактива Гриньяра, который с ацетиленом в среде сухого эфира дает комплекс Иоцича по схеме:
![]()
Ацетилен пропускают при температуре 18—20° С до полного исчезновения магний бромэтила, что контролируется реакцией с кетоном Михлера (наличие вызывает изумрудно-зеленое окрашивание). Дегидратацию диола С4о осуществляют в среде сухого серного эфира спиртовым раствором хлористого водорода в присутствии азота. Реакции протекают по следующей схема:
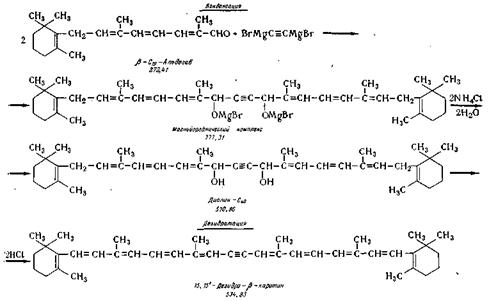
Конденсация. В стальной эмалированный реактор 50, снабженный мешалкой и обратным холодильником, предварительно тщательно высушенный, загружают через люк магниевую стружку из сборника 51, сухой серный эфир (влажность не выше 0,1 %) из мерника 52 и медленно из мерника 53 приливают в течение 1 ч раствор сухого бромистого этила в сухом эфире. Затем в течение 1 ч нагревают реакционную массу до кипения и перемешивают до полного растворения магния. Затем охлаждают массу до 15—18° С и в течение 5—6 ч пропускают из баллона 54 предварительно осушенный через вымораживатель 55 ацетилен до получения отрицательной пробы с жетоном Михлера. Затем реакционную массу охлаждают до 10—12и С и из мерника 56 медленно добавляют раствор альдегида-С19 в сухом эфире так, чтобы температура не превышала 12—13° С. Раствор окрашивается в ярко-оранжевый цвет. Реакция при перемешивании протекает в присутствии азота в течение 1,5—2 ч с повышением в конце процесса температуры до 20—25° С. Полноту реакции конденсации определяют по исчезновению альдегида-С19 (реактив Легаля). После этого реакционную массу сливают в реактор-охладитель 57 с ледяной водой, куда из мерника 58 залит хлористый аммоний. Массу сливают в делительную воронку 59. Органический слой промывают водой, просушивают сульфатом натрия из сборника 60 и направляют через сборник 61 в вакуум-аппарат 62. Растворитель удаляют в вакууме в токе азота при температуре не выше 30° С и получают β-С4о-диолин в виде твердого желтого осадка.
Дегидратация. Процесс осуществляют при помощи хлористого водорода. Для этого из мерника 63 сливают в вакуум-аппарат 62 хлористый метилен, растворяют диолин-С4о и переводят раствор в реактор 64, снабженный мешалкой и рассольным охлаждением. Массу охлаждают до минус 15—18°С, а затем из мерника 65 постепенно добавляют 8%-ный раствор сухого НС1 в абсолютном спирте с таким расчетом, чтобы температура реакционной массы не превышала к концу процесса +3, +5° С. Затем в делительной воронке 66 отделяют органический слой, промывают его насыщенным раствором бикарбоната из мерника 67 и направляют в сборник 68 и далее в вакуум-аппарат 69, где под вакуумом в токе азота при температуре 30—35°С отгоняют хлористый метилен. Кристаллизующуюся массу направляют в кристаллизатор 70, где при температуре - 2, - 3°С в течение 8—10 ч в присутствии азота выпадают кристаллы 15,15'-дегидро-β-каротина. Последние отфуговывают в центрифуге 71, промывают этиловым спиртом. Выход около 50%. Маточный раствор поступает в сборник 72 и является отходом производства. Вопрос о выделении вещества из маточного раствора еще недостаточно изучен. 15,15'-дегидро-β-каротин представляет собой кристаллы красного цвета с металлическим блеском; температура плавления 153—154°С; хорошо растворим в органических неполярных растворителях, плохо — в воде; Хтах = 454 и 430 нм; Е =1568 и 1873. Выход 48—50%.
СИНТЕЗ ТРАНС-β-КАРОТИНА
Синтез осуществляют путем гидрогенизации 15,15'-дегидро-β-каротина в растворе толуола на частично отравленном палладиевом катализаторе с целью превращения ацетиленовой связи до этиленовой и получения 15,15'-цис-β-каротина. Изомеризация в среде петролейного эфира превращает последний в транс-β-каротин. Для успешного проведения реакции гидрирования необходимо применять тщательно очищенный толуол с применением палладиевого катализатора на меле. Реакции протекают по следующей схеме:
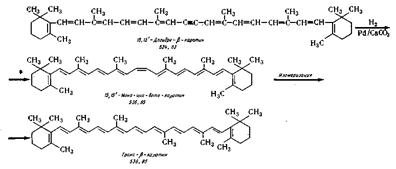
15,15'-моно-цис-β-каротин. В реактор 73 из эмалированной стали загружают через люк 15,15'-дегидро-β-каротин, а из мерника 74 толуол и при нагревании до 35—40°С и перемешивании растворяют кристаллы. Затем добавляют палладиевый катализатор, нанесенный на мел. Аппарат дважды продувают азотом из баллона 75, а затем водородом из баллона 76, после чего при температуре 20°С и избыточном давлении до 0,5 кгс/смг при перемешивании осуществляют процесс гидрогенизации. Реакцию контролируют по количеству поглощенного водорода. Далее реакционную массу фильтруют через нутч-фильтр 77 и сборник 78, откуда фильтрат направляют в перегонный аппарат 79 для отгонки толуола при вакууме (остаточное давление 8—10 мм рт. ст.) в токе азота. Кубовый остаток сливают в кристаллизатор 80, где при минус 5—8° С выкристаллизовывают 15,15'-моно-цис-β-каротин. Кристаллы выделяют при помощи центрифуги 81; маточный раствор поступает в сборник 82 и является отходом производства. Катализатор с нутч-фильтра 77 направляют на регенерацию. Выход цис-Р-каротина составляет 90—95% [70], темно-вишневые кристаллы; температура плавления 148—150°С; Хмах=338 (цис-пяк), 450, 480 нм (в гексане).
Транс-β-Каротин. В эмалированный реактор 83, снабженный мешалкой и обратным холодильником, загружают цис-β-каротин, из мерника 84 петролейный эфир (80—90° С), нагревают массу до кипения и продолжают перемешивать в течение 10—12 ч (изомеризация). Затем сливают в кристаллизатор 85, охлаждают до 0 — минус 2°С и кристаллизуют в течение 6 ч. Кристаллы выделяют в центрифуге 86, а маточный раствор I направляют в сборник 87 и после сгущения в вакуум-аппарате 88, кристаллизации в кристаллизаторе 89, выделения кристаллов в центрифуге 90 получают дополнительное количество кристаллов транс-β-каротина II, которые поступают для перекристаллизации в кристаллизатор 85. Маточный раствор II является отходом производства.
Перекристаллизация технического транс-β-каротина. Перекристаллизацию ведут из петролейного эфира по двухступенчатой схеме: для первой ступени реактор-растворитель 91, нутч-фильтр 92, кристаллизатор 93, центрифуга 94, сборник маточного раствора I 95; для второй ступени — вакуум-аппарат 96, кристаллизатор 97, центрифуга 98, сборник маточного раствора II 99. .Кристаллы β-каротина II поступают на перекристаллизацию совместно с техническим β-каротином в реактор-растворитель 91.
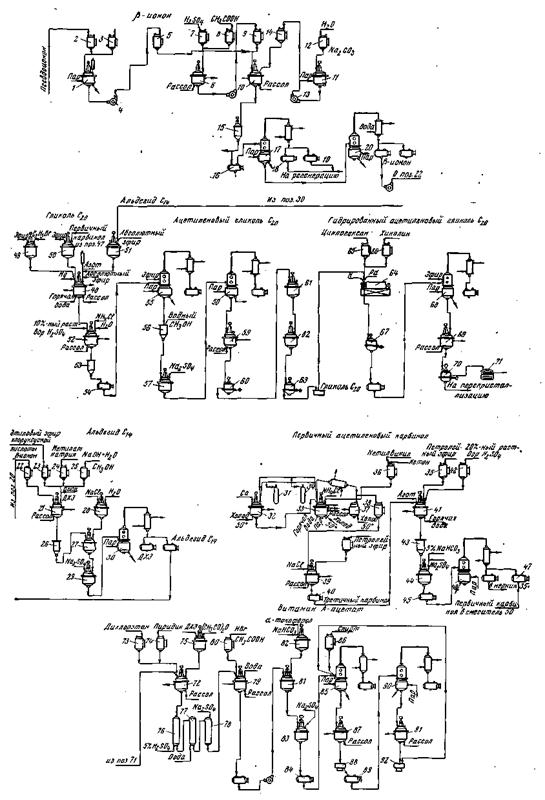
Схема синтеза каротина (объяснения в тексте).
Лекарственные формы витаминов.
Индивидуальные
потребности в витаминах отличаются и по этой причине производители выпускают
витамины в разной форме. Таблетки - общепринятая, привычная и удобная для
применения форда выпуска. Таблетки можно дольше хранить, чем порошки или
жидкости.
Капсулы также удобны для хранения и являются общепринятыми формами выпуска
жирорастворимых витаминов A, D и Е.
Порошки - поскольку в них отсутствуют наполнители, связующие и другие не имеющие отношение к витаминам вещества, могут быть предпочтительной формой применения при наличии у кого-то аллергических реакций. И кроме того, порошки могут "вмещать" большие дозировки витаминов. Одна чайная ложка порошка витамина С может содержать до 4.000 мг витамина.
Жидкости - хороши тем, что легко смешиваются с напитками и удобны для тех, кто не может глотать капсулы и таблетки.
Вдыхание витаминов через нос - обеспечивает весьма быстрое усвоение витаминов С и группы В. Пластыри и имплантанты, содержащие витамины, удобны тем, что могут обеспечить продолжительное и дозированное применение, и в скором времени, возможно, будут более широко применяться.
Сухая или водорастворимая форма?
Жирорастворимые витамины A, D, Е и К могут быть произведены в «сухом», то есть в водорастворимом виде. Такие формы выпуска этих витаминов рекомендуются тем, кто страдает расстройством желудка после приема масел или имеет некоторые кожные расстройства, проявляющиеся, например, в виде сьшей или прыщей. Указанные формы выпуска показаны и тем, кто соблюдает диету с исключением из рациона большинства жиров. Поскольку для нормальной ассимиляции, то есть усвоения, жирорастворимым витаминам нужен жир, я советую вам использовать "сухую" форму витаминов A, D, Е, К обязательно в том случае, если вы находитесь на диете с низким содержанием жира. Синтетическое или натуральное, неорганическое или органическое?
Приобретение и прием синтетических витаминов не сказывается на вашем бюджете, но может неблагоприятно отозваться на вашем желудке, в то время как натуральные витамины, принимаемые даже в больших дозировках, ничего подобного не вызывают. Химическая структура витаминов в том и другом случае может выглядеть одинаково, но не одним лишь этим обусловлена эффективность натуральных витаминов, но и тем, что связано с этими веществами в природе. Синтетический витамин С - это лишь аскорбиновая кислота и ничего больше. Натуральный же витамин С, получаемый из плодов шиповника, содержит еще и биофлавоноиды, то есть целый комплекс витамина С, что делает его намного более эффективным.
Натуральный витамин Е, который может включать в себя не только альфа-токоферол, но и другие токоферолы, оказывается более эффективным, чем его синтетический аналог. Вот что говорит по этому поводу известный аллерголог доктор Герон П. Рандольф: «Синтетически полученное вещество может вызвать реакцию у людей, чувствительных к химическим соединениям, в то время как то же вещество натурального происхождения переносится хорошо, хотя химическая структура этих двух веществ идентична». Тот, кто принимал и те, и другие витамины, мог на собственном примере убедиться в том, что после приема натуральных веществ наблюдалось меньше желудочно-кишечных расстройств. Что особенно важно: в отличие от синтетических препаратов натуральные витамины не вызывают токсических реакций, даже когда они принимаются в дозах, превышающих рекомендуемые.
Разница между неорганическим и органическим - это не то же самое, что разница между синтетическим и натуральным, хотя нередко кое-кто так и думает. Все витамины являются органическими веществами и, как полагается таковым, содержат углерод. Минеральные же вещества являются неорганическими. Они не содержат углерод, но существуют органические соединения железа-глюконат, пептонат и цитрат железа. А вот сульфат железа, например, является его неорганическим соединением.
Что такое хелатирование?
Хелатирование - это процесс, при помощи которого минеральные вещества превращаются в хорошо усвояемую форму. Такие минеральные добавки, как костная мука и доломит, прежде чем могут быть усвоены организмом, должны подвергнуться процессу хелатирования в желудочно-кишечном тракте. Нередко бывает так, что естественный процесс хелатирования в организме нарушается и поэтому большая часть принятых внутрь минеральных веществ не усваивается. Если помнить еще и о том, что организм не полностью использует все поступающие питательные вещества, тогда важность приема хелатированных минералов станет очевидной. Как правило, организмом усваивается только от 2 до 10 процентов поступающего с пищей неорганического железа и к тому же половина оставшегося позже также выводится. Усвояемость хелатированных минеральных веществ в три-десять раз больше, чем нехелатированных, поэтому это оправдывает некоторое увеличение их цены.
Пролонгированные формы.
Шагом вперед в производстве витаминов была разработка добавок в пролонгированной (time release) форме. Пролонгирование - это процесс, при помощи которого витамины заключаются в микрокапсулы, затем связываются в специальной основе, что обеспечивает их постепенное непрерывное выделение, всасывание и усвоение в течение 8-12 часов. Большинство витаминов - водорастворимые - и поэтому не могут накапливаться в организме. Если они используются не в пролонгированной форме, то быстро всасываются, попадают в кровоток и независимо от дозы в течение 2-3 часов выделяются с мочой. Добавки в пролонгированной форме могут обеспечить оптимальную эффективность витаминов, уменьшить их потерю с мочой и поддерживать стабильные уровни витаминов в крови круглосуточно.
© 2010 Интернет База Рефератов
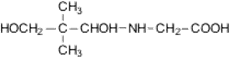
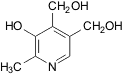 Пиридоксин,
витамин B6
Пиридоксин,
витамин B6