
Рефераты по сексологии
Рефераты по информатике программированию
Рефераты по биологии
Рефераты по экономике
Рефераты по москвоведению
Рефераты по экологии
Краткое содержание произведений
Рефераты по физкультуре и спорту
Топики по английскому языку
Рефераты по математике
Рефераты по музыке
Остальные рефераты
Рефераты по авиации и космонавтике
Рефераты по административному праву
Рефераты по безопасности жизнедеятельности
Рефераты по арбитражному процессу
Рефераты по архитектуре
Рефераты по астрономии
Рефераты по банковскому делу
Рефераты по биржевому делу
Рефераты по ботанике и сельскому хозяйству
Рефераты по бухгалтерскому учету и аудиту
Рефераты по валютным отношениям
Рефераты по ветеринарии
Рефераты для военной кафедры
Рефераты по географии
Рефераты по геодезии
Рефераты по геологии
Рефераты по геополитике
Рефераты по государству и праву
Рефераты по гражданскому праву и процессу
Рефераты по делопроизводству
Рефераты по кредитованию
Рефераты по естествознанию
Рефераты по истории техники
Рефераты по журналистике
Рефераты по зоологии
Рефераты по инвестициям
Рефераты по информатике
Исторические личности
Рефераты по кибернетике
Рефераты по коммуникации и связи
Курсовая работа: Жиры. Аналитическая характеристика жиров
Курсовая работа: Жиры. Аналитическая характеристика жиров
Федеральное агентство по образованию ГОУ ВПО
Тульский государственный педагогический университет
им. Л.Н. Толстого
кафедра органической и биологической химии
Курсовая работа
на тему:
Жиры. Аналитическая характеристика жиров
Выполнила:
студентка 3 курса группы В
естественнонаучного факультета
Алиева Джейран Октаевна
Научный руководитель:
ст. пр.
Бойкова Ольга Ивановна
Тула, 2007
Содержание
Введение
1.Простые липиды. Жиры
1.1 Кислоты жиров
1.2 Строение глицеридов
1.3 Физические свойства жиров
1.4 Химические свойства жиров
1.5 Аналитическая характеристика жиров
2. Сложные липиды
2.1 Фосфолипиды
2.1.1 Глицерофосфолипиды
2.2 Сфинголипиды
2.3 Гликолипиды
2.4 Стероиды
3. Липиды и строение биологических мембран
4. Применение жиров
Вывод
Литература
Приложение 1
Приложение 2
Введение
В настоящее время заметно возрос интерес к липидам со стороны всех направлений медико-биологической науки. Прежде всего - это связано с теми функциями, которые липиды выполняют в организме растений, животных и человека. Исследования трёх последних десятилетий показали, что липиды не только источник и форма хранения информации. Сложные липиды и их природные комплексы являются основой строения биологических мембран и в составе ее осуществляют важнейшие жизненные процессы. Установлено также, что серьезные поражения нервной системы, расстройства сердечно-сосудистой системы тесно связаны с нарушением обмена липидов
К липидам относятся жиры и жироподобные вещества растительного и животного происхождения. Обычно их разделяют на две группы: простые липиды - жиры и сложные липиды, к которым относятся фосфатиды, цереброзиды и фосфосфингозиды. В биохимии к липидам часто относят и свободные длинноцепочечные кислоты жиров, стерины, воски и некоторые другие, растворимые в неполярных растворителях органические соединения.
Окислительное расщепление запасных жиров – универсальный биохимический процесс, протекающий во всех живых организмах и поставляющий энергию, необходимую для жизнедеятельности. Такие запасные жиры или жиры депо наряду с белками и сахарами – один из трех основных питательных компонентов для млекопитающих.
В последние годы выявлена крайне важная роль сложных липидов в функционировании клеточных мембран. Все клеточные мембраны, помимо белка и полисахаридов, содержат от 20 до 75% полярных и нейтральных липидов (фосфолипиды, сфинголипиды, гликосфингозиды, холестерин и жирные кислоты). Липиды образуют бимолекулярный слой толщиной около 5 нм с полярными группами по обе стороны слоя, в которой вкраплены белковые субчастицы и структурированная вода. Этот слой регулирует обмен веществ в клетках, определяя проницаемость мембран для ионов, неэлектролитов и воды.
1. Простые липиды жиры
Природные животные и растительные жиры (растительные жиры называются обычно маслами) состоят главным образом из глицеридов (сложные эфиры глицерина и различных органических кислот, в основном С10 – С18). Жиры содержат две или три главные кислоты и некоторые другие кислоты в меньшем количестве. Так как спирт во всех природных жирах один и тот же – глицерин, наблюдаемые между жирами различия обусловлены исключительно органическими кислотами. Запасные жиры или жиры депо – один из метаболических резервов живых систем.[1]
1.1 Кислоты жиров
Кислоты, содержащиеся в природных жирах, являются монокарбоновыми с нормальной цепью и четным числом атомов углерода. Исключение составляют изовалериановая кислота и ряд циклических кислот, содержащихся в некоторых весьма редко встречающихся жирах.
В природе жирные кислоты в свободном виде встречаются редко. Однако, образуя эфирные или амидные связи, они входят в состав различных классов липидов, перечисленных выше, а также многих промежуточных продуктов метаболизма липидов. Целесообразно рассмотреть некоторые свойства жирных кислот, которые во многих отношениях сходны с другими амфифильными липидами. Биологически важные жирные кислоты характеризуются следующим:
1) являются, как правило, монокарбоновыми кислотами, содержащими одну ионизируемую карбоксильную группу и неполярную ациклическую неразветвленную углеводородную пень;
2) обычно содержат четное число атомов углерода, хотя в природе встречаются также и жирные кислоты с нечетным числом углеродных атомов;
3) представляют собой либо насыщенные соединения, либо соединения с одной пли несколькими двойными связями.
Для разделения смесей кислот, выделенных из жиров гидролизом, применяют разнообразные методы, например, кристаллизацию при низкой температуре, образование комплексов с мочевиной и с циклическими декстринами, противоточную экстракцию и хроматографию в различных формах, но главным образом хроматографию на бумаге и газожидкостную хроматографию. Последний метод наиболее перспективен.[2]
Из всех непредельных кислот, содержащихся а природных жирах, наиболее распространена олеиновая кислота. В очень многих жирах олеиновая кислота составляет больше половины от общей массы кислот, и лишь в немногих жирах ее содержится меньше 10%; олеиновая кислота присутствует во всех исследованных жирах. Две другие непредельные кислоты линолевая и линоленовая – также очень широко распространены, хотя они присутствуют в значительно меньшем количестве, чем олеиновая кислота. В заметных количествах линолевая и линоленовая кислоты содержатся в растительных маслах; для животных организмов они являются незаменимыми кислотами. В природе непредельные кислоты встречаются только в цис-форме.[1]
1.1.1 Насыщенные жирные кислоты
Общепринятые названия и формулы некоторых насыщенных жирных кислот приведены в таблице 1. При нумерации углеродных атомов первым считается углерод карбоксильной группы (С-1) , тогда как остальные атомы нумеруется по порядку так, что последним является углерод концевой метильной группы. Температуры кипения и плавления жирных кислот возрастают с увеличением длины углеводородной цепи. Насыщенные жирные кислоты с четным числом углеродных атомов являются при комнатной температуре жидкостями, если общее число углеродных атомов меньше 10, или твердыми, если углеродная цепь более длинная.
Жирные кислоты являются слабыми кислотами и диссоциируют в водных растворах. Значения констант диссоциации для всех насыщенных жирных кислот очень близки между собой (рК=4,28), а также соответствующей константе уксусной кислоты (рК=4,76). Исключение составляет первый член этого ряда — муравьиная кислота (pК=3,75). Таким образом, в водных растворах неионизированная форма жирной кислоты (RCOOH) является преобладающей при рН<рК, тогда как ионизированная форма (RCOO~) преобладает при рН>р/К.
Смесь жирных кислот, получаемая при гидролизе липидов из различных природных источников, обычно содержит как насыщенные, так ненасыщенные жирные кислоты. В типичных липидах животного происхождения преобладающей насыщенной жирной кислотой является пальмитиновая (С16), второе место занимает стеариновая кислота (С18). Более короткие жирные кислоты (С14 и С12), так же как и более длинные (до С28), встречаются лишь в небольших количествах. Жирные кислоты, содержащие 10 или меньше углеродных атомов, вообще редко встречаются в животных липидах.
Таблица 1.
| Кислота | Число атомов углерода в цепи | Формула |
Предельные (жирные) кислоты |
||
|
Капроновая Каприловая Каприновая Лауроновая Миристиновая Пальмитиновая Стеариновая Арахиновая |
С6 С8 С10 С12 С14 С16 С18 С20 |
СН3(СН2)4СООН СН3(СН2)6СООН СН3(СН2)8СООН СН3(СН2)10СООН СН3(СН2)12СООН СН3(СН2)14СООН СН3(СН2)16СООН СН3(СН2)18СООН |
Непредельные кислоты |
||
|
Олеиновая Ленолевая Линоленовая Элеостеариновая Эруковая |
С18 С18 С18 С18 С22 |
СН3(СН2)7СН=СН(СН2)7СООН СН3(СН2)4СН=СНСН2СН=СН(СН2)7СООН СН3СН2СН=СНСН2СН=СНСН2СН=СН(СН2)7СООН СН3(СН2)3СН=СНСН=СНСН=СН(СН2)7СООН СН3(СН2)7СН=СН(СН2)11СООН |
1.1.2 Ненасыщенные жирные кислоты
В названиях этих соединений по женевской номенклатуре число углеродных атомов в молекуле указывается таким же способом, что и для соответствующих насыщенных кислот (с помощью греческих числительных), а число двойных связей — с помощью суффиксов («ен» — одна, «диен»— две, «триен» — три связи и т. д.). Положение двойной связи обозначается номером ближайшего к карбоксильной группе атома углерода, участвующего в образовании этой связи. Так, например, двойная связь в цис-9-гексадсценовой кислоте находится между девятым и десятым углеродными атомами, а двойные связи в цис-9,12-октадекадиеновон кислоте расположены между 9—10 и 12—13 атомами углерода.
Ненасыщенность жирных кислот цис-ряда существенно влияет на их свойства. Так, с увеличением числа двойных связей значительно снижается температура плавления жирных кислот, возрастает их растворимость в неполярных растворителях (табл. 3.3). Все обычные ненасыщенные жирные кислоты, встречающиеся в Природе, при комнатной температуре жидкости.
Одиночная двойная связь в жирных кислотах животного происхождения обычно находится в 9,10-положении. Двумя преобладающими мононенасыщенными жирными кислотами животных липидов являются олеиновая и пальмитоолеиновая.
СН3- (СН2)7-СН=СН - (СН2)7-СООН СН3-(СН2)5-СН=СН - (СН2)7 -СООН
олеиновая кислота пальмитоолеиновая кислота
Олеиновая кислота является более широко распространенной природе и превалирует в количественном отношении.
Наличие двойной связи создает возможность образования цыстрансизомеров. Известны изомерные формы 9-октадецеиоиой кислоты
Как правило, природные жирные кислоты с одной двойной связью принадлежат к цис-серии. Однако для других классов соединений это правило не всегда применимо. Известно немало кислот, содержащих более одной двойной связи. Две двойные связи, расположенные в углеродном скелете следующим образом:
![]()
называются сопряженными (конъюгированными). Конъюгированные двойные связи обнаружены в жирных кислотах растительного происхождения (элеостеариновая кислота, табл. 3.2), в то время как двойные связи в ненасыщенных жирных кислотах животных липидов обычно входят в дивинилметановую группировку
-СН=СН-СН2-СН=СН—
Наиболее часто встречающимися полиненасыщенными кислотами тканей млекопитающих являются линолевая кислота, содержащая две двойные связи:
СН3(СН2)4 СН=СН-СН2—СН=СН— (СН2)7-СООН
линолевая кислота
Линоленовая кислота и её эфиры легко подвергаются окислению, что и определяет физические свойства высыхающих масел, например льняного масла применяемого в производстве красок.
Важную группу ненасыщенных жирных кислот составляют простагландины, образующиеся в ходе метаболизма преимущественно из арахидоновой кислоты. Поскольку простагландины обладают высокой физиологической активностью, - некоторых полиненасыщенных жирных кислот.[2]
1.2 Строение глицеридов
Глицериды имеют следующую общую формулу:
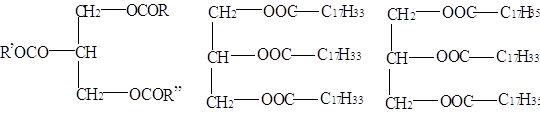
где R, R’, R” – углеводородные радикалы.
Три гидроксила глицерина могут быть этерифицированы либо только одной кислотой, например, пальмитиновой или олеиновой, либо двумя или тремя различными кислотами.
Как уже отмечалось выше, большинство жиров содержит две или три главные кислоты и некоторые другие кислоты в меньшем количестве. Все кислоты распределены таким образом, что образуется по возможности большее число смешанных глицеридов («принцип равномерного распределения»). Иными словами, каждая молекула глицерида стремится к наиболее гетерогенному составу. Так, например, масло какао, содержащее в качестве основных кислот пальмитиновую, стеариновую и олеиновую примерно в равном молярном соотношении, состоит в большей степени (55%) из ольпальмитостеарина, тогда как трипальмитин, тристеарин и триолеин содержатся в незначительных количествах. Оливковое масло, несмотря на то, что оно содержит высокий процент олеиновой кислоты (80% от общего количества кислот), содержит всего 30% триолеина наряду с 45% диолеинов с предельной кислотой (пальмитиновой и стеариновой) и 25% линолеодиолеинов.
Различное распределение кислот в глицеридах объясняет некоторые различия в физических свойствах жиров. Так, масло какао и овечий жир содержат в качестве главных кислот пальмитиновую, стеариновую и олеиновую примерно в равных количествах, и все же они обладают разными свойствами. Масло какао плавится при низкой температуре (34 0С), и оно рассыпчато, в то время как овечий жир, плавящийся при более высокой температуре (44-49 0С), жирный на ощупь и густой. Первое ведет себя как индивидуальное вещество, а второй как сложная смесь.
Выделение чистых глицеридов – сложная операция, требующая применения специальной техники, например дробной кристаллизации при низких температурах.
Впервые глицериды синтетически были получены Бертло (2854) нагреванием до 200 0С смеси глицерина с жирными кислотами в присутствии минеральных кислот. Если в этом синтезе применять смесь кислот, то получается сложная смесь смешанных глицеридов. Позднее глицериды получил Вюрц (1859), нагревая 1,2,3-трибромпропан с серебряными солями жирных кислот:
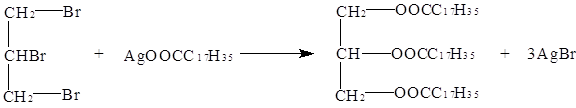
Глицериды, содержащие два различных концевых кислотных остатка, обладают асимметрическим атомом углерода и, следовательно, могут быть оптически деятельными.
1.3 Физические свойства жиров
Как правило, жиры не выдерживают перегонки и разлагаются, даже если
их перегоняют при пониженном давлении.
Температура плавления, а соответственно и консистенция жиров зависят от строения кислот, входящих в их состав. Твердые жиры, т.е. жиры, плавящиеся при сравнительно высокой температуре, состоят преимущественно из глицеридов предельных кислот (стеариновая, пальмитиновая), а в маслах, плавящихся при более низкой температуре и представляющих собой густые жидкости, содержатся значительные количества глицеридов непредельных жирных кислот (олеиновая, линолевая, линоленовая).
Для многих глицеридов характерно наличие «двойной температуры плавления». Так, чистый тристеарин плавится при 71 0С. Однако если тристеарин расплавить, а затем резко охладить, то при повторном нагревании он плавится сначала при 55 0С, затем затвердевает и снова плавится при 71 0С. Удалось установить также существование и третьей точки плавления. Это явление обусловлено наличием для стеарина трех полиморфных кристаллических форм с различной температурой плавления: устойчивая β-форма (71,5 0С); β’-форма (65 0С) и α-форма (54,5 0С).
Так как природные жиры представляют собой сложные смеси смешанных глицеридов, они плавятся не при определенной температуре, а в определенном температурном интервале, причем предварительно они размягчаются. Для характеристики жиров применяется, как правило, температура затвердевания, которая не совпадает с температурой плавления – она несколько ниже. Некоторые природные жиры – твердые вещества; другие же – жидкости (масла). Температура затвердевания изменяется в широких пределах: -27 0С у льняного масла, -18 0С у подсолнечного, 19-24 0С у коровьего и 30-38 0С у говяжьего сала.
Температура затвердевания жира обусловлена характером составляющих его кислот: она тем выше, чем больше содержание предельных кислот.
Жиры растворяются в эфире, полигалогенопроизводных, в сероуглероде, в ароматических углеводородах (бензоле, толуоле) и в бензине. Твердые жиры трудно растворимы в петролейном эфире; нерастворимы в холодном спирте. Жиры нерастворимы в воде, однако они могут образовывать эмульсии, которые стабилизируются в присутствии таких поверхностно-активных веществ (эмульгаторов), как белки, мыла и некоторые сульфокислоты, главным образом в слабощелочной среде. Природной эмульсий жира, стабилизированной белками, является молоко.[1,3]
1.4 Химические свойства жиров
Гидролиз. Среди реакций жиров особое значение имеет гидролиз, который
можно осуществить как кислотами, так и основаниями (щелочной гидролиз называют омылением):
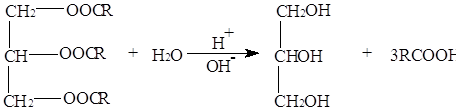
Гидролиз жиров идет постепенно; например, при гидролизе тристеарина
получается сначала дистеарин, затем моностеарин и, наконец, глицерин и стеариновая кислота.
Практически гидролиз жиров производят или перегретым паром, или же нагреванием в присутствии серной кислоты или щелочей. Превосходными катализаторами гидролиза жиров являются сульфокислоты, получаемые сульфированием смеси непредельных жирных кислот с ароматическими углеводородами (контакт Петрова). В семенах клещевины находится особый фермент – липаза, ускоряющий гидролиз жиров. Липаза широко применяется в технике для каталитического гидролиза жиров.
Реакции присоединения. Двойные связи непредельных кислот, входящих в состав жира, могут быть прогидрированы каталитическим путем, они присоединяют бром и йод.
В связи с тем, что твердых жиров не хватает для технического использования и пищевых целей, большое техническое значение приобрело превращение более дешевых жидких жиров в твердые. Это превращение осуществляется путем каталитического гидрирования двойных связей кислот жидких жиров, при этом жидкие ненасыщенные жиры переходят в твердые насыщенные, поэтому процесс называют также отверждением жиров. В качестве сырья применяют жир морских млекопитающих и растительные масла – подсолнечное, хлопковое и др. Гидрирование проводится в жидкой фазе при 160-200 0С и 2-15 атм. в присутствии никелевых катализаторов. Продукты гидрирования известны под различными названиями (салолин, саломас и др.).
Гидрогенезированные жиры сходны во всех отношениях с природными твердыми жирами. Гидрогенизацией некоторых распространенных растительных масел (масло земляного ореха, хлопковое, соевое) получают пищевые жиры. Так, искусственное масло, или маргарин, представляет собой эмульсию гидрогенизированного растительного жира в молоке; он имеет вид, консистенцию, запах и вкус сливочного масла. Запах и вкус придаются предварительным брожением молока с особыми видами молочных бактерий, вызывающих частичное окисление и синтезирующих диацетил – основное душистое вещество сливочного масла. Иногда прибавляют и синтетический диацетил. Для стабилизации эмульсии в маргарин вводят также природные эмульгаторы, такие, как яичный желток или лецитин, выделенный из желтка или сои.[1,3,4]
1.5 Аналитическая характеристика жиров
Кроме температуры плавления и затвердевания, для характеристики жиров применяются следующие величины: кислотное число, число омыления, йодное число.
Природные жиры нейтральны. Однако при переработке или хранении вследствие процессов гидролиза или окисления образуются свободные кислоты, количество которых непостоянно. Кислотное число представляет собой число миллиграммов гидроксида калия, необходимое для нейтрализации свободных жирных кислот, содержащихся в 1 г жира.
Число омыления равно числу миллиграммов гидроксида калия, расходующихся при омылении 1 г жира кипячением последнего с избытком гидроксида калия в спиртовом растворе. Число омыления чистого триолеина равно 192. Высокое число омыления указывает на присутствие кислот с «меньшими молекулами». Малые числа омыления указывают на присутствие более высокомолекулярных кислот или же неомыляемых веществ. При взаимодействии с щелочами жиры гидролизуются с образованием солей высокомолекулярных кислот, называемых «мылами».
Йодное число выражается числом граммов йода, которое может присоединяться по двойным связям к 100 г жира. Для определения йодного числа применяют растворы хлорида йода ICl, бромида йода IBr, или йода в растворе сулемы, которые более реакционноспособны, чем сам йод. Йодное число является мерой ненасыщенности кислот жиров. Оно важно для оценки качества высыхающих масел.[1,2]
2. Сложные липиды
Ткани головного и спинного мозга и главным образом биологические мембраны содержат сложные структурные единицы, построенные из белка холестерина и фосфолипидов - фосфатидов. Все сложные липиды содержат остаток жирных кислот. Спиртовая часть может быть представлена глицерином, сфингозином, инозитом.[3,4]
2.1 Фосфолипиды
Фосфолипиды представляют собой эфиры многоатомных спиртов глицерина или сфингозина с высшими жирными кислотами и фосфорной кислотой. В состав фосфолипидов входят также азотсодержащие соединения: холин, этаноламин или серин. В зависимости от того какой многоатомный спирт участвует в образовании фосфолипиды (глицерин или сфингозин), последние делят на 2 группы Глицерофосфолипиды и сфингофосфолипиды. Необходимо отметить, что в глицерофосфолипидах либо холин, либо этаноламин или серин соединены эфирной связью с остатком фосфорной кислоты; в составе сфинголипидов обнаружен только холин. Наиболее распространёнными в тканях животных являются глицерофосфолипиды.[4,5]
2.1.1 Глицерофосфолипиды
Глицерофосфолипиды являются производными фосфатидной кислоты. В их состав входят глицерин, жирные кислоты, фосфорная кислота и обычно азотсодержащие соединения. Общая формула глицерофосфолипидов выглядит так:
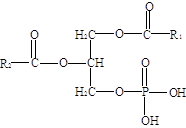
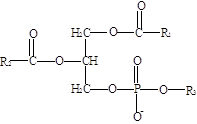
В этих формулах R1 и R2- радикалы высших жирных кислот, a R3-чаще, радикал азотистого соединения. Для всех глицерофосфолипидов характерно, что одна часть их молекул (радикалы R1 и R2) обнаруживает резко выраженную гидрофобность, тогда как другая часть гидрофильна благодаря отрицательному заряду фосфорной кислоты и положительному заряду радикала R3.
Из всех липидов глицерофосфолипиды обладают наиболее выраженными полярными свойствами. При помещении глицерофосфолипидов в воду в истинный раствор переходит лишь небольшая их часть, основная же масса липидов находится в виде мицелл. Существует несколько групп (подклассов) глицерофосфолипидов. В зависимости от характера азотистого основания, присоединенного к фосфорной кислоте, глицерофосфолипиды подразделяют на фосфатидилхолины (лецитины), фосфатидилэтаноламины (кефалины) и фосфатидилсерины. В состав некоторых глицерофосфолипидов вместо азотсодержащих соединений входит не содержащий азота шестиуглеродный циклический спирт инозит, называемый также инозитолом. Эти липиды называются фосфатидилинозитолами.
Фосфатидилхолины (лецитины). В отличие от триглицеридов в молекуле фосфатидилхолина одна из трех гидроксильных групп глицерина связана не с жирной, а с фосфорной кислотой. Кроме того, фосфорная кислота в свою очередь соединена эфирной связью с азотистым основанием-холином [НО—СН2—СН2—N+(CH3)3]. Таким образом, в молекуле фосфатидилхолина соединены глицерин, высшие жирные кислоты, фосфорная кислота и холин:
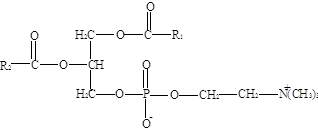
Фосфатидилэтаноламины. Основное различие между фосфатидилхалинами и лецитинами - наличие в составе последних азотистого основания этаноламина (НО-СН2-СН2- NН3):
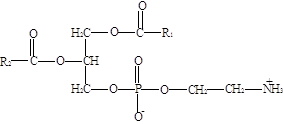
Из глицерофосфолипидов в организме животных и высших растений в наибольшем количестве встречаются фосфатидилхолины и фосфатидилэтаноламины. Эти 2 группы глицерофосфолипидов метаболические связаны друг с другом и являются главными липидными компонентами мембран клеток.
Фосфатидилсерины. В молекуле фосфатидилсерина азотистым соединением служит остаток аминокислоты серина.
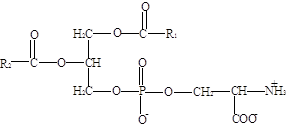
Фосфатидилсерины распространены гораздо менее широко, чем фатидилхолины и фосфоэтаноламины, и их значение определяется в основном тем, что они участвуют в синтезе фосфатидилэтаноламинов.
Фосфатидилинозитолы. Эти липиды относятся к группе производных фосфатидной кислоты, но не содержат азота. Радикалом (R3) в подклассе глицерофосфолипидов является шестиуглеродный циклический спирт инозитол. Фосфатидилинозитолы довольно широко распространены в природе. Они обнаружены у животных, растений и микроорганизмов. В животном организме найдены в мозге, печени и лёгких.
Плазмалогены. Эти фосфоглицериды содержат α, β-ненасыщенный спирт, образующий простую эфирную связь в положении С-1 L-глнцеро-З-фосфата (в отличие от сложноэфирной связи, образуемой остатке жирной кислоты). Так, плазмалогены, содержащие этаноламин имеют следующую структуру:
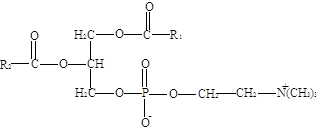
Фосфатидальхолины, фосфатидальэтаноламины и фосфатидальсернны — три основных класса плазмалогенов. Простые эфирные связи α,β-ненасыщенных спиртов в этих соединениях стабильны в разбавленных щелочах, однако в разбавленных кислотах они гидролизуются с образованием альдегида соответствующего α,β- ненасыщенного спирта. α,β- Ненасыщенные спирты имеют цис-конфигурацню и длину цени от С12 до С18. В чистом фосфатидальхолине из бычьего сердца остаток жирной кислоты в положении С-2, как правило, является ненасыщенным, тогда как спиртовый остаток в С-1-положеини является обычно насыщенным (исключение составляет лишь α,β-двойная связь). В тканях животных были обнаружены плазмалогены, не содержащие азотистых оснований, а также подобные триацнлглнцерпнам нейтральные плазмалогены, содержащие две сложноэфирные связи и одну простую эфирную связь, образованную α,β-ненасыщенным спиртом в С-1-положеннн (1-алкенил-2,3-диацилглицерин).
Производные 1-алкил-2-ацилфосфатнднлхолпна широко распространены в животных тканях. Эти соединения имеют общую формулу. Хотя содержание этих веществ в живых организмах составляет лишь несколько процентов общего количества фосфоглицеридов, они обнаружены в значительных количествах в эритроцитах, а в тканях некоторых беспозвоночных их содержание достигает 25% общего количества фосфоглицеридов.[4]
Кардиолипин. Своеобразным представителем глицерофосфолипидов является кардиолипин, впервые выделенный из сердечной мышцы. По своей химической структуре кардиолипин можно рассматривать как соединение, в котором 2 молекулы фосфатидной кислоты связаны с помощью одной молекулы глицерина. В отличие от остальных глицерофосфолипидов кардиолипин является как бы «двойным» глицерофосфолипидом. Кардиолипин локализован во внутренней мембране митохондрий. Функция его пока неясна, хотя известно, что в отличие от других фосфолипидов кардиолипин обладает иммунными свойствами:

В этой формуле Rl , R2, R3, R4-радикалы высших жирных кислот.
Необходимо отметить, что в природе встречается свободная фосфатидиая кислота, но в относительно небольших количествах по сравнению с глицерофосфолипидами. Среди жирных кислот, входящих в состав глицерофосфолипидов, обнаружены как насыщенные, так и ненасыщенные (чаще стеариновая, пальмитиновая, олеиновая и линолевая).
Установлено также, что большинство фосфатидилхолинов и фосфати-дилэтаноламинов содержат одну насыщенную высшую жирную кислоту «положении С-1 и одну ненасыщенную высшую жирную кислоту в положении С-2. Гидролиз фосфатидилхолинов и фосфатидилэтаноламинов при участии особых ферментов (эти ферменты относятся к фосфолипазам А2), содержащихся, например, в яде кобры, приводит к ненасыщенной жирной кислоты и образованию лизофосфолипидов - лизофосфатидилхолинов, или лизофосфатидилэтаноламинов оказывающих сильное гемолитическое действие.[5,6]
2.1.2 Сфинголипиды (сфингофосфолипиды)
Сфингомиелины. Это наиболее распространенные сфинголипиды. В основном они находятся в мембранах животных и растительных клеток. Особенно богата ими нервная ткань. Сфингомиелины обнаружены так же в тканях почек печени и других органов. При гидролизе сфингомиелины образуют одну молекулу жирной кислоты одну молекулу двухатомного ненасыщенного спирта сфингозина одну молекулу азотистого основания и одну молекулу фосфорной кислоты. Общую формулу сфингомиелинов можно представить так:
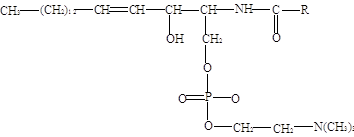
Общий план построения молекулы сфингомиелина в определенном отношении напоминает строение глицерофосфолипидов. Молекула сфингомиелинов содержит как бы полярную «головку», которая несет одновременно, и положительный (остаток холина), и отрицательный (остаток фосфорной кислоты) заряды и два неполярных «хвоста» (длинные алифатическая цепь сфингозина и ацильный радикал жирной кислоты).[4]
2.2 Гликолипиды (гликосфинголипиды)
Гликолипиды широко представлены в тканях, особенно в нервной ткани, в частности в мозге. Главной формой гликолипидов в животных тканях являются гликосфинголипиды. Последние содержат церамид, состоящий из спирта сфингозина и остатка жирной кислоты, и один или несколько остатков сахаров.
Простейшими гликосфинголипидами являются галактозилцерамиды и глюкозилцерамиды.
Галактозилцерамиды - главные сфинголипиды мозга и других нервных тканей, но в небольших количествах встречаются и во многих других тканях. В состав галактозилцерамидов входит гексоза (обычно это D-галактоза), которая связана эфирной связью с гидроксильной группой аминоспирта сфингозина. Кроме того, в составе галактозилцерамида имеется жирная кислота. Чаще всего это лигноцериновая, нервоновая или цереброновая кислота, т. е. жирные кислоты, имеющие 24 углеродных атома. Существуют сульфогалактозилцерамиды, которые отличаются от галактозилцерамидов наличием остатка серной кислоты, присоединенного к третьему углеродному атому гексозы. В мозге млекопитающих сульфогалактозилцерамиды в основном находятся в белом веществе, при этом содержание их в мозге намного ниже, чем галактозилцерамидов.
Глюкозилцерамиды - это простые гликосфинголипиды, представлены в тканях, отличных от нервной, причем главным образом глюкозилпцрамидами. В небольших количествах они имеются в ткани мозга. В отличие от галактозилцерамидов у них вместо остатка галактозы имеется остаток глюкозы.
Более сложными гликосфинголипидами являются ганглиозиды, образующиеся из гликозилцерамидов. Ганглиозиды дополнительно содержат одну или несколько молекул сиаловой кислоты. В тканях человека доминирующей сиаловой кислотой является нейраминовая. Кроме того, вместо остатка глюкозы они чаще содержат сложный олигосахарид. Ганглиозиды в больших количествах находятся в нервной ткани. Они, по-видимому, выполняют рецепторные и другие функции. Одним из простейших ганглиозидов является гаметозид выделенный из стромы эритроцитов. Он содержит церамид одну молекулу глюкозы одну молекулу N- ацетилнейраминовой кислоты.[4,7]
2.3 Стероиды
Все рассмотренные липиды принято называть омыляемыми, поскольку при их щелочном гидролизе образуются мыла. Однако имеются липиды, которые не гидролизуются с освобождением жирных кислот. К таким липидам относятся стероиды. Стероиды - широко распространенные в природе соединения. Они часто обнаруживаются в ассоциации с жирами. Их можно отделить от жира путем омыления (они попадают в неомыляемую фракцию). Все стероиды в своей структуре имеют ядро, образованное гидрированным фенантреном (кольца А, В и С) и циклопентаном (кольцо D).
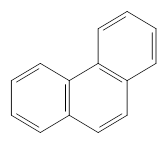
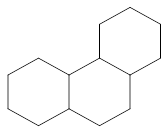
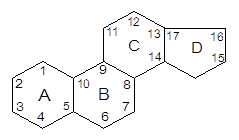
Фенантрен Пергидрофенантрен Общая структурная основа стероидов.[4]
К стероидам относятся, например, гормоны коркового вещества надпочечников, желчные кислоты, витамины группы D, сердечные гликозиды и другие соединения. В организме человека важное место среди стероидов занимают стерины (стеролы), т. е. стероидные спирты. Главным представителем стеринов является холестерин (холестерол).
Ввиду сложного строения и асимметрии молекулы стероиды имеют много потенциальных стереоизомеров. Каждое из шестиуглеродных колец (кольца А, В и С) стероидного ядра может принимать две различные пространственные конформации - конформацию «кресла» либо «лодки».
В природных стероидах, в том числе и в холестерине, все кольца в форме «кресла», что является более устойчивой конформацией. В свою очередь по отношению друг к другу кольца могут находиться в цис- или транс-положениях.
Холестерин. Как отмечалось, среди стероидов выделяется группа соединений, получивших название стеринов (стеролов). Для стеринов характерно наличие гидроксильной группы в положении 3, а также боковой цепи в положении 17. У важнейшего представителя стеринов - холестерина - все кольца находятся в транс-положении; кроме того, он имеет двойную связь между 5-м и 6-м углеродными атомами. Следовательно, холестерин является ненасыщенным спиртом. Кольцевая структура холестерина отличается значительной жесткостью, тогда как боковая цепь - относительной подвижностью. Итак, холестерин содержит спиртовую гидроксильную группу при С-3 и разветвленную алифатическую цепь из 8 атомов углерода при С-17. Химическое название холестерина 3-гидрокси-5,6-холестин. Гидроксильная группа при С-3 может быть эстерифицирована высшей жирной кислотой, при этом образуются эфиры холестерина (холестериды).
Холестерин - источник образования в организме млекопитающих желчных кислот, а также стероидных гормонов. Физиологические функции холестерина многообразны.[4,7]
3. Липиды и строение биологических мембран
Все клетки, даже самые простые, имеют мембраны. Мембраны отделяют внутреннее содержимое клетки от окружающей среды, поэтому нарушение мембраны приводит к гибели клетки. Мембраны не сохраняют молекулы веществ, входящих в ее состав, но и реализуют специфику химического состава клеточной цитоплазмы. С помощью специальных устройств мембрана избирательно выбрасывает из клетки нужные вещества и поглощает из окружающей среды необходимые. Главные компоненты биологических мембран живых организмов — это сложные липиды. Следует обратить внимание на то, что все сложные липиды, имеют характерное строение для поверхностно-активных веществ, т. е. две большие неполярные углеводородные группы и полярную часть, способную к образованию водородных связей. Таким образом, эти молекулы способны самопроизвольно агрегировать, образуя в воде бислойные структуры, составляющие основу мембраны. В состав мембранного бислоя входят и молекулы белков, и свободные жирные кислоты. Последние встраиваются в бислой так, что их «жирные хвосты» погружены внутрь, а полярные группы во внешнюю среду и контактируют с ионами натрия с внешней, а с ионами калия с внутренней стороны бислоя. Биологические мембраны не только регулируют обмен веществ в клетке, но и воспринимают химическую информацию из внешней среды с помощью специальных рецепторов. Биологические мембраны обеспечивают иммунитет клетки, нейтрализуя чужие и свои вредные вещества. Они также способны передавать информацию соседним клеткам о своем состоянии. Наконец, совсем недавно было обнаружено, что многие белки - ферменты могут «работать» только внутри мембраны, запрещая, разрешая или сопрягая ферментативные процессы.[1,8,9]
4. Применение жиров
Животные жиры находят широкое применение, прежде всего, в качестве продуктов питания. Важные пищевые жиры говяжий, бараний и свиной — получают из жировых тканей рогатого скота и свиней. Из тканей морских млекопитающих и рыб приготовляют пищевые, медицинские, ветеринарные (кормовые) и технические жиры. Пищевые жиры, перерабатываемые путём гидрогенизации на маргарин, производят из жировых тканей усатых китов (сейвалы, финвалы и др.). Медицинские жиры, содержащие витамин А и используемые как лечебный и профилактический препарат, получают из печени тресковых рыб: трески, пикши, сайры и др. Ветеринарные жиры предназначаются для подкормки животных и птиц и приготовляются из тканевых и печёночных жиров рыб и морских млекопитающих. Технические жиры используют в лёгкой, химической, парфюмерной промышленности и в других отраслях народного хозяйства для обработки кож, выработки моющих и пеногасительных средств и различных кремов и помад. Технический рыбий жир получают преимущественно в процессе производства кормовой муки из различных отходов (головы, кости, внутренности, плавники), из малоценных в пищевом отношении и некондиционных рыб, из некондиционного сырья, получаемого при переработке усатых китов и ластоногих. Техническим относятся также жиры, получаемые из зубатых китов (главным образом кашалотов) и характеризующиеся большим содержанием восков, что делает их непригодными для пищевых целей.
Животные жиры выделяют из жировой ткани и отделяют от белков и влаги посредством нагревания выше температуры плавления. Вытопку жиров из измельченной ткани производят в открытых котлах, а из неизмельчённой — в автоклавах под давлением. Для вытопки пищевых и других жиров широко применяют установки непрерывного действия АВЖ (отечественного производства), «Титан» (Дания), «Де-Лаваль» (Швеция) и др. Длительность процесса с момента загрузки жирового сырья до получения готового продукта составляет на этих установках 7—10 мин. Вытопка животных жиров на непрерывнопоточной установке АВЖ, широко применяемой в мясной промышленности, включает следующие стадии (см. схему). Сырьё загружают в воронку центробежной машины 1, где оно измельчается ножами и нагревается паром до температуры 85—90°С. Полученная жиромасса поступает через питательный бачок 2 в горизонтальную центрифугу 3 для отделения белков от жира и воды. Жир с водой через центробежную машину 4 направляется в питательный бачок 5 и затем в сепараторы 6 (на схеме показан один) на 2—3-кратную очистку. Прозрачный жир посредством центробежной машины 7 подаётся в приёмник 8, из которого поступает в шнековый аппарат 9 на охлаждение до температуры 35—42 °С, а затем на розлив упаковку в тару.[10,11,12]
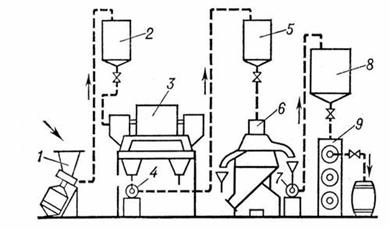
Схема непрерывнопоточной установки АВЖ для производства животных жиров: 1 — центробежная машина АВЖ-245; 2, 5 питательные бачки; 3 — центрифуга; 4, 7 — центробежные машины АВЖ-130; 6 сепаратор; 8 — приёмник жира; 9 — шнековый охладитель.[13]
Масла растительные жирные, растительные жиры, продукты, извлекаемые из масличного сырья и состоящие в основном (на 95—97 %) из триглицеридов, сложных полных эфиров глицерина и жирных кислот. Кроме триглицеридов (бесцветных веществ без запаха и вкуса), в состав жирных масел растительных входят воски и фосфатиды, а также свободные жирные кислоты, липохромы, токоферолы, витамины и другие вещества, сообщающие маслам окраску, вкус и запах. К жирным растительным маслам относятся: абрикосовое, арахисовое, арбузное, буковое, виноградное, вишнёвое, горчичное масло, дынное, касторовое масло, кедровое, кокосовое масло, конопляное масло, кориандровое, кукурузное масло, кунжутное масло, льняное масло, маковое, масло какао, крамбе, ляллеманцевое, миндальное, молочайное, оливковое масло, ореховое, пальмовое, пальмоядровое, перилловое масло, персиковое, подсолнечное масло, рапсовое масло, рисовое, рыжиковое, сафлоровое масло, сливовое, соевое масло, сурепное масло, томатное, тунговое масло, тыквенное, хлопковое масло и другие.[13,14]
Свойства жирных растительных масел определяются в основном составом и содержанием жирных кислот, образующих триглицериды. Обычно это насыщенные и ненасыщенные (с одной, двумя и тремя двойными связями) одноосновные жирные кислоты с неразветвлённой углеродной цепью и чётным числом углеродных атомов (преимущественно C16 и C18). Кроме того, в жирных маслах растительных обнаружены в небольших количествах жирные кислоты с нечётным числом углеродных атомов (от C15 до C23). В зависимости от содержания непредельных жирных кислот меняется консистенция масел и температура их застывания: у жидких масел, содержащих больше непредельных кислот, температура застывания обычно ниже нуля, у твёрдых масел достигает 40 °С. К твёрдым маслам растительным относятся только масла некоторых растений тропического пояса (например, пальмовое). При контакте с воздухом многие жидкие жирные масла подвергаются окислительной полимеризации («высыхают»), образуя плёнки. По способности к «высыханию» масла делят на ряд групп в соответствии с преимущественным содержанием тех или других непредельных кислот; например, масла, высыхающие подобно льняному маслу (льнянообразно высыхающие), из непредельных содержат главным образом линоленовую кислоту. Касторовое масло, содержащее в основном рицинолевую кислоту, вообще не образует плёнок.[14,15]
Основная биологическая ценность масел растительных заключается в высоком содержании в них полиненасыщенных жирных кислот, фосфатидов, токоферолов и других веществ. Наибольшее количество фосфатидов содержится в соевом (до 3000 мг %), хлопковом (до 2500 мг %), подсолнечном (до 1400 мг %) и кукурузном (до 1500 мг %) маслах. Высокое содержание фосфатидов отмечается только в сырых и нерафинированных масел растительных. Биологически активным компонентом растительных масел являются стерины, содержание которых в различных маслах неодинаково. Так, до 1000 мг % стеринов и более содержит масло пшеничных зародышей, кукурузное масло;100 мг % подсолнечное, соевое, рапсовое, хлопковое, льняное, оливковое, до 200 мг % арахисовое и масло какао; до 60 мг % — пальмовое, кокосовое. Масла растительные полностью свободны от холестерина. Очень высоким количеством токоферолов (100 мг % и более) характеризуются масла пшеничных отрубей, соевое и кукурузное масла, до 60 мг % токоферолов в подсолнечном, хлопковом, рапсовом и некоторых других маслах, до 30 мг % — в арахисовом, до 5 мг % — в оливковом и кокосовом. Общее содержание токоферолов ещё не является показателем витаминной ценности масла. Наибольшей витаминной активностью обладает подсолнечное масло, поскольку все его токоферолы представлены α - токоферолом, меньшую E-витаминную активность имеют хлопковое и арахисовое масла. Что касается соевого и кукурузного масел, то они почти полностью лишены витаминной активности, поскольку 90 % общего количества их токоферолов представлены антиокислительными формами.[14]
Области применения масел многообразны. Жирные растительные масла являются важнейшим пищевым продуктом (подсолнечное, хлопковое, оливковое, арахисовое, соевое и др.) и применяются для изготовления консервов, кондитерских изделий, маргарина. В технике из масел производят мыла, олифы, жирные кислоты, глицерин, лаки и другие материалы.
Мыла, соли высших жирных кислот. В производстве и быту мылом (или товарными мылами) называют технические смеси водорастворимых солей этих кислот, часто с добавками некоторых др. веществ, обладающие моющим действием. Основу смесей обычно составляют натриевые (реже калиевые и аммониевые) соли насыщенных и ненасыщенных жирных кислот с числом атомов углерода в молекуле от 12 до 18 (стеариновой, пальмитиновой, миристиновой, лауриновой и олеиновой). К мылам часто относят также соли нафтеновых и смоляных кислот, а иногда и др. соединения, обладающие в растворах моющей способностью. Водорастворимые мыла — типичные мицеллообразующие поверхностно-активные вещества. При концентрации выше определённого критического значения в мыльном растворе наряду с отдельными молекулами (ионами) растворённого вещества находятся мицеллы — коллоидные частицы, образованные скоплением молекул в крупные ассоциаты. Наличие мицелл и высокая поверхностная (адсорбционная) активность М. обусловливают характерные свойства мыльных растворов: способность отмывать загрязнения, пениться, смачивать гидрофобные поверхности, эмульгировать масла и др.[16]
Вывод
Наряду с белками, нуклеиновыми кислотами и углеводами липиды обеспечивают основные функции в процессах жизнедеятельности. Являясь ключевыми компонентами биологических мембран, липиды в их составе обладают свойствами специфических регуляторов внутриклеточных метаболических превращений, участвуют в осуществлении межклеточных взаимодействий, проведении нервного импульса, мышечном сокращении. Эти соединения обеспечивают энергетические потребности клетки, создавая резерв энергии, накапливающейся в ходе биохимических реакций. Они также выполняют важную роль водо- и термозащитного барьера, обеспечивают механическую плотность клеток.
По мнению многих специалистов, липиды представляют собой очень перспективный и далеко не полностью исчерпанный источник потенциальных лекарственных и диагностических препаратов. Однако многие физиологические функции липидов еще до конца не выяснены. Эти вещества таят в себе много загадок, которые еще предстоит разгадать ученым.
Список литературы
1. Грандберг И.И. Органическая химия. - М: Дрофа. - 2001. - С. 393-401.
2. Уайт А. Хендлер Ф. Смит Э. Хилл Р. Леман И. Основы биохимии. - Т. 1 -М: Мир. - 1981. - С. 54-92.
3. Николаев А.Я. Биологическая химия. - М. - 2004. - С. 287- 326.
4. Березов Т.Т. Корявкин Б.Ф. Биологическая химия. - М. - 1998. - С. 188-203.
5. Агрономов А.Е. Избранные главы органической химии. - М. - 1975. - С. 125-136.
6. Зинин И.Н. Труды по органической химии. - М: Наука. - 1982. - С. 115-131.
7. Кери Ф. Сандбер Р. Углубленный курс органической химии. - М. - 1981 - С. 231-253.
8. Альбертс Б. Брей Д. Молекулярная биология клетки. - М: Мир. - 1994. - С. 98-104.
9. Грин Н. Стаут У. Тейлор Д. Биология. - М: Мир. - С. 134-156.
10. Головкин Н.А., Перкель Р.Л. Анализ свободных жирных кислот в природных жирах методом газо-жидкостной хроматографии // в Трудах ВНИИЖ. Выпуск 27. - 1970.
11. Аркадьева З.А., Безбородов А.М. Промышленная микробиология. - М: Высшая школа. - 1989г. - С. 74-88.
12. Евстигнеева Р.П., Звонкова Е.Н. Химия липидов. - М. - 1983. - С. 83-96.
13. Белобородов В.В. Основные процессы производства растительных масел. - М.- 1966.
14. Беззубов Л.П. Химия жиров.- М: Пищевая промышленность. - 1975. - С. 65-79.
15. Тютюнников Б.Н. Химия жиров. - М: Колос - 1992. - С. 102-118.
16. Голдовский А.М. Теоретические основы производства растительных масел. - М.- 1958. - С. 45-67.
17. Белобородов В.В. Основные процессы производства растительных масел. - М. - 1966 -С. 75-86.
18. Хомченко Г.Г. Сборник заданий по химии для поступающих в ВУЗы. - М. - 1998 -С. 67-70.
19. Габриелян О.С. Маскаев Ф.Н. Пономарёв С.Ю. Химия 10 класс. - М. - 1998. - С. 78-82.
20. Иванищев В.В. Сборник заданий для самостоятельной работы. - Т. -2002. - С. 17-20.
Приложение 1
1. Натуральное сливочное масло содержит жиры смешанного характера, содержащие остатки как предельных, как и не придельных карбоновых кислот. Как, используя раствор перманганата калия отличить маргарин от сливочного масла? Можно ли этим способом отличить растительное масло от машинного (минерального)? Как?
2. Как, не используя раствор перманганата калия отличить маргарин от сливочного масла?
3. Сколько изомеров жиров образуют при омылении глицерин и смесь стеарата и пальмитата натрия? Составьте структурные формулы, отвечающие возможным вариантам состава и строения жира? Составьте уравнение реакции омыления одного из них. Могли ли образоваться равные количества пальмитата и стеарата, если жир представлял собой чистое вещество, а не смесь?
4. Неприятный запах горелого масла и любых перегретых жиров объясняется образованием акролеина (пропеналя) который является продуктом дегидратации глицерина. Какие реакции, протекающие при жарке пищи приводят к образованию акролеина из жиров?
5. Напишите формулу 1,3-димиристил-2-стеарил-sn-глицерола.
6. Напишите формулу sn-глицерол-2-стеарил-3-олеината.
7. Напишите формулу 1-стеарил-3-пальмитил-sn-глицерола.
8. Напишите формулу sn-глицерол-1,3-диленолената.
9. Напишите формулу 1-миристил-2-стеарил-sn-пицерола.
10. Напишите формулу любого фосфолипида.
11. Напишите формулу любого стероида.
12. Напишите формулу любого гликолипида
13. Напишите формулу любого терпена.
14. Напишите формулу любого воска.
15. Напишите словами реакцию, которую катализирует ацетил-КоА - карбоксилаза.
16. Напишите реакцию, которую катализирует синтеза жирных кислот при восстановлении кетогруппы до гидроксигруппы у одного из промежуточных продуктов при синтезе пальмитиновой кислоты.
17. Напишите реакцию, которую катализирует синтаза жирных кислот при удлинении углеродной цепи жирной кислоты до 8 атомов.
18. Напишите реакцию, которая протекает in vivo после синтеза пальмитоил - КоА.
19. Напишите реакцию, которую катализирует синтаза жирных кислот при восстановлении двойной связи в промежуточных продуктах при синтезе пальмитиновой кислоты.
20. По какой причине в синтезе жирных кислот используется фосфопроизводное глицерола, а не сам глицерол?
21. Для чего в синтезе жирных кислот используется ферментативная система их денатурации?
22. По какой причине в синтезе жирных кислот у животных в качестве источника Ац-КоА используется цитрат?
23. Для чего в синтезе жирных кислот используется ферментативная система их удлинения?
24. По какой причине в синтезе жирных кислот используется малонил-КоА?
25. В чем особенности строения системы денатурации растений?
26. В чем особенности строения системы десатурации животных?
27. В чем особенности строения Ац-Ко А- карбоксилазы?
28. В чем особенности строения синтезы жирных кислот?
29. В чем особенности строения ферментативной системы удлинения углеродной цепи?
30. Какова биологическая роль альфа-пути окисления липидов?
31. Каково биологическое значение диоксиацетонфосфата для синтеза липидов?
32. Какова биологическая роль омега-окисления жирных кислот?
33. Какова биологическая роль карнитина?
34. Какова биологическая роль бета-пути окисления липидов?
35. Что такое кетоновые тела?
36. Как регулируется метаболизм липидов?
37. Как метаболизм липидов связан с обменом углеводов?
38. Как метаболизм липидов связан с обменом белков?
39. При гидролизе жира массой 222‚5 г. получили предельную одноосновную кислоту213 г. и глицерин. Определите формулу жира и назовите его.
40. Образец жира представляющий собой триолетат подвергли гидролизу. Какая масса жира была взята, если на гидрирование полученной кислоты затратили водород объёмом 336 литров (нормальные условия).
© 2010 Интернет База Рефератов