Рефераты по сексологии
Рефераты по информатике программированию
Рефераты по биологии
Рефераты по экономике
Рефераты по москвоведению
Рефераты по экологии
Краткое содержание произведений
Рефераты по физкультуре и спорту
Топики по английскому языку
Рефераты по математике
Рефераты по музыке
Остальные рефераты
Рефераты по авиации и космонавтике
Рефераты по административному праву
Рефераты по безопасности жизнедеятельности
Рефераты по арбитражному процессу
Рефераты по архитектуре
Рефераты по астрономии
Рефераты по банковскому делу
Рефераты по биржевому делу
Рефераты по ботанике и сельскому хозяйству
Рефераты по бухгалтерскому учету и аудиту
Рефераты по валютным отношениям
Рефераты по ветеринарии
Рефераты для военной кафедры
Рефераты по географии
Рефераты по геодезии
Рефераты по геологии
Рефераты по геополитике
Рефераты по государству и праву
Рефераты по гражданскому праву и процессу
Рефераты по делопроизводству
Рефераты по кредитованию
Рефераты по естествознанию
Рефераты по истории техники
Рефераты по журналистике
Рефераты по зоологии
Рефераты по инвестициям
Рефераты по информатике
Исторические личности
Рефераты по кибернетике
Рефераты по коммуникации и связи
Курсовая работа: Электроосаждение металлов
Курсовая работа: Электроосаждение металлов
Федеральное агентство по образованию
Калужский Государственный Педагогический
Университет им. К.Э. Циолковского
Кафедра философии и социологии
Электроосаждение металлов.
Калуга, 2008г.
Содержание
Глава 1 История
1.1. СТРАНИЦЫ ИСТОРИИ
1.2. СТРУКТУРА ЭЛЕКТРООСАЖДЕННЫХ МЕТАЛЛОВ
1.3. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ ОСНОВА ЭЛЕКТРОХИМИЧЕСКИХ ТЕХНОЛОГИЙ
Глава 2. Электрохимическое выделение металлов
2.1. ОБЩАЯ ХАРАКТЕРИСТИКА ПРОЦЕССОВ
2.2. ОБРАЗОВАНИЕ МОНОАТОМНЫХ СЛОЕВ МЕТАЛЛОВ ПРИ ПОТЕНЦИАЛАХ ПОЛОЖИТЕЛЬНЕЕ РАВНОВЕСНЫХ
2.3. ВЛИЯНИЕ РАЗЛИЧНЫХ ФАКТОРОВ НА ПРОЦЕССЫ КАТОДНОГО ВЫДЕЛЕНИЯ МЕТАЛЛОВ
2.3.1. Роль природы металла
2.3.2. Роль состава раствора
2.4. ПРИРОДА МЕТАЛЛИЧЕСКОГО ПЕРЕНАПРЯЖЕНИЯ
2.5. ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ ВЕЛИЧИНУ ПОЛЯРИЗАЦИИ ПРИ КАТОДНОМ ВЫДЕЛЕНИИ РАЗЛИЧНЫХ МЕТАЛЛОВ
2.5.1. Энергия иона в металле и его состояние в растворе
2.5.2. Активность поверхности катода в процессе осаждения металлов
2.5.3. Заряд поверхности металла в условиях его катодного осаждения
2.5.4. Другие возможные причины появления металлического перенапряжения
Заключение
ГЛАВА 1 ИСТОРИЯ
1.1. СТРАНИЦЫ ИСТОРИИ
Электрохимия принадлежит к числу тех немногих наук, дата рождения которых может быть установлена с высокой точностью. Это рубеж XVIII и XIX веков, когда благодаря знаменитым опытам итальянского физиолога Л. Гальвани и созданию итальянским физиком А.Вольта в 1799 году «вольтова столба» — первого в истории человечества химического источника тока — были сформулированы проблемы, решение которых определило основные задачи электрохимии.
«Без химии путь к познанию истинной природы электричества закрыт» — эта мысль принадлежит великому М.В.Ломоносову, который сделал исключительно важные наблюдения и замечания о природе пассивности металлов. Как под влиянием Ломоносова, так и в соответствии с общей ситуацией в науке, в Московском университете электрохимические исследования всегда занимали важное место и при этом оказывались чрезвычайно результативными [1–3]. Так, в 1807 г. российский академик Ф.Ф.Рейсс открыл явления электроосмоса и электрофореза. Значительно опередили свое время работы профессора физики А.П.Соколова, впервые применившего переменный ток для определения емкости электрода (1887 г.).
Фундаментальный вклад в теорию растворов электролитов внес профессор И.А.Каблуков [4], указавший пути к объединению гидратной теории растворов Д.И.Менделеева и теории электролитической диссоциации С.Аррениуса на основе представления о диссоциации как взаимодействии с растворителем. Каблуков исследовал свойства неводных растворов и открыл явление аномальной электропроводности. Как автор известного учебника по физической химии и электрохимии (первое издание — 1902 г.) И.А.Каблуков оказал огромное влияние на распространение электрохимических знаний в нашей стране. Он был твердо уверен в том, что «без знания электрохимии нельзя приступить к решению многих вопросов не только в области минеральной, но и органической химии; на законах электрохимии основаны методы исследования различных вопросов химической механики...».
В 1911 г. Е.И. Шпитальским было открыто явление электрополировки металлов, которое изучалось в дальнейшем сотрудниками и студентами лаборатории физической химии под его руководством. Одновременно проводились работы и по другим вопросам теоретической и технической химии (электрохимическое получение бертолетовой соли, исследования хлорного электролиза, разработка новых электролитических способов получения свинцового глета и окиси меди и т.д.). В этих работах участвовали Н.Н.Петин, З.А.Иофа, А.В.Командин, В.В.Монбланова и др. Е.И.Шпитальский организовал также исследования реакций выделения водорода и кислорода на платиновых электродах с помощью специально разработанного коммутаторного метода. Изучалось влияние предварительной анодной и катодной обработки платины и палладия на их каталитическую активность в реакции разложения перекиси водорода (М.Я.Каган).
В 1929 г. Е.И. Шпитальский был избран членом-корреспондентом Академии наук СССР и в том же году его научная деятельность оборвалась: он был осужден по делу Промпартии.
Из более поздних работ, проводившихся уже после создания в 1929 году кафедры физической химии, особо следует отметить исследование Н.И.Кобозева и Н.И.Некрасова по механизму электрохимического выделения водорода на металлах (1930 г.). В этой работе впервые было указано на роль энергии связи адсорбированных атомов водорода с металлом в этом процессе. Н.И.Кобозев и В.В.Монбланова впервые использовали электрохимическую ячейку, разделенную палладиевой мембраной, для исследования диффузии атомарного водорода через палладий.
Анализируя влияние природы металла на скорость электрохимического выделения водорода, Н.И.Кобозев и В.В.Монбланова ввели понятие об электрокатализе как явлении ускорения электродной реакции в результате адсорбционного взаимодействия реагента или интермедиата с металлом электрода.
Таким образом, к началу 30х годов на кафедре физической химии работы по электрохимии проводились достаточно интенсивно, что привело к появлению специализации по электрохимии.
В 1930 г. лабораторию технической электрохимии МГУ возглавил А.Н.Фрумкин (1895–1976) автор фундаментальных экспериментальных и теоретических работ по равновесным свойствам заряженных межфазных границ, блестяще образованный ученый мирового класса, работы которого, несмотря на молодость автора, уже стояли в одном ряду с трудами Нернста, Липпмана, Лэнгмюра. В 1932 г. он был избран действительным членом Академии наук СССР. Под руководством академика Фрумкина лаборатория технической электрохимии была преобразована в 1933 году в кафедру электрохимии. В этот период ближайшими сотрудниками А.Н.Фрумкина в МГУ были З.А.Иофа и А.И. Шлыгин, которые работали до этого в области электрохимии как сотрудники кафедры физической химии. А.Н.Фрумкин руководил кафедрой до 1976 г.; с 1976 по 1998 гг. кафедру возглавлял проф. Б.Б.Дамаскин, а с ноября 1998 г. кафедрой заведует проф. О.А.Петрий.
1.2. СТРУКТУРА ЭЛЕКТРООСАЖДЕННЫХ МЕТАЛЛОВ
Роль структуры электролитических осадков в гальванотехнике
Структура электроосажденных металлов является одним из существенных признаков, определяющих нормальное течение, а в некоторых случаях и принципиальную возможность проведения электрометаллургического процесса. Однако между процессами электролитического рафинирования металлов или осаждения металлов с нерастворимыми анодами, с одной стороны, и процессами получения покрытия, с другой, с точки зрения роли структуры имеется принципиальная разница. В первых двух случаях приходится в первую очередь считаться с расходом электрической энергии. По этому признаку и выбирают состав электролита, режим и прочие условия процесса. Структура металла при электролитическом рафинировании их играет подчиненную роль, так как в большинстве случаев осаждающийся металл подвергается переплавке; достаточно для этого получать плотные, не осыпающиеся с катодной поверхности осадки. Важно также, чтобы на катоде не вырастали длинные кристаллы, которые могут вызывать короткие замыкания. При электроосаждении цинка, например, приходится сравнительно часто менять катоды также по соображениям ухудшения качества металла (в структурном отношении) по мере его наращивания.
В гальванотехнике структура осадка играет доминирующую роль в процессе. Расход электрической энергии не отражается сколько-нибудь заметит) на общей стоимости процесса покрытия, так что выбирают не тот электролит, который обладает наименьшим омическим сопротивлением, а тот, который дает возможность получить лучшие в структурном отношении осадки. Стоимость самого электролита допускается более высокой, чем в электрометаллургических процессах. Помимо состава самого электролита все остальные условия процесса также подбирают с той целью, чтобы они обеспечивали получение осадков плотных, мелкокристаллических, а в некоторых случаях даже блестящих.
Не говоря уже о том, что такие требования являются обязательными при декоративных покрытиях, следует отметить, что даже и в случаях осаждения электроотрицательных по отношению к железу металлов, например цинка или кадмия, химическая стойкость защищенного металла тем выше, чем плотнее и мельче структура электроосажденного металла. Еще большую роль структура покрытия играет при осаждении металлов, электроположительных по отношению к основному металлу, например при свинцевании или лужении железа. Как ниже будет показано, механические свойства покрытий также находятся в сильной зависимости от их структуры. По этим причинам мы подробно остановимся на факторах, влияющих в той или иной степени на структуру электроосажденных металлов.
Выделение металлов на катоде рассматривается как процесс кристаллизации. Последняя протекает в две стадии: образование центров кристаллизации (образование зародышей) и рост образовавшихся центров кристаллизации. Каждый из этих двух процессов протекает с определенной скоростью, и в зависимости от условий электролиза (температуры, плотности тока, перемешивания), природы осаждающегося металла и растворителя, наличия примесей в электролите и т. д. преобладает тот или другой процесс, в связи с чем получается та или иная структура металла. Число образующихся в единицу времени кристаллов можно рассматривать как равнодействующую относительных склонностей разряжающихся ионов к образованию новых зародышей и росту существующих кристаллов.
В гальванотехнике представляют ценность лишь равномерные мелкокристаллические осадки. Такие металлы, как железо, кобальт, никель, кристаллизуются из растворов своих простых солей, особенно при низких температурах, в виде мелкокристаллических, блестящих, почти зеркальных осадков. Ближайшие к катоду слои настолько мелкокристалличны, что они целиком воспроизводят форму металлической поверхности. Некоторые металлы (медь, цинк, сурьма, висмут) при, аналогичных условиях, хотя и дают более грубую структуру, но все же образуют плотные сплошные осадки, по крайней мере в тонких слоях. Лишь по мере утолщения осадка начинается, в первую очередь на краях и углах катода (где наблюдается большая плотность тока), образование дендритообразных осадков или наростов. Между тем такие металлы, как свинец — в уксуснокислом или азотнокислом растворе, олово в сернокислом или хлористом растворе, в отсутствии специальных добавок не могут быть осаждены в виде плотного мелкозернистого осадка. Отдельные кристаллы вырастают по направлению к аноду и в очень короткое время могут достичь длины в несколько сантиметров, вызывая короткое замыкание. При осаждении серебра из растворов простых солей также преобладает рост кристаллов над скоростью образования центров кристаллизации. Золото и платина в растворах простых солей выделяются на катоде в виде порошкообразных осадков.
Несмотря на указанные особенности природы металла, мы располагаем в настоящее время значительным количеством данных, позволяющих вести процесс электроосаждения таким образом, чтобы структура покрытия отвечала своему назначению. Вообще говоря, для каждого процесса необходимо соблюдать определенные условия, и общие положения, на которых мы ниже остановимся, имеют не абсолютное, а относительное значение. Нельзя, например, сказать, что если повышенная плотность тока или пониженная температура способствует получению мелкокристаллических осадков, то можно во всех случаях в одинаковой степени повышать плотность тока или понижать температуру. Тем не менее, учитывая особенности каждого конкретного случая, можно заранее сказать, в каком направлении может повлиять такое-то изменение состава электролита или выбор самого электролита, как повлияет, например, повышение плотности тока или температуры, перемешивание и т. д. Для этого нам надо ближе познакомиться с процессом образования металлического покрытия при электролизе.
Электрохимия является разделом науки, изучающим взаимодействие ионов (электрически заряженных частиц вещества, образующихся при потере или присоединении электронов) в электролитах и явления на границе между поверхностями твёрдых токопроводящих тел (электродов) и электролитом.
1.3. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ – ОСНОВА ЭЛЕКТРОХИМИЧЕСКИХ ТЕХНОЛОГИЙ
Общие понятия
Технология наука о ремеслах, о производстве. Электрохимические технологии (ЭХТ) многообразны и могут быть для облегчения ознакомления с ними разбиты на ряд разделов в соответствии с выбранным классификационным признаком. Например, в соответствии с природой производимых продуктов или услуг. По мере развития электрохимических технологий изменялись содержание и масштабы использования ее разделов. В основе всех электрохимических технологий лежат электрохимические процессы в электрохимических системах на границах электрод-электролит (межфазных границах). Они характеризуются, как и другие химические процессы термодинамическими и кинетическими параметрами.
Современный этап развития электрохимии межфазных границ как науки характеризуется, как отмечают специалисты1 как переход от феноменологических к молекулярным подходам. При этом детализация феноменологических подходов играет важную роль в «состыковке» расчетов и теоретических прогнозов молекулярного уровня с экспериментом. Выделяют следующие центральные проблемы:
- Разработка молекулярных моделей строения межфазных границ и адсорбционных слоев.
- Теоретическое описание и молекулярное моделирование элементарных стадий переноса заряженных частиц через межфазные границы.
- Установление кинетики и механизмов электрокаталитических процессов и создание моделей, учитывающих молекулярное строение адсорбционных слоев.
- Развитие феноменологических и микроскопических представлений о механизмах образования и роста новых фаз и коррозионно-электрохимических явлений.
- Создание теоретических основ электрохимических методов получения материалов с заданными (нано)структурой и свойствами и определение принципов функционирования таких материалов. Выявление специфических особенностей электрохимических явлений в наноразмерных системах.
- Совершенствование представлений о сложных стадийных электродных процессах на основе прямого наблюдения их интермедиатов и новых решений макрокинетических задач.
Большинство сформулированных выше фундаментальных проблем существовало в электрохимии межфазных границ на протяжении последних 30-50 лет, и современный этап характеризуется лишь смещением некоторых акцентов. В то же время формулировкой наноэлектрохимических проблем и задач наука полностью обязана прогрессу последнего десятилетия.
Достижения электрохимической науки определяют современное состояние и направления совершенствования ЭХТ.
Электрохимические технологии – это технологические процессы, используемые в производстве товаров и услуг, в основе которых лежат электрохимические процессы.
К основным группам ЭХТ относятся:
· электрохимическая энергетика;
· электрохимическая металлургия;
· электрохимические технологии химических товарных продуктов;
· электрохимические технологии в производстве изделий и инструмента в машиностроении и приборостроении;
· электрохимические технологии, используемые для защиты от коррозии объектов техники;
· электрохимическая сенсорика;
· электрохимические технологии в здравоохранении;
· электрохимические технологии пищевой воды.
Некоторые из классов современных электрохимических технологий в наиболее общих чертах рассмотрены.
Сильные и слабые стороны электрохимических технологий
Преимущества.
1. При производстве химических продуктов с помощью электрохимической технологии достигается высокая селективность электрохимических процессов, так как процессы окисления и восстановления на электродах протекают с участием электронов (а не сложных химических соединений в качестве реагентов).
2. В электрохимических процессах легко изменяется потенциал изменением тока, протекающего через электрод, достигая таких значений окислительно-восстановительного потенциала, которые создают уникальные возможности для процессов окисления и восстановления.
3. С использованием диафрагм или ионообменных мембран в электролизерах оказывается возможным одновременно получать несколько чистых продуктов (например, при электролизе раствора NaCl получают Cl2, H2 и щелочь).
Недостатки.
1. Большой расход электроэнергии, которая затрачивается на электрохимические превращения.
2.Относительно невысокая производительность электрохимических процессов (гетерогенных процессов, протекающих на границе электрод-раствор). В результате имеют место относительно высокие капитальные затраты на оборудование, здания. В настоящее время нашли широкое применение пористые электроды, позволяющие значительно увеличить удельные поверхности, на которых осуществляются электрохимические реакции. Это позволяет повысить производительность электрохимических устройств за счет повышения плотности тока, в общем случае, путем повышения «амперной нагрузки» на единицу производственной площади. При общей оценке вклада в экономику ЭХТ следует отметить, что только стоимость хлора и щелочи, производимых электролизом, составляет около 10 % общей стоимости продукции химической промышленности. Общая мощность ХИТов, находящихся одновременно в эксплуатации, превышает мощность всех электростанций мира. С экологической точки зрения электрохимические производства характеризуются весьма токсичными продуктами (Cl2 и F2) и использованием в производстве сильно токсичных веществ: ртуть в качестве электрода, асбест в качестве диафрагменного материала и т.д. Поэтому вопросы охраны труда и техника безопасности очень важны! Электрохимический объект - это основной элемент электрохимической технологии. Объект может принадлежать к классу искусственных или естественных электрохимических объектов. Могут быть объекты, являющиеся промежуточными. Искусственные объекты – это электрохимические устройства, естественные – коррозионные процессы. К промежуточным можно отнести безэлектролизные объекты (функционирующие без внешнего тока), в которых проходящие на поверхности технических объектов самопроизвольные окислительно-восстановительные процессы. Сюда относят процессы химической металлизации, травления, оксидирования, фосфатирования, хроматирования,
пассивирования, активирования металлов и другие подобные технологические приемы. Они протекают самопроизвольно без внешнего тока, но условия оптимального протекания создаются искусственно.
В некоторых случаях герметичность ЭХУ нужна для того, чтобы электролиты не взаимодействовали с внешней средой. С помощью штуцеров 13 и 14 устройство может включаться в гидравлическую схему (постоянно или временно)
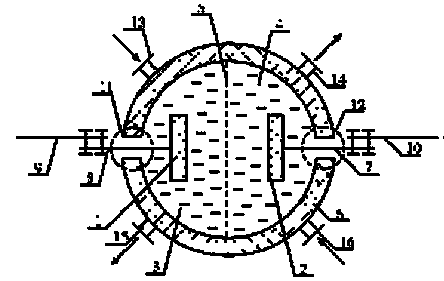 |
Рис. 1.1- Обобщенная схема электрохимического устройства-1, 2 – электроды (анод, катод); 3, 4 – электролиты, находящиеся в анодном и катодном пространствах (анод – анолит, катод - католит); 5 разделитель (сепаратор, диафрагма, мембрана), предназначен для формирования анодного и катодного пространств; 6 – корпус; 7, 8 –токоотводы от электродов (электронные проводники); 9, 10 –токоотводы от внешней цепи (элементы внешней электрической цепи); 11, 12 – узлы герметичного вывода токоотводов из корпуса электрохимического устройства.
Электроды ЭХУ могут быть твердыми, но могут быть и жидкими, например, таким является расплавленный катод в электролизере для получения алюминия или ртутный катод в хлорном электролизере. По геометрической характеристике они могут быть гладкими или пористыми. Поверхности электродов могут быть покрыты каталитическими слоями, природа которых может быть разнообразна, и определяется спецификой реакций на электроде.
Электроды могут быть газовыделяющими или газопоглощающими (газодиффузионными). Пористая структура электродов обеспечивает увеличение реакционной поверхности и увеличение интенсивности процесса в электрохимических устройствах. Важное место в электрохимических технологиях принадлежит электродам, при формировании которых используются явления гидридообразования и интеркаляции, а также электродам с полупроводниковыми, алмазными, каталитическими (в том числе, биокаталитическими) слоями.
Является в форме электрической энергии, а во втором — в форме теплоты. Для этого возьмем какое-либо химическое превращение, например Cu2+
Если эта реакция протекает как химический процесс, то она будет характеризоваться рядом особенностей.
Реакция возможна только при столкновении ее участников друг с другом. Следовательно, необходимость контакта реагирующих частиц является первой характерной особенностью химического процесса.
В момент столкновения, когда реагирующие частицы вплотную подходят друг к другу, становится возможным переход электронов от одной частицы к другой. Совершится ли такой переход в действительности, зависит от энергии реагирующих частиц и ее соотношения с энергией активации; энергия активации является функцией природы химической реакции и для ионных реакций она обычно невелика. Путь электрона при таком переходе очень мал, что является второй характерной особенностью химического процесса.
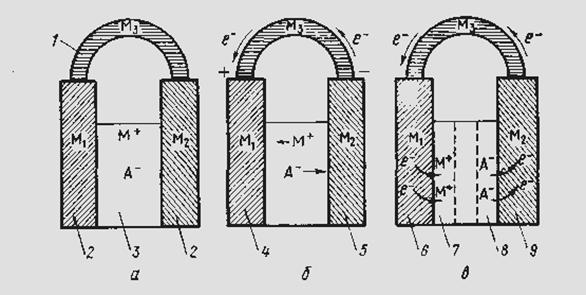
Столкновения могут происходить в любых точках реакционного объема и при любых взаимных положениях реагирующих частиц в пространстве, поэтому электронные переходы могут совершаться в любых направлениях в пространстве (рис. 1). Хаотичность, беспорядочность столкновений между реагирующими частицами и пе-направленность электронных переходов являются третьей характерной особенностью химического процесса.
В результате этих особенностей энергетические эффекты химических процессов проявляются в форме теплоты. Чтобы энергетические изменения, соответствующие химическому превращению, проявлялись в виде электрической энергии, т. е. чтобы происходил электрохимический процесс, необходимо изменить условия его протекания.
Получение или затрата электрической энергии всегда связаны с прохождением электрического тока, представляющего собой поток электронов, перемещающихся по одному и тому же пути. Условия протекания химической реакции необходимо поэтому изменить так, чтобы электронные переходы были не беспорядочны, а совершались в одном определенном направлении. Использование энергии электрического тока возможно лишь в том случае, если путь электронов велик по сравнению с размерами атомов. Таким образом, в электрохимических процессах переход электронов от одного участника реакции к другому должен совершаться по достаточно длинному пути. Однако путь электрона не может быть большим, если реагирующие частицы контактируют друг с другом. Поэтому для электрохимического процесса обязательно пространственное разделение участников реакции. Но одного только пространственного разделения недостаточно, так как оно приведет к прекращению химической реакции, а не к превращению ее в электрохимическую. Для осуществления электрохимического процесса необходимы дополнительные условия: электроны должны отрываться от ионов меди и по одному общему пути переходить к ионам железа. Этого можно достичь, заменив непосредственный контакт между участниками реакции их контактом с двумя металлическими телами, соединенными между собой металлическим проводником. Для того чтобы поток электронов был непрерывным, необходимо обеспечить прохождение электрического тока также и через реакционное пространство. Оно обычно осуществляется и участниками электрохимической реакции (если они находятся в ионизированном состоянии), и специально добавленными соединениями, обладающими в данных условиях высокой ионной проводимостью.
При электрохимической реакции прямой контакт между реагирующими частицами заменяется их контактом с соответствующим металлом. При этом реакция и связанные с ней энергетические изменения остаются теми же (независимо от того, протекает она по химическому или же электрохимическому пути), но кинетические условия могут быть различными. Энергия активации при электрохимическом механизме благодаря каталитическим свойствам металлов может быть иной, чем при гомогенном химическом механизме, кроме того, она зависит от потенциала. В электрохимических реакциях обязательно участвуют электроны, а часто и другие заряженные частицы — катионы и анионы, что составляет одну из их основных характерных особенностей. Энергия таких частиц, естественно, является функцией электрического поля, создаваемого на границе электронопроводящее тело электролит.
Отсюда следует, что и скорость электрохимической реакции зависит не только от температуры, активностей ее участников и катализатора, т. е. от тех же факторов, которые определяют скорость химической реакции, но и от потенциала на границе раздела фаз различной проводимости. Варьирование потенциала границы, при сохранении постоянными концентраций участников электрохимической реакции и температуры, позволяет в десятки, сотни и тысячи раз менять скорость реакции, а в ряде случаев и природу ее продуктов. Это делает электрохимические реакции более управляемыми, легче контролируемыми, чем химические. Электрохимические реакции можно определить как такие химические реакции, скорость которых является функцией потенциала . Поэтому электрохимические реакции отличаются от химических не только по энергетическому эффекту процесса, но также и по величине энергии активации.
Взаимное превращение химической и электрической форм энергии совершается только в электрохимических системах, поэтому их изучение составляет предмет электрохимии.
Электрохимическая система содержит следующие составные части (рис. 2).
|
|
Рис. 2. Схематическое изображение электрохимической системы:
а — равновесная электрохимическая система; б—химический источник тока; в — электрохимическая ванна; / — внешняя цепь; 2 — электроды; 3 — электролит; 4 — положительный электрод; 5 отрицательный электрод; 6 — катод; 7 — като-лит; 8 анолит; 9 — анод
1. Реагенты, а также ионизированные или способствующие ионизации реагентов вещества, обеспечивающие прохождение электрического тока; эта часть системы является ионным проводником электричества (проводник II рода) и называется электролитом.
2. Два электронопроводящих тела, контактирующие с электролитом и обеспечивающие обмен зарядами с участниками электрохимической реакции, а также передачу электронов во внешнюю цепь (см. ниже) или получение их из внешней цепи; они называются электродами. На электродах — на границе раздела двух различно проводящих фаз — происходит перенос заряда, т. е. протекают электрохимические реакции, иными словами, именно здесь локализовано взаимное превращение химической и электрической форм энергии. Электроды поэтому следует рассматривать как наиболее важную часть электрохимической системы
3. Металлический проводник (проводник I рода), соединяющий электроды и обеспечивающий прохождение тока между ними; он называется внешней цепью.
Если электролит представляет собой токопроводящий раствор одного или нескольких веществ в воде или ином растворителе, то такие системы относятся к электрохимии водных или неводных растворов; если электролитом служит расплавленная соль (или смесь расплавленных солей и оксидов), эти системы относятся к электрохимии расплавов или расплавленных сред; если межэлектродное пространство заполнено газом — к электрохимии газов. Электрохимическая система может находиться в равновесном (рис. 2, а) или неравновесном (рис. 2, б, в) состоянии.
Электрохимическая система, производящая электрическую энергию за счет протекающих в ней химических превращений, называется химическим источником тока или гальваническим элементом (рис. 2, б). Здесь электрод, посылающий электроны во внешнюю цепь, называется отрицательным электродом или отрицательным полюсом элемента. Электрод, принимающий электроны из внешней цепи, называется положительным электродом или положительным полюсом элемента.
Электрохимическая система, в которой за счет внешней электрической энергии совершаются химические превращения, называется электролизером или электролитической ванной (рис. 2, в). Электрод, принимающий электроны от участников реакции, называется анодом. Электрод, отдающий электроны участникам реакции, — катодом. Часть электролита, примыкающая к аноду, называется анолитом; примыкающая к катоду — католитом.
Поскольку потеря электронов отвечает реакции окисления, а их приобретение — реакции восстановления, то можно сказать, что анод — это электрод, на котором происходит окисление, а катод — электрод, на котором происходит восстановление. Поэтому анод одновременно является отрицательным, а катод — положительным полюсом химического источника тока.
Изложенные соображения о различии электрохимических и химических реакций и о предмете и содержании электрохимии отвечают воззрениям, сложившимся в отечественной литературе. В согласии с расширенным определением электрохимии к ней можно отнести явления, связанные с электрохимическими свойствами коллоидов, с химическими реакциями, вызванными действием света или потока радиоактивных частиц (и приводящими к возникновению разности потенциалов), с электрохимическими явлениями в животных и растительных организмах и т. п. Представляется, однако, более правильным говорить в этих случаях о коллоидной электрохимии, фотоэлектрохимии, радиоэлектрохимии, биоэлектрохимии и т. д., сохранив название собственно электрохимии для
До сих пор рассматривалась роль, которую адсорбция играет лишь непосредственно в самом процессе электролитического восстановления (или окисления). Этот фактор должен сказываться на кинетике конкурирующих процессов, т. е. на кинетике электрохимического выделения водорода (или кислорода). Присутствие адсорбированных веществ на поверхности электрода может и увеличивать и уменьшать перенапряжение водорода (или кислорода). Это, в свою очередь, будет изменять условия протекания реакции восстановления (или окисления). Такого рода представления согласуются с тем экспериментальным фактом, что реакции электроокисления или электровосстановления многих веществ часто протекают со значительным выходом по току при потенциалах, заметно больших, чем те, при которых (при той же плотности тока) происходит выделение водорода или ирииелодит выделение водорода или кислорода из растворов, не содержащих «деполяризатора». В частности, проведение синтеза Кольбе возможно именно потому, что органические соединения, адсорбируясь на платиновом электроде, отравляют его, затрудняя тем самым выделение кислорода и смещая потенциал до значения, при котором уже может начинаться окисление анионов карбоновых кислот. Адсорбция органических веществ при столь положительных и удаленных от нулевой точки металла потенциалах кажется невозможной, если не учитывать окисления поверхности. Нулевая точка окисленного металла, как это было отмечено на примере свинца, сдвинута далеко в положительную сторону по сравнению с ее значением для чистого металла.
Глава 2. Электрохимическое выделение металлов
2.1. ОБЩАЯ ХАРАКТЕРИСТИКА ПРОЦЕССОВ
Электрохимическое выделение металлов из водных растворов и соединений лежит в основе гидроэлектрометаллургических процессов, т. е. процессов извлечения металлов из руд (электроэкстракцпя) и их очистки (рафинирование) при помощи электролиза. Гидро-электрометаллургическим путем получают и очищают такие металлы, как медь, никель, цинк, кадмий, олово, свинец, серебро, золото, марганец и др. Гидроэлектрометаллургия позволяет получать технически чистые металлы и в ряде случаев вести успешную переработку бедных руд. Электрохимическое выделение металлов использутся для защиты основного металла от разрушения при помощи покрытий из более устойчивых металлов или сплавов, а также для придания изделиям красивого, декоративного вида (гальванотехника). Кроме того, выделение металлов применяется для получения копий и воспроизведения художественных предметов, изготовления лент, бесшовных труб, печатных схем и т. д. (гальванопластика). Возможность использования процесса электролиза с выделением металлов для практических нужд была открыта в 1837—1838 гг. русским академиком Б. С. Якоби.
Электролитическое выделение металлов чаще всего проводят из растворов их простых солей — сульфатов, хлоридов или нитратов. Суммарной катодной реакцией в этом случае будет разряд гидра-тироваппых металлических ионов с их последующим переходом в кристаллическую решетку образующегося на катоде осадка:
ге-== [М] + * Н2О (22.1)
Электрохимическое выделение металлов из водных растворов происходит при более отрицательном потенциале, чем равновесный потенциал соответствующего металла в данных условиях. Разность между потенциалом электрода под током (при катодном выделении металла) и соответствующим обратимым электродным потенциалом дает электродную поляризацию
А #н = * J*-*!>• (22-2)
Долю общей поляризации, не связанную с замедленностью процессов транспортировки, часто называют перенапряжением металла. Перенапряжение и здесь тесно связано с природой электродного процесса.
Поляризация при электрохимическом выделении металлов, так же как и при других электродных реакциях, зависит от плотности тока, увеличиваясь вместе с ней. Однако в данном случае характер этой зависимости часто оказывается более сложным. Даже при осаждении одного и того же металла результаты поляризационных измерений могут укладываться в зависимости от диапазона применяемых плотностей тока, состава раствора и температуры на прямые в одной из следующих систем координат:
Ti — J. -n — lgJ, —~lg/. —r-lgj'
Экспериментальное исследование кинетики катодного выделения металлов представляет собой сложную задачу, что связано с некоторыми специфическими особенностями этого процесса. В ходе электролиза поверхность катода не постоянна, а непрерывно изменяется вследствие осаждения металла. Характер роста осадка существенно зависит от природы металла и условий электролиза
Для некоторых металлов, например серебра и таллия, типично образование нитеобразных кристаллов и древовидных ответвлений, так называемых усов и дендритов. При наблюдении за развитием отдельного нитеобразного кристалла можно обнаружить изменение его сечения, если меняется приложенный ток. Часто (рис. 22.1, а) с ростом силы тока нить утолщается, а при его уменьшении становится тоньше. Поверхность, на которой происходит осаждение, как бы приспосабливается к силе тока таким образом, чтобы плотность тока, а следовательно, и линейная скорость роста кристалла не менялись. Нередко наблюдается также слоистый рост осадка, при котором кристаллический пакет перемещается с определенной скоростью по поверхности катода (рис. 22.1, б). Металл осаждается в этом случае не на всей поверхности, а лишь на склоне пакета, который, таким образом, представляет собой действительный фронт роста кристалла. При исследовании условий образования осадка на монокристалле серебра было установлено, что устойчивый рост кристалла совершается по одной или несколько спиралям. На рис. 22.2 дана типичная микрокартина спирального роста осадка серебра
h _ h _ h _ h _ .
S\ S-2 S$ S4
и — распространение осадка по поверхности катода в виде толстого пакета
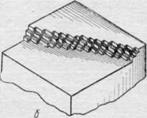
Рис. 22.1. Различные формы роста катодного осадка: а изменение сечения растущей нити с изменением плотности тока
|
|
| Рис. 22.2. Микрофотография спирального роста осадка серебра |
Своеобразие роста электролитических осадков металлов затрудняет измерение плотности тока, иными словами, скорости электрохимического процесса. Здесь необходимо различать кажущуюся плотность тока, т. е. силу тока, приходящуюся на единицу геометрической (видимой) поверхности электрода, и истинную плотность тока, равную отношению силы тока к активной поверхности, т. е. к действительной поверхности роста осадка. В процессе образования катодного осадка при неизменной кажущейся плотности тока истинная плотность тока может меняться.
Изучение кинетики электроосаждения металлов связано также с затруднениями, возникающими в связи с неустойчивостью во времени потенциала катода. Изменение потенциала и электродной поляризации вызывается не только изменением активной поверхности и истинной плотности тока, по и другими причинами. Особенно заметно изменение потенциала со временем при выделении металлов на чужеродных электродах, когда электролиз приводит к образованию новой металлической фазы, например при осаждении кадмия, меди, серебра, ртути и ряда других металлов на платиновом катоде. Впервые это явление было обнаружено еще в 1910 г. Лебланом. Изменение величины перенапряжения со временем наблюдается при выделении металла и на одноименном катоде. На рис. 22.3 приведена типичная кривая поляризация -- время, полученная при выделении серебра на серебряном катоде.
По обычной методике снятия поляризационных кривых потенциалы измеряют через некоторый промежуток времени с момента наложения нового значения тока. В результате, как это следует из характера временного изменения потенциала (рис. 22.3), при одной и той же плотности тока получаются сильно отличающиеся значения поляризации, что затрудняет сопоставление данных, полученных разными авторами.
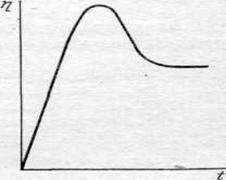
| Рис. 22.3. Изменение перенапряжения во времени, часто наблюдаемое при катодном выделении металлов |
Впервые это явление было обнаружено еще в 1910 г. Лебланом. Изменение величины перенапряжения со временем наблюдается при выделении металла и на одноименном катоде. На рис. 22.3 приведена типичная кривая поляризация - время, полученная при выделении серебра на серебряном катоде.
По обычной методике снятия поляризационных кривых потенциалы измеряют через некоторый промежуток времени с момента наложения нового значения тока. В результате, как это следует из характера временного изменения потенциала (рис. 22.3), при одной и той же плотности тока получаются сильно отличающиеся значения поляризации, что затрудняет сопоставление данных, полученных разными авторами.
Характер осадка и условия его формирования во времени при постоянной силе тока (или при заданном потенциале) зависят не только от природы металла, но и от состава раствора и присутствующих в нем примесей. Примеси поверхностно-активных веществ, а также различных окислителей (например, растворенного кислорода) влияют на кинетику электровыделения металлов. В зависимости от степени чистоты раствора и природы примесей могут меняться характер роста кристаллов, число центров кристаллизации, возникающих за единицу времени на единице поверхности катода, значение поляризации при данной плотности тока, характер ее изменения со временем и т. п. В тех случаях, когда катодный выход металла меньше единицы (электроотрицательные металлы, высокие плотности тока), возникают осложнения, связанные с изменением (обычно повышением) рН прикатодного слоя вследствие выделения водорода. Подщелачивание раствора вблизи катода благоприятствует процессам гидролиза солей металла с образованием его основных солей и гидроксидов, которые могут влиять на ход электроосаждения и включаться в катодный осадок.
2.2. ОБРАЗОВАНИЕ МОНОАТОМНЫХ СЛОЕВ МЕТАЛЛОВ ПРИ ПОТЕНЦИАЛАХ ПОЛОЖИТЕЛЬНЕЕ РАВНОВЕСНЫХ
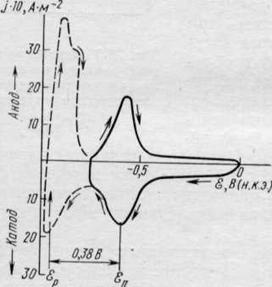
К настоящему времени можно считать доказанным, что на подложке из металла Mi, отличного по своей природе от осаждаемого металла М2, в очень многих случаях процесс осаждения начинается с образования моноатомного слоя, а возникновение и развитие кристаллических зародышей совершается уже на этом слое. Осаждение первого монослоя металла на чужеродной подложке наблюдается при потенциале более положительном, чем равновесный потенциал выделяющегося металла в данном растворе, т. е. при данной активности его ионов. В связи с этим в зарубежной литературе широко используется термин «допотенциальное осаждение» (underpotential deposition), который при буквальном его переводе на русский не передает сущности явления, вместо него поэтому используются термины «осаждение при недонапряжении» или «дофазовое осаждение». По-видимому, первым, кто наблюдал эффект дофазового осаждения металлов, был Гевеши, работы которого относятся к 1912 г. Они были затем основательно забыты, и интерес к этой проблеме возродился лишь в 60—70-х годах, и сейчас она оказалась в центре внимания и электрохимиков и физиков. Очень интересные результаты были получены с применением циклической вольтамперометрии и тонкослойных электрохимических систем. На рис. 22.4 приведена циклическая /—£-кривая, описывающая осаждение таллия на серебряном электроде. Катодный пик тока наблюдается при потенциале примерно на 0,4 В положительнее равновесного потенциала таллия в растворе выбранного состава и отвечает образованию первого монослоя. Второй подъем тока приходится на равновесный потенциал таллия и соответствует выделению компактного осадка таллия, т. е. появлению в системе новой твердой фазы — металлического таллия. Переход в анодную область позволяет наблюдать максимум тока при равновесном потенциале таллия и другой максимум, отвечающий растворению дофазового слоя. Количество таллия, осевшего в области дофазового осаждения, можно с достаточной точностью рассчитать по количеству электричества, потраченного на его растворение при потенциале первого пика. Расчеты показывают, что при дофазовом осаждении образуются обычно полные или незавершенные моноатомные металлические слои. Так как потенциал дофазового осаждения (потенциал пика) ё>П положительнее соответствующего равновесного потенциала &р, то энергия связи атомов первого монослоя с чужеродной подложкой должна быть больше, чем атомов осаждаемого металла с одноименной подложкой. Сдвиг потенциала Дс?п в положительную сторону является следствием повышенной энергии связи A<?m,2 или, с некоторым приближением, повышенной теплоты адсорбции:
|
Рис. 22.4. Циклическая вольтампер иая кривая, полученная на Ag-электроде в 2-Ю-4 М T1NO3 на фоне 0,5 М Na2SO,i; скорость развертки 20-Ю-3 В-с-1 |
Потенциал дофазового осаждения можно описать формулой Нерн-ста для электродов первого рода:
Если принять, что активность металла аи в растущем моноатомном слое отлична от единицы (как это обычно принимается для компактного металла) и зависит от степени покрытия в подложки монослоем,
Поскольку 02f2<l, потенциал монослоя в согласии с опытом оказывается положительнее равновесного потенциала того же металла в том же растворе. Из (22.5) также в согласии с опытом следует, что &П меняется с активностью ионов металла в растворе по такому же закону, как и равновесный потенциал электрода первого рода:
Соблюдение зависимости (22.6) указывает на то, что величина п отвечает заряду иона z, т. е. в образовании монослоя участвуют не ионы или частично разрядившиеся ионы, а атомы металла.
Уравнение (22.5), таким образом, удовлетворительно описывает ряд основных особенностей дофазового осаждения металлов, но не раскрывает его механизм. В этом отношении более перспективными представляются работы, в которых Д£„ сопоставляется с элект-роотрицательностями металлов, работами выхода электронов из них и т. д. По Кольбу, Прзасницкому и Геришеру, между Д£п и разностью работ выхода электрона a«'£ из металла подложки (Mi) и из осаждающегося металла (М2) существует прямо пропорциональная зависимость с наклоном, равным 0,5:
F\g]{= 0,5 Ды1'! . (22.7)
Подобная же зависимость была найдена Трасатти, ко с наклоном, равным единице:
F \ё „ = Wgl . (22.8)
Рассмотрение кривых Д£ —Да>£- с привлечением всех наиболее надежных данных по потенциалам дофазового осаждения и работам выхода показало, что коэффициент пропорциональности k лежит между 0,5 и 1, т. е.
F \(о и — k Дсо ' . /99 Q\
Независимо от величины k из уравнений (22.7) (22.9) следует, что дофазовое осаждение металлов наблюдается только в том случае, когда работа выхода электрона из металла подложки (металл Mi) больше, чем из металла монослоя (М2). Следовательно, образование монослоя сопровождается переносом электронов из него в субстрат и появлением диполей на границе раздела М, и М2, причем положительный конец диполя расположен на монослое. Свойства монослоя, его структура, во многом определяемая структурой субстрата, играют очень важную роль в процессе дальнейшего развития осадка, влияя также на адсорбционные, каталитические, коррозионные и другие характеристики металла. Дофазовое осаждение представляет поэтому не меньший интерес, чем. зароды-шеобразование, и с ним необходимо считаться при рассмотрении механизма возникновения новой металлической фазы.
Несмотря на все особенности протекания процессов электрохимического выделения металлов, создающие серьезные трудности при проведении экспериментов и при теоретической интерпретации их результатов, к настоящему времени уже накоплен значительный фактический материал и сформировались определенные взгляды на природу этих процессов. Получение достаточно достоверных опытных данных сделалось возможным благодаря развитию техники эксперимента (применение новых методов исследования, при помощи которых удается избежать осложнений, связанных с особенностями построения кристаллической решетки и изменением
потенциала во времени), разработке методики измерения поверхностен роста и, соответственно, истинной плотности тока, тщательной очистке растворов и т. п.
2.3. ВЛИЯНИЕ РАЗЛИЧНЫХ ФАКТОРОВ НА ПРОЦЕССЫ КАТОДНОГО ВЫДЕЛЕНИЯ МЕТАЛЛОВ
2.3.1. Роль природы металла
При электролизе растворов простых солей характер катодных осадков и величина электродной поляризации определяются в первую очередь природой выделяющегося металла (табл. 22.1).
Таблица 22.1. Классификация металлов по значению металлического перенапряжения при их выделении из растворов простых солей
| группы | Металлы | Перенапряжение, В | 2 Ток обмена, А-м | Средние размеры зерен осадка, м |
| I | Hg, Ag, Tl, Pb, Cd, Sn |
0—П-1Э-3 |
п-103- п-13 |
>10-5 |
| II | Bi, Cu, Zn |
п -13-2 |
/;. 13—1!. 13-1 | 10-5—Ю-6 |
| III | Co, Fe, Ni |
п-13-1 |
п-13-4—п-13-5 |
<10-7 |
Все металлы, приведенные в табл. 22.1, можно разделить на три группы. К первой из них относятся металлы, выделяющиеся из водных растворов или совсем без перенапряжения (ртуть), или с очень малым перенапряжением, не превышающим при обычных плотностях тока тысячных долей вольта (серебро, таллий, свинец, кадмий, олово). Для этой группы металлов (кроме ртути) наиболее отчетливо проявляются неустойчивость потенциала во времени, сложный характер роста катодного осадка и другие особенности, свойственные процессу катодного выделения металлов. При промышленных плотностях тока эти металлы дают грубые осадки. Токи обмена для металлов этой группы очень велики. Так, например, ток обмена между металлической ртутью и раствором ее нитрата превышает 103 А-м-2, а между серебром и раствором нитрата серебра достигает 102 А-м~2.
Висмут, медь, цинк образуют вторую, промежуточную группу. Для нее характерно металлическое перенапряжение порядка нескольких десятков милливольт, образование более тонких осадков и меньшие, чем у металлов предыдущей группы, токи обмена. Для меди, например, ток обмена в контакте с раствором сульфата меди близок к Ю-1 А-м-2.
Наибольшим металлическим перенапряжением обладают металлы третьей группы, у которых оно достигает нескольких десятых долей вольта. Эти металлы выделяются на катоде в виде плотных тонкокристаллических осадков. Токи обмена у них малы, составляя для железа и никеля в растворах их сульфатов соответственно 10-4и 10-5А-м-2.
Данные, приведенные в табл. 22.1, относятся к обычным условиям электролиза, когда металл выделяется на поликристаллической основе и дает отложения, также имеющие поликристаллическую структуру. Поверхность таких осадков образована гранями с различными кристаллографическими индексами. В зависимости от режима электроосаждения на поверхности осадка могут преобладать те или иные грани. Поэтому важно выяснить, зависит ли металлическое перенапряжение от того, на какой грани выделяется металл. Опыты с монокристаллами ряда металлов, ориентированными по отношению к раствору различными граниями, подтвердили существование подобной зависимости (см. табл. 22.2).
Таблица 22.2. Зависимость металлического перенапряжения (В• 103) от природы грани монокристалла (при 10 Ам~2, / = 25° С)
| Индекс грани | ||||
| Металл | Раствор | |||
| (100) | (ПО) |
(Ш) |
||
| РЬ |
0,5 М РЬ(СЮ4)2, |
3,0 | 3,0 | 4,4 |
|
0,5 М НС1О4 |
||||
| Sn |
0,5 М SnCl2 |
2,5 | 4,0 | _____ |
| 0,5 М НС1 | ||||
| Си |
0,5 М Си(С1О4)>, |
35 | 40 | 43 |
|
0,5 М НС1О4 |
||||
| Ni |
10 М NiCl2, |
768 | 839 | 819 |
|
0,33 М Н3ВО3 |
||||
| (рН 3,1) | ||||
Из табл. 22.1 и 22.2 следует также, что значение металлического перенапряжения в большей степени определяется природой металла, чем кристаллографической ориентацией электродной поверхности. Независимо от того, на какой из граней происходит выделение металла, перенапряжение всегда выше для никеля, чем для меди, а для меди оно всегда больше, чем для олова или свинца.
На подчиненную роль кристаллизационных факторов в явлениях перенапряжения указывают также данные по кинетике катодного выделения растворимых в ртути металлов на соответствующих амальгамах. Результаты кинетического исследования реакций обмена металлическими ионами между разбавленными амальгамами и растворами нитратов указывают на уменьшение тока обмена в следующем ряду:
TI, Pb, Cd>Cu, Zn>Ni
Характер кривых потенциал — время, полученных Гейровским методом осциллографической полярографии, показывает, что степень обратимости реакции разряда и ионизации на ртутных (точнее амальгамных) электродах уменьшается в последовательности TI, Pd, Cd, Sn, Bi, Sb, Sb, Cu
Порядок расположения металлов по степени их необратимости, а следовательно, по величине металлического перенапряжения практически не зависит от того, осаждается ли металл на твердом одноименном катоде или на разбавленной амальгаме соответствующего металла. Выделение металлов группы железа и на ртутном катоде сопровождается значительно большей поляризацией, чем у всех других металлов, приведенных в табл. 22.1. Оно протекает здесь еще менее обратимо, чем на твердых катодах. Однако эти металлы почти не способны образовывать амальгамы, и их осаждение в случае применения ртутных катодов совершается на плохо связанных между собой мелких кристаллических островках.
2.3.2. Роль состава раствора
Систематические исследования влияния состава раствора на кинетику электроосаждения металлов были начаты в 1917 г. Н. А. Из-гарышевым. Было установлено, что при катодном выделении металлов из растворов их простых солей существенное значение имеет природа аниона соли. Влияние природы аниона на перенапряжение и на характер образующихся осадков наблюдается для многих металлов, но наиболее сильно оно проявляется для металлов, выделение которых не сопровождается высокой поляризацией. Обычно перенапряжение уменьшается при переходе от одного аниона к другому в следующем порядке:
POJj-, №^, SO2-, C104->NH2S03~>Cl->Br->I-
Причем в том же направлении увеличивается тенденция к образованию более грубых, крупнокристаллических осадков. Влияние анионов вполне сравнимо с эффектами, связанными с кристаллографическими факторами. Так, например, замена перхлоратных растворов на сульфаминовые уменьшает перенапряжение при выделении свинца примерно в той же степени, как и переход от грани (111) к грани (ПО).
Присуствие в растворе, помимо ионов разряжающегося металла, «индифферентных» катионов увеличивает металлическое перенапряжение. Подобные эффекты наблюдались при выделении никеля, цинка, меди и других металлов. В водных растворах обычными «посторонними» катионами являются водородные ионы. Увеличение их концентрации приводит чаще всего к росту металлического перенапряжения. Значительное его повышение наблюдается в присутствии поверхностно-активных катионов типа тетразамещенного аммония.
Высокая чувствительность процесса электроосаждения металлов к чистоте растворов указывает на то, что присутствие не только электролитов, но и любых веществ, особенно обладающих поверхностно-активными свойствами, должно играть здесь существенную роль. Так, введение в ванну цинкования ничтожного количества желатины (порядка 0,005%) изменяет величину катодный поляризации и характер получающихся осадков (Н. А. Йзгарышев, П. С. Титов, 1917).
Введение в раствор небольших количеств молекулярных и ионных веществ — один из наиболее эффективных способов воздействия на ход процесса электроосаждения металлов. Многие, преимущественно органические, вещества способны увеличивать блеск осадков (блескообразователи), сглаживать их поверхность (выравниватели), и изменять другие свойства, например пористость, твердость, хрупкость, способность окклюдировать водород и т. д. (Кудрявцев, Матулис и др.).
Обнаруженная М. А. Лошкаревым адсорбционная поляризация проявляется в том, что при добавлении к раствору некоторых поверхностно-активных веществ (например, трибензиламина) изменяется скорость выделения металла на ртутном и на твердых катодах. Она становится, во-первых, меньше той, что наблюдалась до введения добавки, и, во-вторых, не зависящей в широкой области потенциалов от катодного потенциала. Однако после того как достигается определенный (обычно весьма отрицательный) потенциал, действие добавки прекращается. Скорость выделения начинает быстро расти, приближаясь к нормальному для этих условий значению, отвечающему предельному диффузионному току. Сопоставление результатов поляризационных измерений на ртутных катодах с электрокапиллярными кривыми и кривыми дифференциальной емкости (снятыми до и после введения добавки) показали, что потенциал, при котором прекращается действие добавки, совпадает с потенциалом ее десорбции (рис. 22.5). Действие добавки оказывается при этом специфическим. Одни и те же добавки или определенная их комбинация в разной степени тормозят разряд различных ионов на ртутном катоде. Явление адсорбционной поляризации используется для улучшения качества гальванических осадков при электролитическом получении сплавов.
Все эти данные относятся к тому случаю, когда металлы выделяются из растворов их простых солей. Если неорганические или органические добавки образуют комплексные соединения с выделяющимся металлом, то ход катодного процесса существенно меняется. Прежде всего образование комплексов в растворе смещает равновесный потенциал металла в отрицательную сторону за счет уменьшения концентрации его свободных ионов. Добавление вещества М. А (анионы которого способны давать комплексные соединения МАХ с ионами выделяемого металла Мг+) вызывает в растворе реакцию комплексообразования:
Мг+ +х А- = МА£"* , (22 10)
где (г—х)—заряд образующихся ионов. Реакции (22.10) отвечает константа комплексообразования
Обратная ей величина называется константой нестойкости комплекса
Константа нестойкости характеризует способность комплекса с диссоциации с регенерацией исходных ионов Mz+ и, таким образом, определяет их равновесную концентрацию.
В результате реакции комплексообразования определенная доля (юнов Мг+ (тем большая, чем ниже константа нестойкости) будет присутствовать в растворе в виде сложных ионов MA*""* и, следовательно, концентрация свободных ионов металла должна уменьшиться. Это уменьшение и, соответственно, сдвиг эбратимого потенциала электрода в отрицательную сторону будут тем значительнее, чем меньше констан-га нестойкости и чем выше концентрация добавки. Подбирая соответствующие комплексообразо-вателн и их концентрации, можно изменить равновесные потенциалы присутствующих в растворе попов различных металлов таким образом, чтобы обеспечить или их совместное осаждение в виде сплава, или наиболее полное разделение.
Появление комплексов в растворе сказывается не только на равновесных потенциалах металлов, но и на величине перенапряжения и на характере катодных осадков. При переходе от простых электролитов к комплексным обычно наблюдается повышение перенапряжения и уменьшение зернистости осадков; одновременно подавляется тенденция к образованию и росту дендритов. Так, серебро, которое при электролизе раствора его нитрата выделяется на катоде почти без поляризации и дает грубые, шероховатые осадки, из комплексных цианистых электролитов может быть получено в виде гладких тонкокристаллических отложений.
2.4. ПРИРОДА МЕТАЛЛИЧЕСКОГО ПЕРЕНАПРЯЖЕНИЯ
Электродная поляризация, наблюдаемая при выделении металлов, может быть связана либо с фазовыми превращениями (см. гл. 16) и представлять собой один из видов фазового перенапряжения (за-медленость образования трехмерных и двухмерных зародышей, поверхностная диффузия адатомов или аднонов), либо с замедленностью собственно электрохимической стадии (см. гл. 17) и совпадать с электрохимическим перенапряжением. При осаждении металлов существенную роль играют затруднения на стадии транспортировки, а также на стадии химического превращения (см. гл. 15), предшествующего электрохимическому акту. При рассмотрении процессов катодного выделения металлов (особенно из комплексных электролитов) необходимо поэтому всегда учитывать концентрационную поляризацию, т. е. диффузионное перенапряжение и химическое или реакционное перенапряжение. Наконец, в условиях катодного выделения металлов энергетическое состояние иона в образующемся осадке может отличаться от его состояния в нормальной кристаллической решетке данного металла и, как правило, отвечать более высокому уровню энергии. Переход из такого мета-стабильного состояния к обычному также может обусловливать появление особого вида фазового (кристаллизационного) перенапряжения.
Преобладание того или иного вида перенапряжения определяется природой металла, составом раствора, плотностью тока, температурой электролита. При обычных температурах и при использовании простых, некомплексных электролитов перенапряжение изменяется с природой металлов, как это показано в табл. 22.1. Опытные данные указывают на то, что выделение металлов, стоящих в начале ряда (Hg, Ag, Tl, Pb, Cd, Sn), сопровождается лишь незначительной поляризацией, связанной главным образом с замедленностью возникновения и развития новой фазы. Замедленность электрохимической стадии не играет здесь существенной роли. В электрохимической литературе эти металлы, для которых характерно фазовое перенапряжение, называются часто нормальными металлами. Напротив, при выделении металлов, стоящих в конце ряда табл. 22.1 (металлы группы железа), наблюдается высокая поляризация; обусловленная преимущественно замедленностью электрохимической стадии. Эти металлы, для которых характерно электрохимическое перенапряжение, называются инертными металлами. Промежуточное положение и по величине поляризации, и по природе перенапряжения (здесь наиболее вероятно наложение нескольких видов перенапряжения) занимают такие металлы, как Bi, Си и Zn.
Это различие в величине и механизме перенапряжения обусловливает, согласно Фольмеру, различный характер осадков, в виде которых нормальные и инертные металлы выделяются па катоде. Все факторы, вызывающие торможение акта разряда, должны, с этой точки зрения, уменьшать относительную роль кристаллизационных явлений и приводить к получению равномерных мелкозернистых осадков. Увеличение торможения достигается или переводом простых ионов в более прочные комплексы, или при помощи добавок поверхностно-активных веществ (если их адсорбция больше всего сказывается на акте разряда). Изменение структуры осадков, наблюдаемое при переходе от простых электролитов к цианистым, а также характер электроосаждения в условиях адсорбционной поляризации подтверждают эту точку зрения.
2.5. ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ ВЕЛИЧИНУ ПОЛЯРИЗАЦИИ ПРИ КАТОДНОМ ВЫДЕЛЕНИИ РАЗЛИЧНЫХ МЕТАЛЛОВ
2.5.1. Энергия иона в металле и его состояние в растворе
До сих пор остается недостаточно ясным, почему существует такое большое различие в величине и природе металлического перенапряжения для нормальных и инертных металлов и с какими свойствами металлов (или растворов) оно связано. Была сделана попытка объяснить эти явления различным соотношением между прочностью связи ионов в растворе и в кристаллической решетке нормальных и инертных металлов. Подобное предположение эквивалентно допущению, что в разряде участвуют ионы в той форме, в какой они присутствуют в растворе, и что разряд переводит ион непосредственно в его конечное положение в решетке металла.
При таком допущении энергия активации должна быть функцией энер'гии гидратации ионов и работы их выхода из металла, возрастая с увеличением разности между ними. На основании этого следовало бы ожидать, что для инертных металлов энергия гидратации больше, а работа выхода меньше, чем для нормальных металлов. Однако имеющиеся данные (см. табл. 22.3) не подтверждают такого предположения: так, для цинка и никеля значения энергии гидратации и работы выхода почти одинаковы, но цинк выделяется со значительно меньшим перенапряжением, чем никель. Это отнюдь не означает, что прочность ионов в растворе и в металле не играет никакой роли, ее просто нельзя учесть подобным примитивным способом.
Недостаточность такой упрощенной картины следует и из более общих соображений. Стандартные электродные потенциалы изменяются параллельно с изменением разности между химической' энергией гидратации ионов в растворе и работой удаления ионов из кристаллической решетки. Поэтому казалось бы, что металлическое перенапряжение должно изменяться в такой же последовательности, как и ряд стандартных электродных потенциалов. Опыт противоречит этому выводу. Так, например, цинк, стандартный потенциал которого равен —0,76 В, выделяется с меньшим перенапряжением, чем железо со стандартным потенциалом —0,44 В. В то же время перенапряжение при выделении цинка примерно такое же, как и при выделении меди — электроположительного металла (<r ^U2+ ( Cu = + 0,34В).
Таблица 22.3. Энергия гидратации и работы выхода ионов для ряда металлов (в кДжмоль"1)
| Свойства | Нормальные | и переходные металлы | Инертные металлы | |||||
| Ag + | Cd2+ |
Pb2+ |
CU2 + |
Zn2+ | Со2+ |
Fe2+ |
N,2+ | |
|
v+ |
477 498 | 18)4 18)8 | 1498 1553 | 2082 2240 | 2)3) 1926 | 2024 1712 | 1920 180) | 2)74 1976 |
Допущение о том, что выделение металла совершается не как последовательная стадийная реакция, а как один элементарный акт, противоречит всем результатам, полученным при изучении кинетики различных электрохимических процессов. Например, для реакции катодного выделения водорода принятие такого допущения привело бы к не отвечающему действительности выводу о независимости водородного перенапряжения от природы металла. Чтобы объяснить связь, существующую между металлическим перенапряжением и природой металла, а также характер влияния состава раствора на величину перенапряжения, необходимо принимать во внимание не только начальное и конечное состояния металлических ионов, но и природу элементарных актов. При этом следует учитывать состояние и свойства реагирующих частиц на разных стадиях суммарного процесса.
Многие исследователи пытались усовершенствовать теорию электровыделения металлов, привлекая представления об электронном строении их ионов. Одна из таких попыток принадлежит Лайон-су (1954). По Лайонсу, величина металлического перенапряжения зависит от характера электронных структур разряжающихся ионов и выделившегося на катоде металла. При этом перенапряжение будет особенно большим в двух случаях. Во-первых, если аквакомп-лексы (или иные комплексы) образованы ионами за счет электронов, находящихся на внутренних орбитах (внутриорбитальные комплексы), благодаря чему создаются наиболее прочные связи ионов в растворе. Во-вторых, если велика разница в электронных структурах иона и металла; в этом случае требуется значительная энергия активации для их перестройки в процессе разряда. Разряжающиеся ионы имеют обычно иную структуру, чем ионы, присутствующие в растворе. Это обстоятельство связано с тем, что при адсорбции на электроде происходит частичная диссоциация простого гидратированного или комплексного иона. Освобождающиеся связи удерживают ион на поверхности электрода, причем до момента разряда идет дальнейшая перестройка его электронной структуры в направлении, сближающем ее со структурой иона в металле. Далее следует разряд или с полной дегидратацией иона, или с распадом комплекса и внедрением атома металла в кристаллическую решетку.
Все металлы, приведенные в табл. 22.1, дают, по Лайонсу, впеш-неорбитальные аквакомплексы, т. е. комплексы, образованные с участием электронов, находящихся на внешних орбитах. Это делает возможным их выделение из водных растворов в отличие от таких металлов, как титан, цирконий и др., ионы которых в растворе присутствуют в виде внутриорбитальных комплексов. Высокое перенапряжение металлов группы железа объясняется тем, что электронная структура их разряжающихся акваионов значительно отличается от структуры соответствующего металла. Электронные структуры нормальных металлов в кристалле и в водных комплексах близки, и поэтому они обладают низким перенапряжением.
Взгляды Лайонса в какой-то мере отражают некоторые особенности, свойственные катодному выделению металлов. Несомненно, что известная роль в этих процессах должна быть отведена специфике электронного строения ионов. Однако этого недостаточно для полного выяснения природы процессов электроосаждения металлов. Прежде всего это связано с отсустствием надежных данных о строении ионов в растворе и на поверхности электрода, что заставляет прибегать к помощи гипотетических структур. Далее, теория Лайонса даже при использовании подобных структур не в состоянии объяснить некоторые полученные экспериментально закономерности, относящиеся, например, к выделению металлов группы платины. В его теории не учитывается влияние потенциала электрода и строения двойного электрического слоя на процесс электроосаждения металла. Наконец, она не может объяснить той роли, какую играют в этом процессе состав раствора и особенно поверхностно-активные вещества. Дальнейшее развитие представлений о роли структуры разряжающихся металлических ионов при электроосаждении металлов было дано Вылчеком (1957).
2.5.2. Активность поверхности катода в процессе осаждения металлов
Согласно другой точке зрения природа и величина металлического перенапряжения являются функцией состояния поверхности катода, которое может быть неодинаковым для разных металлов. Одна из причин этого различия связана с возможностью выделения
водорода и его влиянием на ход осаждения металлов. Известно, что электролитические осадки железа, никеля и кобальта всегда содержат заметное количество водорода. Включения водорода можно рассматривать как одну из возможных причин искажения кристаллической решетки осадков этих металлов, появления в них внутренних натяжений, хрупкости и т. п. В меньших количествах водород присутствует в осадках меди и цинка. Его практически не удается обнаружить в электролитически осажденных кадмии или свинце. Из этого следует, что металлическое перенапряжение увеличивается параллельно с количеством водорода, включенного в осадок металла, т. е. водород, по-видимому, затрудняет процесс катодного выделения металла. Предполагалось, что водород выступает здесь в роли отрицательного катализатора, тормозя разряд за счет создания поверхностной пленки или образования гидридов металлов.
В связи с влиянием водорода на кинетику электроосаждения металлов важно выяснить причины, которые приводят к различному содержанию водорода в разных металлах и, следовательно, изменяют величину его тормозящего действия при переходе от одного металла к другому. Оказалось, что в общем случае нет прямой зависимости между долей общего тока, расходуемой на выделение водорода, и его содержанием в металле. Так, например, при электроосаждении цинка выход по току водорода обычно больше, чем в случае железа; тем не менее содержание водорода в нем всегда меньше и перенапряжение при его выделении ниже. Расположение металлов в порядке увеличения перенапряжения при их выделении примерно соответствует их расположению по степени уменьшения водородного перенапряжения. Однако большее значение должна иметь не величина перенапряжения водорода, а механизм его выделения на данном металле (Л. И. Антропов, 1952). Включение водорода в осадок металла тем вероятнее, чем медленнее протекает удаление адсорбированных водородных атомов с поверхности металла. Наибольшие количества водорода обнаруживаются поэтому в катодных осадках металлов группы железа, где стадия рекомбинации водородных атомов протекает медленно.
Присутствие адсорбированного или окклюдированного водорода все-таки не может считаться главным фактором, определяющим специфику катодного выделения металлов.
Причину различия в значениях металлического перенапряжения и в характере катодных осадков можно было бы искать в неодинаковой склонности металлов к пассивированию и в их разной адсорбционной способности. Появлениен на поверхности растущего осадка посторонних.веществ затрудняет и разряд металлических ионов, и их внедрение в кристаллическую решетку. Этот тормозящий эффект должен быть тем заметнее, чем легче пассивируется данный металл. Пассивирующими агентами могут быть растворенный кислород, примеси органических соединений и каталитических ядов, некоторые посторонние ионы, не участвующие непосредственно в электродной реакции, и другие вещества. Особое положение металлов группы железа, в частности их высокое металлическое перенапряжение, объясняется с этой точки зрения тем, что они в большей мере, чем другие металлы, склонны к пассивированию. Однако и этот фактор не является, по-видимому, решающим и не обусловливает порядка расположения металлов по величине их перенапряжения. Даже после самой тщательной очистки растворов от примесей и удаления из них кислорода разница в значениях металлического перенапряжения между инертными и нормальными металлами остается большой. Точно так же свинец, который пассивируется несравненно легче, чем цинк, выделяется при более низком перенапряжении.
2.5.3. Заряд поверхности металла в условиях его катодного осаждения
Протекание адсорбционных явлений на границе металл — электролит, а следовательно, В степень их влияния на процессы, идущие на этой границе, во многом зависит от потенциала, или точнее, от заряда металла.
Ранее считалось, как само собой разумеющееся, что поверхность катода всегда отрицательна, причем тем более отрицательна, чем менее электроположителен электродный металл. Эта точка зрения, сохранившая известное распространение и в настоящее время, ошибочна. Заряд поверхности металла не определяется ни той ролью, какую металл играет в электрохимическом процессе (т. е. является ли он катодом или анодом), ни его электродным потенциалом в данных условиях. Заряд поверхности электрода можно оценить, если воспользоваться предложенной Л. И. Антроповым приведенной, или ср-шкалой потенциалов. Потенциал электрода в ф-шкале представляет собой разность между его потенциалом в данных конкретных условиях (например, в процессе электроосаждения металла) и соответствующей нулевой точкой. Потенциал электрода в приведенной шкале служит мерой заряда поверхности и позволяет предвидеть, адсорбция каких именно ионов будет наиболее вероятной в данных условиях. Это положение можно проиллюстрировать на примере катодного выделения никеля, цинка, кадмия и свинца из растворов их простых солей. Все эти металлы выделяются при отрицательных потенциалах (по водородной шкале), которые в обычных режимах электролиза имеют следующие значения: —0,80 В (№), —0,80 В (Zn), —0,45 В (Cd) и —0,15 В (РЬ). Их потенциалы в приведенной шкале, т. е. заряды, можно оценить, воспользовавшись данными о нулевых точках этих металлов (см. табл. 11.6):
?М, ==-0,83 —( —0,2) = -0,6В;
<PZn = - 0,80 — (- 0,5) = - 0,3 В;
?Cd = - 0,45- ( - 0,7) = + 0,25 В;
9РЬ = — 0,15 — (-0,7) ==+0,55 В.
Из этих значений ф-потенциалов следует, что в условиях электроосаждения никель имеет наиболее отрицательный заряд, за ним следует цинк, который также заряжен отрицательно, в то время как кадмий и свинец заряжены положительно. В ходе электровыделения на поверхности осадков никеля и цинка должны , адсорбироваться преимущественно катионы, а на поверхности осадков кадмия и свинца — главным образом анионы. Эти выводы, строго говоря, справедливы течением концентрации водородных ионов и при введении поверхностно-активных катионов, резкое увеличение перенапряжения водорода при переходе от положительно заряженной поверхности металла к отрицательно заряженной и т. д. Все нормальные металлы (Hg, Ag, Tl, Pb, Cd), при выделении которых перенапряжение ничтожно мало, заряжены положительно по отношению к растворам их простых солей (ф>0), а все металлы, выделение которых сопровождается высоким перенапряжением (металлы группы железа), — отрицательно (ф<0). Поэтому в явлениях электроосаждения металлов необходимо учитывать заряд поверхности электрода, хотя он и не определяет всех особенностей этих процессов. Так, например, неясным остается факт существования большой разницы в значениях перенапряжения при выделении цинка и никеля — металлов, обладающих в условиях равновесия приблизительно одинаковым отрицательным зарядом поверхности. Точно так же выделение меди, судя по ее ф-потенциалу, должно бы происходить с такой же легкостью, как и выделение кадмия или свинца, тогда как данные опыта противоречат этому.
2.5.4. Другие возможные причины появления металлического перенапряжения
Невозможность объяснить все кинетические особенности электрохимического выделения металлов с какой-либо одной общей точки зрения заставляет искать новые пути истолкования этих процессов и прибегать к предположениям частного характера. Так, например, существует мнение, что перенапряжение при выделении металлов связано с числом электронов, участвующих в элементарном акте разряда (Гейровский). При этом предполагают, что одно электронные реакции протекают практически без торможения.
В тех случаях, когда только один электрон участвует в акте разряда (или когда процесс можно разбить на ряд последовательных одноэлектронных стадий), перенапряжение должно быть низким. Если в разряде ионов металла участвуют одновременно два электрона, то следует ожидать появления высокого металлического перенапряжения. Согласно этим представлениям низкое перенапряжение, наблюдаемое при выделении таллия и серебра, связано с тем, что реакция восстановления требует участия одного электрона:
Ag+ + е- = [Ag]
Невысокое металлическое перенапряжение, свойственное меди и цинку, объясняют возможностью протекания разряда в две одно электродные стадии:
CU2+ +е~ = Си+ Cu+ + e~ = [Си]
е~ = Zn+
Zn+ ■+• е~ = [Zn]
Для металлов группы железа разряд совершается при одновременном присоединении двух электронов чем обусловливаются малая скорость этого процесса (вероятность одновременного присоединения двух электронов низка) и высокое перенапряжение.
2е~ = [Fe]
Однако уже давно было замечено, что скорость электроосаждения, а также электрорастворения металлов группы железа зависит от рН раствора и присутствия в нем примесей. Р. X. Бурштейн, Б. Н. Кабанов и А. Н. Фрумкин (1947) высказали предположение о непосредственном участии ионов ОН~ в кинетике этих процессов. По их мнению, ионы ОН~ играют роль своеобразных катализаторов. Механизм реакций катодного осаждения и анодного растворения железа, кобальта и никеля с образованием промежуточных частиц типа FeOH, FeOH+ или Fe-FeOH+ рассматривался затем Хейслером, Бокрисом, Фишером и Лоренцом и многими другими авторами. Было предложено несколько схем, объясняющих такие экспериментальные данные, как характер зависимости скорости реакции от рН, небольшой наклон тафслсвской прямой в чистых растворах серной кислоты, его повышение при переходе к растворам соляной кислоты и при введении добавок поверхностно-активных веществ и т. д. В качестве иллюстрации можно привести схему Бокриса
Fe2+ + ОН- = FeOH+ FeOH+ + e~ = FeOH
— [Fe] + O
СМ ворд док – глюк
Лаборатория электрокатализа и коррозии (зав. лабораторией — д.х.н., профессор О.А.Петрий)
В лаборатории изучается широкий круг электрокаталитических и коррозионных явлений на металлах, сплавах, оксидах и различных композиционных материалах в водных и апротонных средах. В основе подхода к этим исследованиям лежит экспериментальное и теоретическое рассмотрение процессов на микроскопическом уровне, поэтому наряду с электрохимическими методами используются и совершенствуются применительно к новым объектам и задачам методы сканирующей туннельной микроскопии и спектроскопии, эллипсометрии, а также комплекс физико-химических методов структурного анализа материалов. Разрабатываются нетрадиционные способы получения наноструктур и многофазных композиций, основанные на процессах анодной и катодной электрокристаллизации. Развиваются новые подходы к молекулярному дизайну поверхностей электродов-катализаторов.
В теоретическом плане важнейшими задачами лаборатории являются развитие теории электрокатализа, представлений о механизмах электрокаталитических процессов, а также установление закономерностей элементарного акта переноса электрона в гетерогенных системах, в первую очередь экспериментальная проверка квантово-механической теории элементарного акта с использованием нетрадиционных модельных реакций. Развиваются представления о влиянии заряда электрода на различные кинетические параметры и рассматриваются на микроскопическом уровне эффекты двойного электрического слоя в электрохимической кинетике. На основе экспериментальных исследований электродов с обновляемой поверхностью и компьютерного моделирования развиваются представления о реконструкции многокомпонентных поверхностей и о процессах поверхностной диффузии.
С целью разработки никель-металлогидридных аккумуляторов проводится широкий поиск материалов АВ5- и АВ2-типов, обратимо сорбирующих водород в электрохимических условиях.
С 1997 г. лаборатория входит вместе с Институтом физической химии РАН и кафедрами физической и коллоидной химии в состав Учебно-научного центра «Нанохимия».
Последние публикации
1. O.A.Petrii, G.A.Tsirlina, Electrochemistry of Oxide High-Temperature Superconductors, in «Adv. Electrochem. Sci. Eng.»/Ed. R.C.Alkire, H.Gerisher, D.M.Kolb and C.W.Tobias, 1997, V.5, P.61-123.
2. R.R.Nazmutdinov, G.A.Tsirlina, Yu.I.Kharkats, O.A.Petrii, M.Probst, Activation Energy of Electron Transfer between a Metal Electrode and Reagents of Nonspherical Form and Complicated Charge Distribution. Cr(EDTA) Complexes//J.Phys. Chem, 1998, V.102, P. ??-??.
3. V.A.Safonov, M.A.Choba, Yu.D.Seropegin, Peculiarities of the Electrical Double Layer Structure on Renewed Electrodes of Eutectic Alloys//Electrochim. Acta, 1997, V.42, P.1907–1914.
Литература:
Основная:
1. Дамаскин Б.Б., ПетрийО.А., Основы теоретической электрохимии,
М., Высшая школа, 1978
2. Дамаскин Б.Б. , О.А. Петрий Введение в электрохимическую кинетику, 1986 г.
3. Антропов Л.И., Теоретическая электрохимия , М.,Высшая школа, 1975 г.
4. Скорчелетти В.В., Теоретическая электрохимия ,М.. Высшая школа, 1974г.
5. Ротинян А.Л., Тихонов К.И. ,Шонина И.А. Теоретическая электрохимия, Высшая школа 1980 г.
6. Попова С.С. Анодное растворение металлов и пассивация в кислых окислительных средах.- Саратов ,Изд-во СГУ, 1984 г.
7. Кукоз Ф.И. Сборник задач по теоретической электрохимии.
8. Попова С.С. Теоретическая электрохимия. Сборник задач.
9. Левин А.И., Помосов А.В. Лабораторный практикум по теоретической электрохимии.- М: Металлургия, 1979 г.
10. Дамаскин Б.Б.Практикум по электрохимии-М: Высшая школа, 1991г.
Дополнительная
1. Феттер К., Электрохимическая кинетика, М.,Л., «Химия», 1967г.
2. Фрумкин А.Н., БагоцкийВ. С., ИофаЗ.А., Кабанов Б.Н., Кинетика электродных процессов , изд-во МГУ, 1952г.
3. Дамаскин Б.Б., Петрий О.А. , Батраков В.В., Адсорбция органических соединений на электродах. М.-Л., «Наука», 1968г.
4. Дамаскин Б.Б., Принципы современных методов изучения электорохимических реакций, Изд-во МГУ ,1965г.
5. Делахей П., Новые приборы и методы в электрохимии .,ИЛ, 1957г.
6. Делахей П., Двойной слой и кинетика электродных процессов ,»Мир», 1967г.
7. Плесков Ю.В. , Фидиновский В.Ю., Вращающийся дисковый электрод, М-Л., «Наука», 1972г.
8. Измайлов Н.А., Электрохимия растворов, М-Л.,»Химия»,1966г.
9. Корыта И., Дворжак И.,Богачкова В., Электрохимия ,»Мир», 1977г.
10. Кравцов В.И. ,Электродные процессы в растворах комплексов металлов , Изд-во ЛГУ; 1969г.
11. Мишенко К.П., Полторацкий Г.М.,Термодинамика и строение водных и неводных растворов элекролитов. М-Л., «Химия» 1976г.,1984г.
12. Латимер В., Окислительные состояния элементов, ИЛ, 1954г.
13. Методы измерения в электрохимии, т.1 и 2, Под ред.Э.Егера и А.Залкинда «Мир», 1974г.
14. Использование наглядных пособий, ТСО, вычислительной техники.
© 2010 Интернет База Рефератов