
Рефераты по сексологии
Рефераты по информатике программированию
Рефераты по биологии
Рефераты по экономике
Рефераты по москвоведению
Рефераты по экологии
Краткое содержание произведений
Рефераты по физкультуре и спорту
Топики по английскому языку
Рефераты по математике
Рефераты по музыке
Остальные рефераты
Рефераты по авиации и космонавтике
Рефераты по административному праву
Рефераты по безопасности жизнедеятельности
Рефераты по арбитражному процессу
Рефераты по архитектуре
Рефераты по астрономии
Рефераты по банковскому делу
Рефераты по биржевому делу
Рефераты по ботанике и сельскому хозяйству
Рефераты по бухгалтерскому учету и аудиту
Рефераты по валютным отношениям
Рефераты по ветеринарии
Рефераты для военной кафедры
Рефераты по географии
Рефераты по геодезии
Рефераты по геологии
Рефераты по геополитике
Рефераты по государству и праву
Рефераты по гражданскому праву и процессу
Рефераты по делопроизводству
Рефераты по кредитованию
Рефераты по естествознанию
Рефераты по истории техники
Рефераты по журналистике
Рефераты по зоологии
Рефераты по инвестициям
Рефераты по информатике
Исторические личности
Рефераты по кибернетике
Рефераты по коммуникации и связи
Курсовая работа: Химический состав снежного покрова Гомельского района в 2001-2003 гг.
Курсовая работа: Химический состав снежного покрова Гомельского района в 2001-2003 гг.
Курсовая работа
"Химический состав снежного покрова Гомельского района в 2001–2003 гг."
Введение
Проблема выпадения кислотных осадков, возникшая в середине прошлого столетия, проявилась в ряде регионов мира такими негативными последствиями, как закисление поверхностных вод с последующим снижением численности популяций рыб, закисление почв, сокращение продуктивности лесов, коррозия промышленных материалов, разрушение культурных ценностей и ухудшение прозрачности атмосферы. Это стимулировало развитие комплексных исследований в рамках национальных и международных проектов, результаты которых отражены в ряде обзоров и монографий [1–3].
Основными техногенными предшественниками кислотных выпадений являются оксиды серы и азота в газовых выбросах энергетики, транспорта, ряда отраслей промышленности. Локальные выбросы летучих кислот (соляной, плавиковой и др.) или продуктов, трансформирующихся в атмосфере в кислоты (например, муравьиную), вносят дополнительный вклад в повышение естественной кислотности. Из катионов, нейтрализующих сумму анионов в ионном составе атмосферных аэрозолей и осадков, только аммоний образуется из газовой фазы, а другие (Ca2+Mg2+Na+K+) должны поступить с наземной или водной поверхности в составе солей твердых частиц. Таким образом, в ионном балансе атмосферных аэрозолей и осадков (в эквивалентах основных ионов):
[H+] = ([HCO3-]+[SO42-]+[NO3-]+[Cl-]+[F-])+([NH4+] [Na+] – [K+] – [Ca2+] – [Mg2+])
избыточное количество Н+-ионов может быть следствием как избытка газообразных предшественников анионов, так и дефицита катионов терригенного или морского происхождения. Расчетное значение [H+] для осадков при фоновом уровне СО2, SO2, NH3 в атмосферном воздухе близко к 1,6×10-6 моль×кг-1, что соответствует рН=5,8 [2,6].
В регионах с выраженными кислотными выпадениями среднегодовые значения рН осадков достигают 4,1–4,4, а в отдельных дождях – до 2,3 [1].
Следует отметить, что пониженные значения рН дождей (4,5 и ниже) регистрируются и в фоновых регионах, удаленных как от техногенных, так и от природных (вулканы) источников газовых выбросов. Расчеты показывают, что такой уровень кислотности может достигаться при отсутствии в чистой атмосфере над океанами аммиака и карбоната кальция.
В геохимически чистых зонах основной вклад в кислотность осадков вносит диоксид углерода (около 80%); суммарный вклад серной и азотной кислот составляет около 10%. В высокоиндустриальных на диоксид углерода приходится не более 4%, а на серную, азотную и соляную кислоты – 95% [3]. В некоторых районах, например на юго-западе США, определяющий вклад в закисление вносят соединения азота (более половины), а на северо-востоке – соединения серы, что связано с высокой относительной эмиссией этих веществ в данных районах. [1]. В России за последние 30 лет также произошло увеличение минерализации атмосферных осадков. Кислотные дожди выпадают в районе крупных промышленных центров (Северо-западный округ, Московская область, Урал, Поволжье). По данным [1,2,6], концентрация сульфат-иона в атмосферных осадках Европейской России составляла от 5–10 мг/л до 25–30 мг/л, хлорида – 1–11 мг/л.
Крупные промышленные центры региона можно считать постоянно действующими источниками кислотообразующих поллютантов, формирующими основную антропогенную нагрузку на пригородные экосистемы и определяющими состав атмосферных аэрозолей, подверженный трансграничному переносу. Активность таких источников наиболее четко выявляется при исследовании состава атмосферных выпадений города и его ближайшего пригорода.
Целью настоящей работы являлось оценка возможности проявления проблемы кислотных выпадений на территории г. Гомеля и ближайшего пригорода. Такая оценка основана на обобщении экспериментальных данных (рН и химический состав снеговых вод), полученных 2001–2003 гг.
Отбор проб атмосферных осадков выполнялся: 4 марта 2001 г. (29 проб), 30 декабря 2001 г. (25 проб) и 19 января 2003 г. (29 проб) в пригороде г. Гомеля вдоль основных радиально расходящихся автотрасс на одних и тех же площадках, расположенных на открытых пространствах за пределами влияния транспорта. Расстояние от точек отбора проб до городской черты не превышало 15–17 км.
Расположение мест отбора проб снега показано на рисунке 1. Каждой площадке был присвоен порядковый номер. Площадки 1–5 расположены вдоль дороги Гомель-Калинковичи (западное направление), площадки 6–9 – вдоль шоссе Гомель-Минск (северо-западное направление), 11–15 площадки располагались в северном направлении (Гомель Могилев), площадки 16–19 расположены по направлению Гомель – Ветка (северо-восточное), 20–24 площадки – вдоль дороги Гомель – Кленки (восточное направление), площадки 25–29 – в южном направлении (шоссе Гомель – Чернигов).
Пробы снега отбирали по стандартной методике [5] после окончания снегопада пластмассовым пробоотборником на полную толщину снегового покрова. Образцы помещали в полиэтиленовые емкости для оттаивания при комнатной температуре. Кислотность проб снега определяли при помощи рН-метра – милливольтметра рН‑150М, на следующие сутки после отбора, после доведения температуры снеговой воды до комнатной. Концентрацию анионов – SO42-, Cl-, NO3-, NO2-, F-, РО43- и катионов – NH4+, Na+, K+, Ca2+, Mg2+ – определяли с использованием системы капиллярного электрофореза «Капель‑103Р» по стандартной методике. При различных диапазонах измерений данных анионов и катионов погрешность составляет от 10 до 20%. Концентрацию гидрокарбонат-иона определяли методом обратного титрования избытка соляной кислоты раствором тетробората натрия. По метрологическим результатам исследования, при определении массовой концентрации гидрокарбонат-ионов в пробах атмосферных осадков в диапазоне 0–50 мг/дм3 суммарная погрешность не превышает 15% [5].
В пробах, отобранных в марте 2001 года, определяли хлорид, сульфат, нитрат, калий, натрий, кальций-ионы, ион-аммония, а также рН снеговых вод. В пробах декабря 2001 г. и пробах января 2003 г. дополнительно определяли магний, гидрокарбонат, нитрит и фосфат-ионы.
Результаты и обсуждениеВ отличие от химически чистой воды атмосферные осадки в естественных условиях всегда содержат различные примеси, влияющие на рН. Благодаря наличию в атмосфере углекислого газа рН даже очень чистых осадков бывает близким к 5,6. В незагрязненной атмосфере могут присутствовать кислотообразующие вещества естественного происхождения, вследствие чего за нижний предел естественного закисления принята величина рН=5,5. Во всяком случае, рН>5,8 атмосферных осадков свидетельствует не о закислении, а о защелачивании.
Следует отметить, что осадки вымывают из атмосферы как кислотные, так и щелочные примеси, поэтому в случае их соизмеримого количества происходит нейтрализация осадков уже на момент их выпадения, и значения рН становятся равными 5,2–5,8. В результате имеет место существенная минерализация осадков при значениях рН, близких к нейтральным.
Результаты определения рН отобранных проб снега приведены в таблице 1, в таблице 2 – результаты статистической обработки полученных данных по направлениям отбора.
Таблица 1. Значения рН снеговых вод по отдельной стационарной площадке
|
Номер пробы |
Направление | Дата отбора | ||
| 4 марта 2001 г. | 30 декабря 2001 г. | 19 января 2003 г. | ||
| 1 | Западное | 5,85 | 5,90 | 5,70 |
| 2 | 6,05 | 5,82 | 5,48 | |
| 3 | 5,85 | 5,80 | 5,52 | |
| 4 | 5,75 | 5,57 | 5,45 | |
| 5 | 6,05 | 5,91 | 5,87 | |
| 6 | Северо-западное | 6,65 | 5,60 | 6,02 |
| 7 | 6,0 | 5,62 | 5,72 | |
| 8 | 6,65 | 5,40 | 5,42 | |
| 9 | 5,80 | 5,67 | 6,15 | |
| 10 | 6,25 | 6,10 | 5,98 | |
| 11 | Северное | 5,90 | 5,87 | 6,11 |
| 12 | 6,00 | 7,05 | 6,25 | |
| 13 | 5,85 | 5,99 | 6,30 | |
| 14 | 6,00 | 7,15 | 6,18 | |
| 15 | 5,85 | 5,92 | 5,98 | |
| 16 | Северо-восточное | 6,25 | – | 6,22 |
| 17 | 6,05 | – | 5,62 | |
| 18 | 6,40 | – | 6,10 | |
| 19 | 6,00 | – | 5,72 | |
| 20 | Восточное | 5,90 | 5,87 | 5,55 |
| 21 | 5,95 | 5,71 | 5,58 | |
| 22 | 6,00 | 6,05 | 5,85 | |
| 23 | 5,80 | 5,70 | 5,68 | |
| 24 | 6,00 | 5,25 | 5,84 | |
| 25 | Южное | 5,75 | 5,84 | 5,55 |
| 26 | 6,00 | 6,10 | 5,50 | |
| 27 | 5,75 | 5,78 | 5,81 | |
| 28 | 5,80 | 5,38 | 5,72 | |
| 29 | 6,00 | 5,66 | 5,84 | |
Как видно из представленных данных, не обнаружено существенных отличий величин рН снега как в зависимости от удаленности точек отбора от города, так и от направлений розы ветров.
По результатам проведенных исследований можно заключить, что имеет место тенденция возрастания кислотности осадков. Так, все пробы 1 отбора имели слабощелочную реакцию, т.е. рН>5,6; из проб 2 отбора – 3 пробы являлись слабокислотными (рН<5,5), 2 пробы имели характеристики чистых осадков (рН=5,5–5,6) и 20 проб – слабощелочными (рН>5,6); для проб 3 отбора эти значения составляли 3,5,21 соответственно. Для западного, восточного и южного направлений отмечены наименьшие значения рН осадков. В тоже время, для северо-западного, северного и северо-восточного – более характерны условно щелочные осадки.
Таблица 2. Статистика рН осадков по направлениям отбора проб
| Направление |
Период отбора |
Среднее | Медиана | Min | Max | 25% квантиль | 75% квантиль |
| Западное | 1 | 5,91±0,06 | 5,85 | 5,75 | 6,05 | 5,85 | 6,05 |
| 2 | 5,80±0,06 | 5,82 | 5,57 | 5,91 | 5,80 | 5,90 | |
| 3 | 5,60±0,06 | 5,52 | 5,45 | 5,87 | 5,48 | 5,70 | |
| Северо-западное | 1 | 6,27±0,17 | 6,25 | 5,80 | 6,65 | 6,00 | 6,65 |
| 2 | 5,68±0,12 | 5,62 | 5,40 | 6,10 | 5,600 | 5,67 | |
| 3 | 5,86±0,13 | 5,98 | 5,42 | 6,15 | 5,72 | 6,02 | |
| Северное | 1 | 5,92±0,03 | 5,90 | 5,85 | 6,00 | 5,85 | 6,00 |
| 2 | 6,40±0,29 | 5,99 | 5,87 | 7,15 | 5,92 | 7,05 | |
| 3 | 6,16±0,06 | 6,18 | 5,98 | 6,30 | 6,11 | 6,25 | |
| Северо-восточное | 1 | 6,18±0,09 | 6,15 | 6,00 | 6,40 | 6,03 | 6,33 |
| 3 | 5,92±0,15 | 5,91 | 5,62 | 6,22 | 5,67 | 6,16 | |
| Восточное | 1 | 5,93±0,15 | 5,95 | 5,80 | 6,00 | 5,90 | 6,00 |
| 2 | 5,72±0,13 | 5,71 | 5,25 | 6,05 | 5,70 | 5,87 | |
| 3 | 5,70±0,06 | 5,68 | 5,55 | 5,85 | 5,58 | 5,84 | |
| Южное | 1 | 5,86±0,06 | 5,80 | 5,75 | 6,00 | 5,75 | 6,00 |
| 2 | 5,75±0,12 | 5,78 | 5,38 | 6,10 | 5,66 | 5,84 | |
| 3 | 5,68±0,07 | 5,72 | 5,50 | 5,84 | 5,55 | 5,81 |
1 – 4 марта 2001 г.; 2 – 30 декабря 2001 г.; 3 – 9 января 2003 г.
Несмотря на возрастание количества проб с кислыми значениями рН, следует отметить, что интерквартильный размах выборок по всем направлениям отбора укладывается в значения рН, соответствующие чистым и условно щелочным.
При анализе и сравнении данного показателя снеговых вод по направлениям целесообразно оперировать не средним, а медианным значением (небольшие выборки и относительно большой размах значений рН) – наиболее объективно отражающим тенденции изменения рН снега. Для северо-западного, северного и северо-восточного направлений характерны слабощелочные показатели (от 5,90 до 6,25) и для западного, восточного и южного – слабокислотные и нейтральные (от 5,52 до 5,95).
Для объективной характеристики величины рН осадков необходимо определить анионный и катионный состав снеговых вод. Результаты концентраций которых представлены в таблицах 3 и 4.
Определение содержания Cl-, SO42-, SO42-, HCO3- в пробах снеговой воды показало, что существует пространственная неравномерность содержания анионов в осадках. При сравнении результатов зонального распределения хлорид-иона наибольшие значения как по отдельно взятым пробам, так и по медианным значениям характерны для западного, северо-западного и северного направлений отбора, которые составляли от 1,44 до 20,35 мг/л и 1,70 до 11,90 мг/л соответственно. При принятых фоновых значениях 1,5–2,5 мг/л. Данная закономерность характерна и для сульфат-иона (1,52 до 18,88 мг/л и 1,52 до 6,19 мг/л) и нитрат-иона (0,01 до 16,38 мг/л и 1,38 до 5,10 мг/л). При фоновых значениях для сульфат-иона 7–9 мг/л и нитрат-иона – 0,5–1,5 мг/л.
Таблица 3. Средние концентрации ионов: хлорида, сульфата, нитрата и гидрокарбоната (мг/л) в снежном покрове
| Направление |
Период отбора |
Cl- |
SO42- |
NO3- |
HCO3- |
| Западное | 1 | 7,95±0,79 | 6,41±0,80 | 3,41±0,39 | – |
| 2 | 4,36±1,43 | 2,07±0,35 | 0,33±0,33 | 8,45±0,91 | |
| 3 | 7,33±1,63 | 3,69±1,71 | 2,02±0,37 | 13,28±0,62 | |
| Северо-западное | 1 | 12,0±22,53 | 3,80±0,46 | 5,55±0,83 | – |
| 2 | 4,0±01,44 | 7,08±2,37 | 0,52±0,20 | 10,46±1,52 | |
| 3 | 5,71±0,62 | 7,32±3,12 | 0,58±0,42 | 13,12±1,32 | |
| Северное | 1 | 8,46±3,05 | 5,66±2,19 | 4,90±1,17 | – |
| 2 | 3,41±1,66 | 2,40±0,35 | 0,49±0,11 | 9,94±1,43 | |
| 3 | 7,40±0,98 | 1,80±0,30 | 5,75±2,72 | 9,83±0,29 | |
| Северо-восточное | 1 | 4,56±0,15 | 1,24±0,15 | 1,61±0,13 | – |
| 3 | 3,65±0,22 | 1,12±0,22 | 1,54±0,08 | 8,52±0,95 | |
| Восточное | 1 | 2,74±0,62 | 1,70±0,43 | 1,05±0,25 | – |
| 2 | 0,50±0,21 | 1,98±0,29 | 0,47±0,20 | 10,44±2,62 | |
| 3 | 4,34±0,31 | 1,60±0,23 | 3,23±0,86 | 11,62±1,09 | |
| Южное | 1 | 5,81±1,54 | 3,12±1,51 | 1,31±0,39 | – |
| 2 | 4,69±2,13 | 1,27±0,10 | 0,09±0,50 | 12,74±0,79 | |
| 3 | 4,33±0,24 | 1,62±0,28 | 1,52±0,50 | 10,81±1,44 |
Полученные данные свидетельствуют, что средние концентрации основных кислотообразующих анионов характерных для западного, северо-западного и северного направлений отбора по отношению к северо-восточному, восточному и южному превышают в 1,5–4 раза. Это может быть объяснено тем, что он расположен в зоне влияния выбросов ТЭЦ‑2 ПОЭиЭ «Гомельэнерго», Гомельского химического завода, Гомельского стекольного завода, три домостроительных комбината. По данным Областного комитета охраны окружающей среды и природных ресурсов, на долю этих предприятий приходится до 76% суммарных выбросов соединений хлора, серы и азота, основных кислотообразующих анионов.
В тоже время результаты определения рН снеговых вод свидетельствуют о нейтральных и слабощелочных показателях рН осадков, выпадающих в зимний период в зоне влияния этих предприятий. Значит в снеговых водах должна быть более высокая концентрация катионного компонента, в состав которого могут входить твердые топливные частички (концентрация которых возрастает в зимний период) или другие катионы промышленного или территориального геологического происхождения.
Таблица 4. Средние концентрации ионов: калия, натрия, кальция и аммония (мг/л) в снежном покрове
| Направление |
Период отбора |
NH4+ |
K+ |
Na+ |
Ca2+ |
| Западное | 1 | 3,72±0,90 | 2,18±0,27 | 3,91±0,30 | 12,39±3,35 |
| 2 | 2,51±0,36 | 1,72±0,16 | 4,43±0,80 | 16,47±9,00 | |
| 3 | 2,56±0,51 | 4,41±0,76 | 5,82±0,67 | 8,07±1,50 | |
| Северо-западное | 1 | 3,66±1,46 | 3,36±0,76 | 5,28±0,98 | 10,37±2,06 |
| 2 | 1,52±0,22 | 1,10±0,14 | 3,88±0,94 | 5,44±1,60 | |
| 3 | 1,43±0,36 | 3,00±0,58 | 4,00±0,36 | 9,67±1,65 | |
| 1 | 2 | 3 | 4 | 5 | 6 |
| Северное | 1 | 3,34±0,33 | 3,50±0,34 | 5,820,22 | 17,34±2,35 |
| 2 | 1,30±0,32 | 1,09±0,07 | 4,69±1,33 | 4,32±1,57 | |
| 3 | 2,67±1,91 | 4,21±0,28 | 5,44±0,50 | 11,30±7,20 | |
| Северо-восточное | 1 | 2,38±0,39 | 3,21±0,27 | 4,00±0,69 | 10,33±2,83 |
| 3 | 0,37±0,18 | 2,05±0,90 | 2,56±0,83 | 2,75±0,24 | |
| Восточное | 1 | 2,51±0,56 | 4,35±0,49 | 6,42±0,27 | 6,86±0,78 |
| 2 | 1,29±0,06 | 1,47±0,16 | 1,76±0,09 | 2,58±0,34 | |
| 3 | 2,42±0,90 | 3,24±0,62 | 4,22±0,64 | 19,66±11,0 | |
| Южное | 1 | 2,24±0,80 | 4,35±0,22 | 6,32±0,61 | 10,58±0,78 |
| 2 | 1,97±0,38 | 1,84±0,19 | 2,42±0,16 | 4,48±2,37 | |
| 3 | 0,68±0,20 | 4,23±1,09 | 5,31±1,33 | 7,65±4,54 |
Для NH4+, K+, Na+, Ca2+- ионов характерна зональность распределения по различным периодам отборов как по отдельно взятым образцам, так и по направлению, как и для анионов.
При сравнении результатов зонального распределения иона-аммония наибольшие значения как по отдельно взятым пробам, так и по медианным значениям характерны для западного, северо-западного и северного направлений отбора, которые составляли от 0,04 до 10,08 мг/л и 0,43 до 4,40 мг/л соответственно. При принятых фоновых значениях – 0,25–0,75 мг/л. Данная закономерность характерна и для: Ca2+ (1,26 до 40,07 мг/л и 2,10 до 16,02 мг/л); K+ (0,75 до 6,92 мг/л и 1,21 до 4,02 мг/л) и Na+ (2,34 до 9,12 мг/л и 2,69 до 6,04 мг/л).
Для эффективной нейтрализации хлорида и других анионов ионов аммония, образовавшегося из газовой фазы недостаточно, так как соотношение эквивалентов NH4+ к остальным анионам намного меньше единицы. Значит в составе водорастворимой фракции атмосферных осадков необходимо значимое количество литофильных катионов (K+, Na+, Ca2+), вынесенных с земной поверхности или промышленных предприятий. Так как значения по данным катионам в 2–9 раз превышают фоновые, то основной вклад вносят промышленные предприятия, находящиеся в данном районе – Гомельский стекольный завод, три домостроительных комбината. По данным Областного комитета охраны окружающей среды и природных ресурсов, на долю этих предприятий приходится до 56% суммарных выбросов соединений в виде аэрозолей и пыли.
Для осадков, выпадающих в зимний период на данной территории, характерна зависимость – с увеличением концентрации и минерализации кислотообразующих анионов в снеговых водах прямо пропорционально возрастает и содержание нейтрализующих катионов, поэтому значения рН осадков близких к нейтральным.
Данные по химическому составу снеговых вод представлены в таблице 5.
Таблица 5. Содержание анионов и катионов (мг/л) в снеговых водах
| Ионы |
Период отбора |
Среднее | Медиана | Min | Max | 25% | 75% |
|
NH4+ |
1 | 3,00±0,34 | 2,81 | 0,74 | 9,11 | 0,74 | 9,11 |
| 2 | 1,72±0,15 | 1,46 | 0,30 | 3,88 | 1,32 | 2,03 | |
| 3 | 1,73±0,39 | 1,11 | 0 | 10,08 | 0,34 | 2,55 | |
|
K+ |
1 | 3,50±0,22 | 3,11 | 1,48 | 6,24 | 1,48 | 6,24 |
| 2 | 1,44±0,09 | 1,36 | 0,75 | 2,39 | 1,21 | 1,70 | |
| 3 | 3,58±0,31 | 3,65 | 1,11 | 7,07 | 2,21 | 4,94 | |
|
Na+ |
1 | 5,34±0,28 | 5,14 | 2,01 | 9,12 | 2,01 | 9,12 |
| 2 | 3,44±0,41 | 2,65 | 1,54 | 9,12 | 2,06 | 4,45 | |
| 3 | 4,63±0,35 | 4,72 | 1,56 | 8,44 | 3,11 | 5,98 | |
|
Ca2+ |
1 | 11,35±1,02 | 11,06 | 3,07 | 26,06 | 3,07 | 26,06 |
| 2 | 6,66±2,02 | 2,62 | 1,26 | 51,15 | 2,10 | 8,08 | |
| 3 | 10,10±2,41 | 4,70 | 1,65 | 60,31 | 3,39 | 10,31 | |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
|
Mg2+ |
1 | – | – | – | – | – | – |
| 2 | 0,91±0,07 | 0,82 | 0,64 | 2,39 | 2,39 | 0,75 | |
| 3 | 1,16±0,11 | 0,93 | 0,20 | 2,30 | 0,73 | 1,75 | |
|
Cl- |
1 | 7,01±0,89 | 4,85 | 1,50 | 20,35 | 4,10 | 8,40 |
| 2 | 3,39±0,69 | 1,70 | 0,03 | 11,83 | 1,05 | 6,87 | |
| 3 | 5,52±0,42 | 4,83 | 3,09 | 13,55 | 4,14 | 6,17 | |
|
SO42- |
1 | 3,74±0,57 | 3,10 | 0,75 | 14,14 | 1,50 | 4,90 |
| 2 | 2,96±0,62 | 1,67 | 0,92 | 14,46 | 1,50 | 3,06 | |
| 3 | 2,92±, 70 | 1,60 | 0,53 | 18,88 | 1,27 | 2,40 | |
|
NO3- |
1 | 3,02±0,42 | 2,40 | 0,55 | 9,25 | 1,40 | 4,10 |
| 2 | 0,38±0,09 | 0,31 | 0 | 1,64 | 0 | 0,42 | |
| 3 | 2,47±0,56 | 1,77 | 0 | 16,38 | 1,08 | 2,94 | |
|
NO2- |
1 | – | – | – | – | – | – |
| 2 | 0,19±0,14 | 0 | 0 | 3,35 | 0 | 0 | |
| 3 | 0,20±0,10 | 0 | 0 | 2,79 | 0 | 0 | |
|
PO43- |
1 | – | – | – | – | – | – |
| 2 | 0,84±0,37 | 0 | 0 | 6,11 | 0 | 0,36 | |
| 3 | 0,06±0,01 | 0,06 | 0 | 0,15 | 1,91 | 2,73 | |
|
F- |
1 | – | – | – | – | – | – |
| 2 | – | – | – | – | – | – | |
| 3 | 0,20±0,01 | 0,20 | 0,10 | 0,29 | 0,17 | 0,23 | |
|
HCO3- |
1 | – | – | – | – | – | – |
| 2 | 10,41±0,71 | 10,12 | 4,25 | 18,14 | 7,80 | 13,02 | |
| 3 | 11,29±0,50 | 10,91 | 6,33 | 16,25 | 9,46 | 13,19 |
1 – 4 марта 2001 г.; 2 – 30 декабря 2001 г.; 3 – 9 января 2003 г.
Широкое варьирование для каждого анализируемого аниона и катиона по отдельным стационарным площадкам в различное время отбора, видимо, можно объяснить «возрастом» снежного покрова. Так, в феврале 2001 г. были отобраны суммарные сезонные пробы снега, тогда как в декабре 2001 г. и в январе 2003 г. были отобраны суммарные декадные пробы. Разница в «возрасте» этих проб превышала 2,5 месяца, чем, по-видимому, и объясняются отличия концентраций анионов и катионов в пробах снеговой воды.
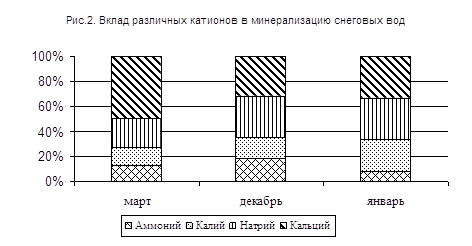
Процентный вклад различных ионов в суммарную минерализацию осадков приведен на рис 2 и 3.

Как видно из представленных данных, в атмосферных осадках зимнего периода изучаемого урбанизированного региона среди анионов наблюдается преобладание гидрокарбонат-ионов – от 73,5 до 57,5% (при сравнении снеговых вод декабря и января). Содержание SO42 – уменьшилось с 12 до 8% (в 0,5 раза), а Cl- и SO42 – увеличилось с 12,5 до 25,5% (2) и с 2,0 до 9,0% (4,5) соответственно.
Из катионов преобладают ионы кальция – с 50 до 32% и ионы натрия – с 23 до 34%.
Процентное содержание Ca2+ уменьшилось в 1,56 раза, а содержание Na+ увеличилось в 1,47 и K+ в 1,78 (с 14 до 25%). Для NH4+ такая закономерность не прослеживается – максимальное содержание во втором отборе 18%, а минимальное в третьем – 8%.
В порядке убывания вклада в минерализацию, ионный состав снеговых вод Гомельской городской агломерации можно представить в виде следующего ряда: HCO3-> Cl- > SO42- > NO3- или HCO3- > Cl- > NO3-> SO42 – (вклад PO43 – F – NO2 – менее 3%) – для анионов и Ca2+> Na+ > K+>NH4+ или Na+ >Ca2+ >K+ >NH4+ – для катионов.
Величину поступления анионов на единицу поверхности земли оценивали по фактическим данным о сумме выпадения осадков за сезон (таблица 6).
Таблица 6. Поступление анионов и катионов, мг/м2, с снеговыми водами на поверхность земли
| Ион | Дата отбора | ||
| 4 марта 2001 г. | 30 декабря 2001 г. | 19 января 2003 г. | |
|
Cl- |
329,63±45,26 | 139,95±27,71 | 210,26±15,56 |
|
SO42- |
173,93±28,70 | 130,20±34,64 | 112,00±26,82 |
|
NO3- |
138,94±19,46 | 16,35±3,87 | 96,72±23,70 |
|
NO2- |
– | 5,79±4,19 | 8,13±4,34 |
|
РО43- |
– | 0,84±037 | 2,37±0,29 |
|
HCO3- |
– | 429,23±33,81 | 433,89±20,49 |
|
NH4+ |
138,06±16,80 | 70,28±6,55 | 67,81±16,04 |
|
K+ |
157,77±9,87 | 57,87±3,22 | 136,86±12,20 |
|
Na+ |
243,07±12,17 | 147,29±21,66 | 177,71±13,97 |
|
Ca2+ |
517,25±53,41 | 268,93±76,62 | 396,65±97,34 |
Наибольшее количество с осадками на земную поверхность поступает среди анионов – гидрокарбонат-ионов до 463,04 мг/м2 –; хлоридов – до 225,82 мг/м2, сульфатов – до 164,84 мг/м2, нитратов – до 120,42 мг/м2; среди катионов – кальция – до 463,04 мг/м2; натрия – до 191,68 мг/м2; калия – до 167,64 мг/м2; иона-аммония – 154,86 мг/м2.
Распределение значений поступления катионов и анионов с осадками в зимний период на единицу площади несколько отличается от ряда их концентраций в снеговых водах. Это связано с толщиной снежного покрова в местах отбора проб, «возрастом» снега и другими факторами. Поэтому целесообразно оценивать фактические валовые концентрации ионов в снеговых водах. Концентрации исследуемых катионов и анионов по периодам составили: март 2001 – 34,47 мг/л; декабрь 2001 – 22,71 мг/л; январь 2003 32,47 мг/л. Превышение полученных значений над фоновыми составило от 2 до 5 раз.
Заключение
Для Гомельской городской агломерации и прилежащих территорий характерно зональное распространение основных кислотообразующих анионов и катионов в снежном покрове. Максимальные концентрации ионов и, как следствие, минерализация снеговых вод характерны для западного, северного и северо-восточного направлений, в зоне влияния северного промышленного узла, в 0,75–3,87 раза больше, чем в остальных районах. Среди анионов доминируют гидрокарбонат и хлорид, а среди катионов – кальций и натрий, которые вносят от 51 до 72% в общую минерализацию осадков.
Общее поступление ионов со снеговыми водами на поверхность земли составляло от 893,7 до 1462,4 мг/м2 в зависимости от периода отбора и направления удаления от города. По валовому содержанию катионов и анионов в снеговых водах, а также величины поступления на единицу площади Гомель и прилегающие районы относятся к высокоурбанизированной территории. Повышенное содержание основных кислотообразующих анионов (в 2–4 раза больше фоновых) полностью нейтрализуются ионом-аммония и литофильными катионами.
Комплексное изучение ионного состава снеговых вод Гомельского района не свидетельствуют о наличии кислотных осадков, выпадающих в холодный период времени. Необходимо выяснить как большая минерализация осадков может влиять при активном снеготаянии в весенний период на окружающую среду (биоту, поверхностные воды, миграцию металлов в почве).
1. Зайков Г.Е., Маслов Н.А., Рубайло В.Л. Кислотные дожди и окружающая среда. – М.: Химия, 1991. – 144 с.
2. Кислотные дожди / Ю.А. Израэль, И.М. Назаров и др. – Л.: Гидрометеоиздат, 1989. 271 с.
3. Ченяева Л.Е., Черняев А.М., Могилевских А.К. Химический состав атмосферных осадков (Урал и Приуралье). – Л.: Гидрометеоиздат, 1978. – 180 с.
4. Кислотные выпадения. Долговременные тенденции. / Пер. с англ. Под ред. Ф.Я. Ровинского, В.И. Егорова Л.: Гидрометеоиздат, 1990. – 184 с.
5. РД 52.04.86–89. (руководящий документ). Методические указания по определению химического состава осадков // Руководство по контролю загрязнения атмосферы. – Л.: Гидрометеоиздат, 1991. – 725 с.
6. Лавриненко Р.Ф. Осреднение значений рН атмосферных осадков с учетом щелочных и кислотных компонентов их состава // Мониторинг фонового загрязнения природных сред. Выпуск 6. – Л.: Гидрометеоиздат, 1990. – С. 130–139.
© 2010 Интернет База Рефератов